引起库欣综合征(CS)的病因很多,具体的治疗方法也有不同(如下图)。
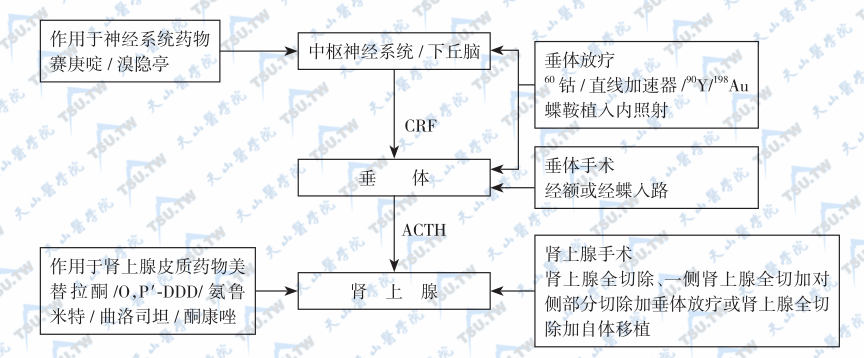
Cushing 库欣综合征病治疗方案的选择
手术摘除垂体ACTH瘤
被MRI确诊的Cushing病的治疗基本原则是手术或放射治疗,降低ACTH分泌,减轻肾上腺增生,使皮质醇分泌减少而达到治疗目的。目前,对于MRI阴性(约占40%)而临床能确诊的Cushing病的首选治疗亦是垂体手术,但宜采用内镜下探查,以扩大视野和探查范围。如上述方法无效,可以加用调节神经递质或抑制皮质醇合成的药物减少皮质醇合成;如仍不能控制,可施行双肾上腺切除术,术后终生接受糖皮质激素替代治疗。
垂体手术方式
一般分为以下3种情况。
- 垂体微腺瘤摘除术:由于近年显微外科技术的不断发展及术中采用电视监视,加上术中B超定位和分段分区采血测定ACTH,垂体微腺瘤的定位准确性较前明显提高。现多采用经蝶窦垂体微腺瘤切除术,此方法手术创伤小,手术及术后并发症少,可最大限度地保留垂体分泌功能,治愈率80%~90%,术后复发率10%~30%,而无经验操作者失败率也可能相当高。Meller等成功经蝶窦选择性垂体微腺瘤切除手术治疗Cushing病并妊娠患者。多数在术后发生一过性垂体-肾上腺皮质功能减退,宜补充糖皮质激素治疗,直至功能恢复。常见的并发症有一过性尿崩症、脑脊液鼻漏、出血、感染、颅高压等;还有报道并发低钠血症者,后者多见于伴鞍内扩散的年轻男性患者。
- 垂体大腺瘤摘除术:由于垂体大腺瘤的生物学特性为浸润性生长,易向垂体外、鞍上扩展,体积大,宜选用开颅手术,尽量切除肿瘤组织,但往往难以完全清除,术后宜配合放射治疗或药物(化学)治疗。垂体大腺瘤的治疗效果及预后由其浸润性生长特性决定,临床综合治疗可缓解患者症状,延长生命。
- 垂体腺癌和异位神经节瘤摘除术:垂体腺癌和异位神经节瘤引起Cushing病者极少见。条件允许时应尽可能开颅手术切除癌肿,防止肿瘤扩大和转移。
垂体ACTH瘤摘除术治愈/缓解标准
Cushing病儿童在经蝶手术后应接受疗效评价以估计预后和复发可能性。尿游离皮质醇降低不是可靠的预测指标,而ACTH和oCRH试验可用于预后评估。目前更强调在未使用糖皮质激素情况下,测定术后数小时至2天内的血清皮质醇水平。垂体ACTH瘤摘除术治愈/缓解的一般标准是:①血清皮质醇5~7μg/dl;②依赖于外源性糖皮质激素的时间>6个月;③皮质醇和ACTH对CRH或DDAVP缺乏反应;④DXM抑制试验恢复正常;⑤皮质醇昼夜节律恢复。符合以上各点越多,术后复发的可能性越低。由于正常垂体组织长期被高皮质醇血症抑制,术后必然出现低皮质醇血症。因此,血皮质醇降低本身就是手术成功的标志,但如果患者术前的高皮质醇血症不严重,或使用了大量药物或合并其他疾病,术后血皮质醇亦可正常。在使用生理量DXM情况下,建议术后第1周测定晨间血皮质醇,如果术后使用糖皮质激素则主要根据症状和体征估计病情。
如果术后多次测定的晨间血皮质醇<2μg/dl(50nmol/L)可认为病情缓解,不需要做进一步的监测和评估(复发率为10%/10年);如果血皮质醇介于2~5μg/dl,或尿游离皮质醇在20μg/24h(55nmol/24h)以下,亦可认为已经缓解。晨间血皮质醇>5μg/dl(140nmol/L)或尿游离皮质醇>100μg/24h,且持续6周以上,提示仍未治愈或已经复发,需要做进一步的病情评估和长期追踪。
垂体ACTH瘤摘除术后CS复发与术后并发症
垂体瘤摘除术后复发较常见,其原因是:①由于手术难度大或摘除技术等原因而未能去除全部垂体瘤组织;②分泌ACTH的垂体瘤恶变或垂体癌复发;③肾上腺存在自主功能性结节(血ACTH测不出)。对垂体瘤术后复发者要根据病因分别进行放疗、药物治疗、再次垂体手术或肾上腺自主功能结节切除。
GH缺乏症的发生率较高,部分患者的GH缺乏症为永久性。GH缺乏症亦见于垂体放疗后,但发生率较低。儿童CS患者在垂体瘤摘除术后应密切观察血GH变化,必要时,应根据病情补充GH,以防止发生生长发育障碍。
垂体ACTH瘤术后药物治疗
手术期间常规给予氢化可的松。术后改用替代剂量的糖皮质激素,一般在术后第4天停药,次日上午9时采血测定皮质醇,由于ACTH瘤抑制垂体剩余的ACTH细胞,故在腺瘤摘除后,血皮质醇<30nmol/L(1μg/dl)者提示需用糖皮质激素替代治疗。如果皮质醇不能被抑制,即使此时的血皮质醇已经降至正常以下,也说明ACTH瘤未被“治愈”(尤其是儿童患者),这些患者必须严密追踪,并定期评价垂体功能。
放射治疗无法定位的垂体微腺瘤和不能手术的大腺瘤及Nelson综合征
放射治疗垂体瘤在20世纪60年代显示了其治疗作用;80年代的资料表明,放疗可减少垂体瘤术后复发率。由于垂体瘤摘除术快速发展,垂体放射治疗已很少单独应用,现仅作为Cushing病的辅助治疗方法,常用于无法定位的垂体微腺瘤、因各种原因不能施行垂体手术的大腺瘤、Nelson综合征或腺癌术后。经改进放射治疗技术,减少照射野周围组织损伤,γ刀及X刀的应用增多,但缺乏远期效果、术后并发症及对机体影响的观察结果。
在临床上,如果Cushing病已经确诊,但找不到垂体肿瘤依据(MRI阴性)时,必须重新评价诊断;如确系无误,仍然首选经蝶垂体微腺瘤(ACTH瘤)切除术。内镜探查蝶鞍全部,并重点视察中部海绵窦壁。当MRI不能发现放射治疗点时,可对全蝶鞍区进行放疗。60钴(60Co)或(和)直线加速器都有一定效果,50%~80%的Cushing病病情缓解,一般在放疗后6个月出现疗效。还可用内照射治疗垂体瘤,将放射性物质(198Au、90Y等,其中90Y放射单一的β射线,无γ射线,对垂体周围组织无损伤作用)植入蝶鞍进行放射治疗,但因需要手术进行,目前很少应用。
由于放射治疗的副作用有组织放射性水肿,故不宜作为大腺瘤、已有或可能有视交叉压迫患者的首选治疗方法。Cushing病多次垂体放疗后出现头痛、头晕及耳鸣等不适反应,考虑为放射性脑损伤所致。随着时间延长,可出现部分性或全垂体功能低下,首先是促性腺激素和GH分泌不足,随后是促甲状腺激素、促皮质激素缺乏,需终身激素替代治疗。长期随访的发生率20%~60%。放疗后脑部恶性病变的报告有增加趋势,除神经胶质瘤外,还可发生星状细胞瘤、脑膜瘤及多发性动脉瘤等。
肾上腺切除缓解Cushing病
肾上腺切除术是Cushing病的传统治疗方法,目前已不作为首选。肾上腺结节既可见于Cushing病,也可能是Cushing病合并肾上腺“意外瘤”。而Cushing病引起的肾上腺皮质增生又可分为弥漫性增生、结节性增生和瘤样增生等多种形式;尤其在双侧增生不对称时,其病因鉴别相当困难。除肾上腺皮质自主性结节外,Cushing病所致的肾上腺皮质增生均在垂体手术后自发消退,不必手术治疗。而肾上腺皮质自主性结节必须手术切除。所以,在实施肾上腺切除术前,必须仔细将肾上腺增生性结节和腺瘤鉴别开来。
切除方法
主要适用于非CRH/ACTH依赖性CS,即肾上腺皮质醇瘤、自主结节性增生和Cushing病行垂体瘤手术失败者。肾上腺切除术方法包括肾上腺次全切除术、全切除术和肾上腺切除后自体移植术等。当Cushing病经垂体手术、放疗等治疗无效时,最终可选择肾上腺全切术,95%患者可获缓解。可以经腰部切口入路或腹腔镜进行手术。腹腔镜手术可以经腹腔或经腹膜后两种方法。腹腔镜方法手术创伤小,减少术中腹部并发症,术后恢复快,可作为肾上腺切除的新方法。但技术要求较高,凡有腹部手术史或心肺功能差者,经腹膜后腹腔镜方法更合适。术中应静脉给予氢化可的松,术后3~7天改为维持量。一般于术后第5天检测血皮质醇(检测日停用氢化可的松),如血皮质醇<30nmol/L(1μg/ dl),应给予糖皮质激素替代治疗。如果虽然血皮质醇正常,但不能被DXM抑制,亦提示手术治疗失败或仅部分有效,成人CS的复发率约2%,儿童CS复发率可达40%。因此,手术后必须对垂体-肾上腺功能进行重新评价和定期追踪。
对诊断Cushing病而垂体MRI未发现微腺瘤者、因年龄大或其他某种原因不能作垂体手术而病情严重者,宜作肾上腺次全切除术,加术后垂体放射治疗。病情轻者用药物加垂体放射治疗控制肾上腺皮质激素过度分泌。术前无法预测治疗后是否发生Nelson综合征,故提倡定期随访并复查垂体MRI。
不良反应和并发症
肾上腺全切除术后可明显缓解高皮质醇血症,但术后易出现肾上腺皮质功能低下,需终身服糖皮质激素替代治疗。部分患者(10%~40%)术后发生Nelson综合征,即出现垂体分泌ACTH肿瘤或原有的微腺瘤快速增生成大腺瘤,血ACTH明显升高,皮肤色素沉着加深。为了避免终身替代服药及Nelson综合征,有人提出肾上腺次全切除术,即一侧肾上腺全切除,对侧肾上腺大部分切除,而单侧肾上腺全切后不需要用糖皮质激素替代治疗。其缺点是肾上腺切除多少的尺度难以掌握。其中部分患者在病情缓解一段时期(数月或数年)后又复发,小部分发生肾上腺皮质功能不全和垂体瘤。Nelson综合征是Cushing病患者行双侧肾上腺切除后的重要并发症。进行性加重的皮肤黏膜色素沉着是本征最主要特点,蝶鞍或鞍外组织受压时表现为头痛、视力减退、视野缩小、眼睑下垂、眼底视乳头水肿和视神经萎缩。多数患者血浆ACTH基础值>500pg/ml,同时血皮质醇显著降低。头颅X线摄片可显示蝶鞍扩大、骨质破坏或肿瘤征象。
术后处理
为了防止术后并发肾上腺皮质功能减退症和Nelson综合征,可将切下的肾上腺作自体移植。移植的肾上腺组织可能存活下来,而原有的肾上腺皮质功能亢进获得缓解。具体方法是:将切下的两侧增生肾上腺在低温容器中切成若干小块,分别移植于两侧缝匠肌中,手术准备同肾上腺切除术。术后仍作激素替代治疗,密切观察下逐渐减少剂量以至停用,小部分患者的CS症状迅速减轻或消失,血皮质醇、UFC、尿17-OHCS降至正常或略低于正常水平,但大多数由于移植组织未存活,仍需终身糖皮质激素替代治疗。
CS患者手术治疗后补充糖皮质激素的判断指标为:血皮质醇和ACTH水平正常者不必补充糖皮质激素;如血皮质醇降低而ACTH升高,需要补充糖皮质激素。糖皮质激素补充治疗过程中,评价补充糖皮质激素的量是否合适的指标主要是症状、血电解质和ACTH,血皮质醇不能作为判断指标。部分患者无肾上腺皮质功能减退的临床表现,血皮质醇和ACTH亦正常,但有不同程度的精神症状,其原因未明,可能是一种戒断反应。对这些患者不宜再给予外源性糖皮质激素。肾上腺次全切除术后,患者的HPA轴形态与功能的恢复需要数月至数年时间。一般主张早晨服用亚生理量地塞米松0.5mg/d,并在服用地塞米松前定期(数周1次)测定血皮质醇,当达到或超过180nmol/L(6.5μg/dl)时即可停用地塞米松。必要时可用胰岛素耐量试验了解患者对应激的反应性,如反应性低下,必须告诫患者应激时增加地塞米松用量。
药物控制CS
用于CS治疗的药物分为类固醇合成阻滞剂、糖皮质激素受体拮抗剂、血清素受体拮抗剂、GABA神经能激动剂、多巴胺受体激动剂、生长抑素类似物和PPAR-γ激动剂7类(参见此表),应用最多的皮质醇合成抑制药物见下表。
抑制皮质醇合成药物

- 美替拉酮:是目前应用最多的药物。美替拉酮(metyrapone)对皮质醇合成的多种酶有抑制作用,主要阻滞11β-羟化酶,抑制了皮质醇合成的最后步骤。适于术前准备或危重患者无法手术者。0.5~4.0g/d,建议用牛奶冲服。此药副作用少,仅轻度头痛、头昏,有的患者有消化道症状、皮疹等,对肝脏与骨髓无毒性。观测疗效指标应为血皮质醇含量,而测定尿17-OHCS无临床意义。
- 米非司酮:米非司酮(mifepristone,RU486)为糖皮质激素受体拮抗剂,与糖皮质激素受体结合而阻止皮质醇的作用,并可抑制21-羟化酶活性。每日5~30mg/kg可明显改善症状,因作用迅速,尤其适应于皮质醇引起的应激性精神症状患者,血皮质醇/ACTH和雄激素进一步升高而血皮质醇及UFC下降。但有头痛、乏力、厌食、恶心、肌肉和关节疼痛、直立性低血压等,肾上腺皮质功能不全、子宫内膜增生(抗孕激素作用所致)、闭经、男性乳腺发育、低钾血症等不良反应较常见,经少量补充糖皮质激素治疗即可消失。应用该药治疗时,因不能用血皮质醇或ACTH作为疗效的评价指标(米非司酮使血ACTH和血皮质醇升高),一般主要根据临床表现(体重、血压、皮肤改变、血钾等)进行判断,而且药物导致肾上腺皮质功能减退后,难以发现和诊断。
- 米托坦:米托坦(密妥坦,邻对氯苯二氯乙烷,mitotane,O,P′-DDD)是一种毒性较小的DDD异构体,其活性比DDD 大20倍。该药除抑制皮质醇合成的多种酶外,还直接作用于肾上腺,使肾上腺发生出血、坏死或萎缩,尿17-OHCS、醛固酮、雄激素等排泄量减少。由于O,P′-DDD诱导肾上腺皮质功能不全,于用药(每日50~75mg/kg)的第3天起要补充糖皮质激素和盐皮质激素。
- 氨鲁米特:氨鲁米特(氨基导眠能,aminoglutethimide)为3β-羟脱氢酶及11β-羟化酶阻滞剂,抑制胆固醇向孕烯醇酮转换。剂量0.5~1.0g/d,分次口服。副作用有食欲减退、发热、皮疹及嗜睡。由于其可阻止碘代谢,故不能长期使用。
- 依托咪酯:依托咪酯(etomidate)是一种新的中枢神经镇静与抗惊厥药物,有时也用于手术麻醉。本药的最明显副作用是抑制肾上腺皮质功能,据说该药治疗重症疾病伴高皮质醇血症能取得较好效果。
- 生长抑素类似物:pasireotide(SOM230)是一种新的多靶向生长抑素类似物,可与5个生长抑素受体中的4个结合,尤其是与SSTR5(主要在ACTH瘤细胞表达)呈高亲和性结合。初步的观察发现,对Cushing病有良好疗效。
- 皮质醇合成抑制剂:老年人难以耐受手术治疗,用皮质醇合成抑制药为控制高皮质醇血症的有效选择。酮康唑(ketoconazole)抑制线粒体细胞色素P450依赖酶(如胆固醇碳链酶和11β-羟化酶),阻断皮质醇及醛固酮合成。剂量0.2~1.8g/d,从小剂量开始,分次口服,维持量0.6~0.8g/d。副作用有消化道症状,恶心、发热、肝功能受损等。
- 多巴胺激动剂与血清素拮抗剂:多巴胺激动剂(如溴隐亭,bromocriptine)或血清素拮抗剂(如赛庚啶,cyproheptadine)对CRH/ACTH依赖性CS有一定效果,尤其适用于周期性CS的治疗。
- 降糖药物:胰岛素增敏剂可降低围术期并发症的发生率,但患者能否从长期治疗中获益有待进一步研究。并发或合并糖尿病时,在降低血皮质醇水平的同时,加用抑制皮质醇合成的药物,如甲吡酮、酮康唑或米托坦;降低血糖的药物可选择二甲双胍或胰岛素。
抑制皮质醇合成药物的作用机制及用法参见此表。Cushing病的治疗需要采取综合方案,如各种治疗方法配合适当,不仅可提高疾病的治愈率,还可减少不良反应如腺垂体功能减退及Nelson综合征等的发生率。除上述综合治疗方案外,随着Cushing病病因、发病机制研究的深入,Cushing病可能与遗传、基因改变有关。在此基础上,有人提出在手术、放疗的基础上加基因治疗,有可能成为治疗垂体肿瘤的新途径。Frankel等将反义寡核苷酸链试用于抑制ACTH分泌以治疗Cushing病和异源性CRH/ACTH分泌综合征,取得一定效果。
