脂质是体内的一种重要组成成分,广泛存在于各种生物膜(如细胞浆膜和细胞器膜)的结构中。脂质为疏水性分子,不溶或微溶于水,在维持细胞完整性方面具有非常重要的作用,并可使血浆中物质通过直接弥散或经载体转运进入细胞。同时,脂质是体内能量贮存的主要形式,也是肾上腺和性腺类固醇激素以及胆酸合成的前体物质。此外,脂质还是血液中许多可溶性复合物运输的载体。
血脂谱异常分类
脂质分为脂肪酸(fatty acids,FA)、甘油三酯(triacylglycerol,TG)、胆固醇(cholesterol,Ch)和磷脂(phospholipides,PL)等类型。其中,TG和PL为复合脂质。血浆中的胆固醇又分游离胆固醇(free cholesterol,FC)和胆固醇酯(cholesterol ester,CE)两种,两者统称为血浆总胆固醇(total cholesterol,TC)。根据分子长度及双键数目和位置的不同,脂肪酸(fatty acids)可进一步分为不含双键的饱和脂肪酸(saturated fatty acids)与含有双键的不饱和脂肪酸(unsaturated fatty acids),后者包括单不饱和脂肪酸(monounsaturated fatty acids)和多不饱和脂肪酸(polyunsaturated fatty acids)。脂肪酸是机体能量的主要来源,在组织中通过酯化作用(esterification)转变为复合脂质,并可与蛋白质结合形成脂蛋白复合物(protein-lipid complex,PLC),或以非酯化脂肪酸与白蛋白结合后在血液中转运。
胆固醇
胆固醇具有4个碳氢环结构和1个8碳的侧链,它是细胞膜结构中的主要组成成分,也是类固醇激素和胆酸合成的前体物质。血液中的胆固醇约有2/3以酯化形式存在。
一:胆固醇的生物合成
由乙酸开始,首先由3分子乙酸缩合成3-羟-3-甲基戊二酰辅酶A(HMG-CoA),后者在HMG-CoA还原酶的作用下转变为甲羟戊酸(mevalonic acid)。经过一系列步骤,甲羟戊酸最后转变成胆固醇。HMG-CoA还原酶是胆固醇生物合成过程中的限速环节。除了HMGCoA还原酶的竞争性抑制剂可以减少胆固醇合成外,细胞内胆固醇升高亦可反馈抑制HMG-CoA还原酶的活性。反之,胆固醇降低可增加HMG-CoA还原酶活性。
二:胆固醇的分解
胆固醇不能被分解为CO2和H2O,只能以游离胆固醇的方式分泌进入胆汁,或转变为胆酸后排入肠道。进入肠道的胆固醇约50%通过重吸收再回到肝脏,其余部分则从粪便排出。小肠中的胆酸(cholic acid)有97%通过重吸收重新回到肝脏。两者共同构成肠-肝循环。通过重吸收胆固醇和胆酸可抑制肝内胆固醇和胆酸的合成。在胆酸合成过程中,胆固醇的7α-羟化酶(7α-hydroxylase)是调节游离胆固醇转变为7α-羟胆固醇的限速酶,由503个氨基酸残基构成,分子量57kD,并受再循环胆酸的调节。7α-羟化酶与HMG-CoA还原酶的活性变化往往是平行的,以维持细胞内胆酸合成所需胆固醇浓度的相对恒定。
三:胆固醇合成的调节
血液中的胆固醇的水平主要受低密度脂蛋白(low density lipoprotein,LDL)受体的调节。此受体分布于全身所有细胞表面,并调节细胞从血液中摄取富含胆固醇的脂蛋白(如LDL)。一些脂蛋白(如载脂蛋白B100和载脂蛋白E)表面的特异性蛋白可与LDL受体相互作用,促进脂质利用。LDL主要在肝脏进行分解代谢,肝细胞通过LDL受体摄取LDL和清除血清胆固醇。细胞内的胆固醇水平对细胞表面的LDL受体数目有直接影响。当细胞内胆固醇升高时,LDL受体的表达随即减少;反之,LDL受体数目增加。细胞内胆固醇在酰基辅酶A胆固醇酰基转移酶(acyl coenzyme A acyltransferase,ACAT)的作用下进行酯化。ACAT通过酯化细胞内的游离胆固醇而促进肠道内游离胆固醇的摄取,并由此产生和维持游离胆固醇的跨膜浓度梯度。
甘油三酯
甘油三酯(TG)由3个脂肪酸分子和1个甘油分子通过酯化作用形成,在脂肪组织中以脂肪滴(fat drop)的形式贮存,也可作为某些脂蛋白的组成成分在血液中转运。脂肪细胞或脂蛋白颗粒中的TG水解后,释放非酯化脂肪酸,以提供能量。甘油中的3个羟基与2分子脂肪酸和1分子磷酸盐(磷脂酸)进行酯化后形成的复合物称为磷脂(phospholipids)。通常,磷脂酸(phosphatidic acids)与一种亲水性胆碱、丝氨酸或胆胺等酯化,形成磷脂酰胆碱(phosphatidylcholine;卵磷脂,lecithin)、磷脂酰丝氨酸(phosphatidylserine)或磷脂酰胆胺(phosphatidylcholamine)等。磷脂中的疏水部分与亲水部分结合后,可以融合于水与脂质之间的界面,因此是各种膜和脂蛋白表面结构的重要组分。
一:脂蛋白脂酶(lipoprotein lipase,LPL)的调节
通过LPL作用,可使乳糜微粒(chylomicrons,CM)和极低密度脂蛋白(VLDL)中的TG释放出非酯化脂肪酸。在邻近脂肪、肌肉和乳腺组织的毛细血管内皮细胞内,LPL将脂肪酸从脂蛋白的TG中游离出来。为满足组织对非酯化脂肪酸的各种需要,但不同组织的LPL功能有所不同。例如,空腹时脂肪组织中LPL水平较低,而心肌LPL水平较高,分娩前乳腺组织中LPL水平一直很低,但哺乳期的LPL水平较非哺乳期升高10倍以上。
二:葡萄糖和胰岛素的调节
高水平的葡萄糖和胰岛素促进脂肪组织中的非酯化脂肪酸转变为TG,以贮存能量。当以糖类取代饮食中的脂肪时,胰岛素和葡萄糖还可刺激肝内的非酯化脂肪酸合成,使其转化为TG并包裹在VLDL中。胰岛素通过增加磷酸甘油(phosphoglycerol)的生成而增加LPL的活性,刺激脂肪酸酯化,并通过对胰岛素敏感性酯酶(insulin-sensitive esterase)的抑制作用减少非酯化脂肪酸的生成。在缺乏胰岛素的情况下,LPL活性降低。
三:其他因素的调节
在许多情况下,如应激、运动、禁食以及未控制的糖尿病等,脂肪中的TG释放出非酯化脂肪酸和甘油(glycerine)。此过程取决于调节激素作用。与许多激素的作用相反,胰岛素对脂肪组织中的酯酶具有抑制作用。生长激素则通过增加酯酶的生物合成而使脂肪酸从TG中游离出来。脂肪酸进入血液循环与血清蛋白结合形成复合物。在剧烈运动和内脏血管床的血流减少时,非酯化脂肪酸主要集中于肌肉组织。在不同代谢状态下,非酯化脂肪酸被肝脏再摄取后用于TG或磷脂合成、氧化为CO2或转化成酮体,而释放出来的甘油则被肝脏和肾脏摄取,用于TG合成和糖原生成。
脂肪细胞脂肪代谢
脂肪细胞中脂肪的代谢以循环方式进行,脂肪合成与脂肪分解维持动态平衡。如合成大于分解,脂肪贮存增加,脂肪细胞肥大,形成肥胖;反之脂质消耗增加,贮存的脂质减少,体重下降。脂肪细胞的脂代谢见图5-33-1。除极长链脂肪酸的氧化是在过氧化物酶体内进行外,其他脂肪酸的氧化及酮体生成均在线粒体内进行。由于非酯化脂肪酸及其CoA衍生物只能通过线粒体膜的外层,因而只能在线粒体膜内转化成肉碱衍生物后才可穿膜转运。进入线粒体内再转变为CoA衍生物,并经过β氧化产生乙酰CoA和还原型烟酰胺腺嘌呤二核苷酸(NADH)及黄素腺嘌呤二核苷酸(FADH)。NADH和FADH随非酯化脂肪酸进入电子传递系统,形成ATP和水。乙酰CoA与草酰乙酸缩合成枸橼酸盐进入三羧酸循环,然后被氧化成CO2,或被转运至线粒体外,或再次转化为非酯化脂肪酸。在长时间禁食和糖尿病未得到控制等情况下,胰岛素不足使非酯化脂肪酸大量进入肝脏,导致VLDL-TG生成减少,线粒体内NADH、FADH和乙酰CoA大量堆积,并使乙酰乙酸、β-羟丁酸和丙酮生成增多。
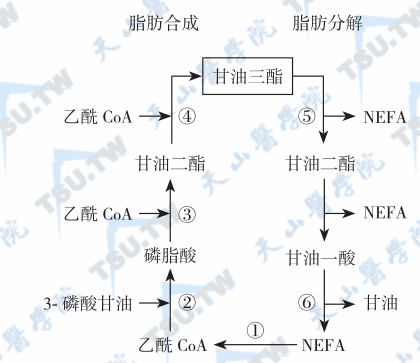
脂肪细胞中脂代谢循环
注:①乙酰CoA合成酶;②3-磷酸甘油酰基转移酶;③磷脂酸磷酸水解酶;④甘油二酯酰基转移酶;⑤甘油三酯脂肪酶;⑥甘油一酯脂肪酶。NEFA:非酯化脂肪酸。
酮体的生成包括以下几个步骤。首先,乙酰CoA经缩合转变成乙酸乙酰CoA和HMG-CoA;HMG-CoA再与乙酰乙酸和乙酰CoA结合,释放出CoA,并进行非酯化脂肪酸的β-氧化。通过NADH形成β-羟丁酸后可降低乙酰乙酸的水平,而所产生的NAD可继续用于脂肪酸的β-氧化。此外,乙酰乙酸亦可分解为丙酮。酮体积累过多引起酮症酸中毒。
脂蛋白分类
从肠道消化吸收的和在肝脏合成的脂质必须以脂蛋白形式才能在血液中转运,进而为机体各组织所利用或贮存。脂蛋白中的脂质包括甘油三酯、胆固醇酯、游离胆固醇和磷脂。此外,脂蛋白还可转运脂溶性维生素、某些药物、病毒和抗氧化酶。
脂蛋白呈球形颗粒状结构,其核心为疏水性脂质(甘油三酯和胆固醇酯),表层由亲水的蛋白质、游离胆固醇和磷脂等成分构成。通常,脂蛋白可分为乳糜微粒(chylomicron,CM)、乳糜微粒残粒(CM cruel)、极低密度脂蛋白(VLDL)、低密度脂蛋白(LDL)、中密度脂蛋白(intermediate density lipoprotein,IDL)和高密度脂蛋白(HDL)等6种不同的类型,其在脂质转运中的作用各不相同,见下表。
血浆脂蛋白的分类
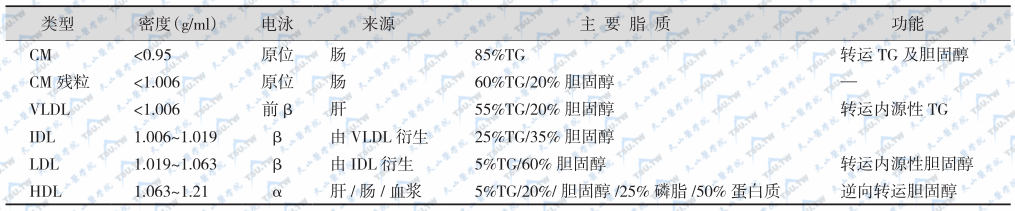
注:IDL:中密度脂蛋白胆固醇;VLDL:极低密度脂蛋白;LDL:低密度脂蛋白;HDL:高密度脂蛋白;TG:甘油三酯;Ch:胆固醇。
乳糜微粒(CM)
乳糜微粒是血浆中颗粒最大的脂蛋白。其脂质含量高达98%~99%(其中85%~90%为TG),蛋白质占1%~2%,在未离心的血浆中处于漂浮状态。乳糜微粒含有ApoB48、ApoAⅠ、ApoAⅣ、ApoE及ApoC等多种载脂蛋白,其特异性载脂蛋白为ApoB48。其主要存在于餐后血浆中,正常人的过夜空腹血浆中看不见乳糜微粒。
乳糜微粒是在十二指肠和空肠上段上皮细胞的高尔基体中由TG、磷脂和胆固醇共同形成的。新合成的乳糜微粒中有ApoB48、ApoAⅠ和ApoAⅣ等载脂蛋白。在血液中,经过脂蛋白脂酶的作用,乳糜微粒中的TG释放出非酯化脂肪酸,其后转化成为少TG和富胆固醇的乳糜微粒残粒。在肝脂酶的作用下,乳糜微粒残粒被肝细胞摄取,从血浆中被迅速清除(下图)。
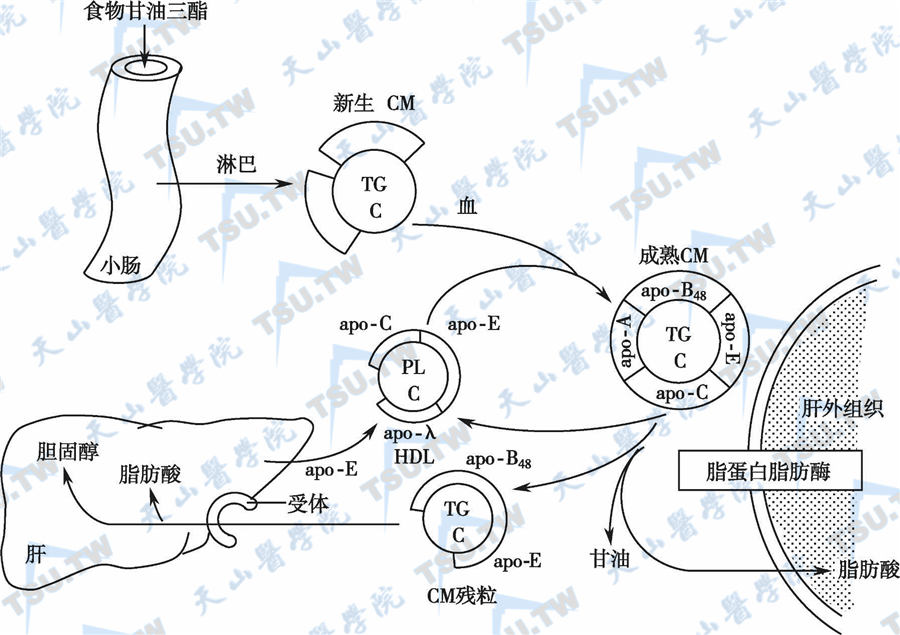
乳糜微粒的代谢
注:CM:乳糜微粒;TG:甘油三酯;C:胆固醇;PL:磷脂。
极低密度脂蛋白(VLDL)
VLDL由85%~90%的脂质(其中55%为TG、20%为胆固醇和15%为磷脂)和10%~15%的蛋白质构成,位于离心血浆的表层。其特异性载脂蛋白为ApoB100。此外,还有ApoE和ApoC。VLDL通过在肝脏利用TG和磷脂合成而来。来自饮食脂肪或由空腹和未控制的糖尿病脂肪组织中的脂肪酸动员而产生的非酯化脂肪酸,可增加VLDL合成。在脂蛋白脂酶和肝脂酶的作用下,VLDL TG被水解为颗粒较小而胆固醇含量更多的中密度脂蛋白(IDL)。IDL丢失了多数的ApoC,而保留了ApoB100和ApoE。通过肝脂酶的继续作用,IDL被降解为LDL。约有一半的VLDL最终转化为LDL,其余的一半是以VLDL残粒和IDL的形式直接被肝脏清除。肝细胞摄取VLDL残粒和IDL 受ApoE调节。
低密度脂蛋白(LDL)
LDL是血浆中胆固醇含量最高的脂蛋白,约70%的血浆总胆固醇存在于LDL中。在LDL中,脂质占75%(胆固醇酯约占35%,游离胆固醇占10%,TG占10%和磷脂占20%),其余25%为蛋白质(主要为ApoB100和少量的ApoE)。如前所述,LDL是VLDL水解后的最终产物,肝脏摄取75%左右,其余部分为其他组织所摄取。近2/3的LDL摄取受LDL受体的调控,但其具体过程尚不清楚。LDL具有较强的致动脉粥样硬化作用。
高密度脂蛋白(HDL)
HDL主要来源于肝、肠和乳糜微粒与VLDL的分解。HDL是一种很小的颗粒,由50%的脂质(其中磷脂25%,胆固醇酯15%,游离胆固醇和TG各占5%)和50%的蛋白质构成。其主要蛋白质为ApoAⅠ(65%)、ApoAⅡ(25%)和少量的ApoC与ApoE。
HDL可分为3个亚类,以HDL2和HDL3为主。由于两者都缺乏ApoE,所以均不能与LDL受体结合。HDL1是体内的ApoE库,血浆中的ApoE中有50%存在于HDL1中。HDL有3种主要来源:①肝脏分泌的新生HDL;②由肠道直接合成的HDL颗粒和来自于乳糜微粒的HDL;③VLDL脂解过程中脱落的表面物质(下图)。血浆HDL-胆固醇(HDL-C)水平主要由遗传因素决定(40%~60%),其浓度与冠心病的发病风险呈负相关。因此认为,提高HDL可提供冠心病的保护因素,但HDL是一种混合体,包括了许多成分,而且它们的密度、大小、电荷与蛋白成分以及功能各不相同,见图5-33-3。HDL具有冠心病保护作用的机制未明,可能涉及多个方面,其中最主要的原因是HDL可以逆转胆固醇的转运方向,使较多的胆固醇进入肝脏,再经胆道排泄;HDL还可能有抗感染、阻滞LDL氧化、内皮细胞凋亡和抗血栓形成作用;新生的HDL颗粒(nascent HDL particles)代谢迅速,具有更好的保护意义;但也有不同意见。
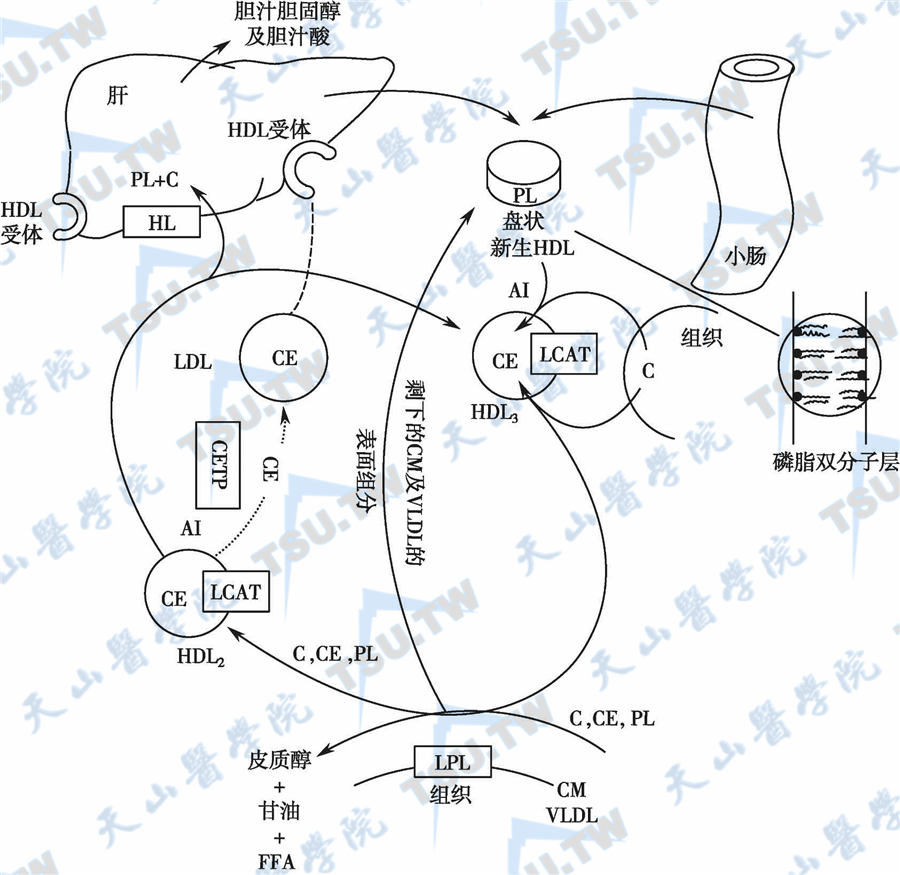
高密度脂蛋白代谢
注:LPL:脂蛋白脂肪酶;HL:肝脂酶;LCAT:卵磷脂胆固醇脂酰转移酶;CETP:胆固醇酯转移蛋白;TG:甘油三酯;C:胆固醇;CE:胆固醇酯;PL:磷脂
脂蛋白(a)是独立的脂蛋白成分
脂蛋白(a)[lipoprotein(a),LP(a)]是一种独立的脂蛋白成分,颗粒大小为25.0nm,平均密度为1.065,由36%胆固醇酯、9%游离胆固醇、3%TG、18%磷脂、34%蛋白质及5%蛋白结合糖构成。它具有类似于LDL的脂质核心,载脂蛋白为Apo(a)和ApoB100,其中Apo(a)是LP(a)的抗原性蛋白,仅存在于LP(a)中。LP(a)主要在肝脏合成。脂蛋白(a)并不是由VLDL转化而来,也不能转化成其他的脂蛋白。目前对调控LP(a)产生和清除的因素尚了解不多。LP(a)能和LDL竞争LDL受体,因此LDL受体缺陷可影响LP(a)的水平。不同种族人群之间LP(a)的差异较大,其在血浆中的水平主要受遗传因素的影响。LP(a)水平升高可竞争性地与纤溶酶原受体结合而影响纤维蛋白原的溶解,因而被认为具有致动脉粥样硬化作用。LP(a)升高是家族型高胆固醇血症患者发生冠心病的危险因素,但只有在同时有LDL水平升高的情况下才如此。
降低LDL-C已经成为血脂谱紊乱治疗的目标,但是从化学结构上看,LDL-C的量并不能反映其携带胆固醇的能力。研究发现,载脂蛋白B-100(apolipoprotein B-100,ApoB)或磁共振LDL颗粒数目(nuclear magnetic resonance LDL particle number,NMR LDL-P)能更好地预期冠心病的危险度,因此有人提议,除LDL-C和非HDL-C外,也应将ApoB(或NMR LDL-P)作为降脂治疗的评价指标。
