遗传性纤维蛋白原异常包括量与质的异常,量的异常根据纤维蛋白原的水平高低分为无纤维蛋白原血症和低纤维蛋白原血症;质的异常是纤维蛋白原结构异常,所致疾病称为异常纤维蛋白原血症。
纤维蛋白原是一个血浆中循环的340kDa的糖蛋白,其浓度是160~400mg/dl,半衰期大约是4天。人纤维蛋白原主要在肝细胞中表达,虽然肝外合成主要是在肠、子宫颈和肺的上皮细胞中。关于巨核细胞中纤维蛋白原生物合成已经争论了几年了,现在普遍认为血小板纤维蛋白原储存在α颗粒中,最近这也被实时定量PCR实验证实,α颗粒最初来源于血浆提取物。
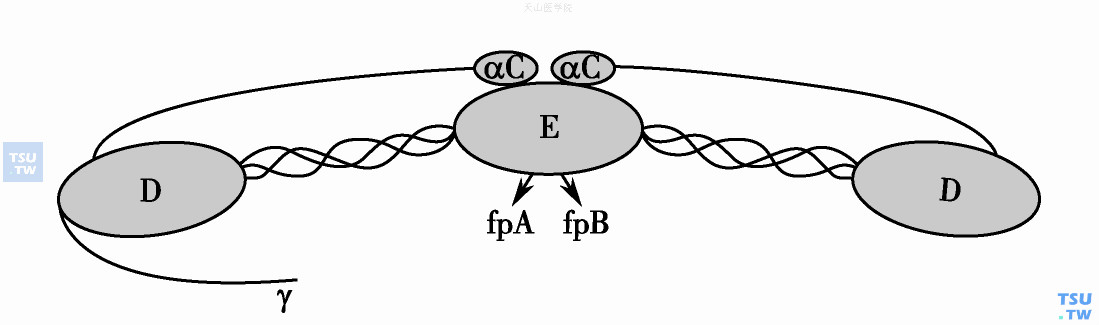
纤维蛋白原分子结构示意图
中间E区包含六个纤维蛋白原肽链的N末端,在纤维蛋白形成过程中α和β肽链的N末端被剪切;D结构域中包括γ和β肽链的C末端,卷曲的区延伸到D结构域的外面;α肽链的C末端区延伸到中间的E结构域
分泌在血中的纤维蛋白原是由二硫键将两个相同的异质三联体连接的六聚体,异质三联体分别包括一个Aα,一个Bβ和一个γ链,分子量分别是67 (610个残基),57(461个残基)和47kDa(411个残基)。三条链通过平行基因编码(平行基因FGA,FGB和FGG分别编码Aα、Bβ和γ链),在4号染色体(4q31. 3)的50kb区簇生。FGA基因包括六个外显子,跨度为7. 5kb,位于FGG(10外显子,8. 5kb)和FGB(8外显子,8kb)之间,FGB基因是从相反方向转录的。在不同的应激刺激(例如炎症和组织损害)下,三个人纤维蛋白原基因的协同转录被上调2~10倍。作为二类急性期反应物,纤维蛋白原可以被IL-6和糖皮质激素信号通路上调。循环中的纤维蛋白原呈现广泛的异质性,主要是由于Aα和 γ mRNAs的选择剪接以及Aα链的C末端降解。尤其是较小的γ'链(占总γ链的8%)来源于用20个氨基酸序列替换了较大的γA的后四个氨基酸,从而保留了内含子9。Aα链是延长αE链236个残基,羧基端是延长其他两个已经确定的同源染色体的C末端。αE链来源于成熟转录后的六个外显子,并优先组装成αE/αE 420kDa纤维蛋白原变异体。因为Bβ和γ链是单个天门冬酰胺残基的糖基化(分别在Bβ和γ链的第362位和52位),而不是唾液酸化作用模式,这主要说明这些链的微观不均匀性。
纤维蛋白原分子的450-Å-长的三节的结构包括两个对称的末端球状D结构域(由Bβ和γ链的C末端构成)和由卷曲螺旋区域连接的中心的E结构域。纤维蛋白原是用步骤-方法的方式组装:首先是产生Aα-γ和Bβ-γ二聚体,随后增加了第三条链,最后Aα- Bβ-γ半分子二聚化成六聚体的纤维蛋白原。六聚体分子由29个链内和链中的双硫键固定。这个过程是在内质网中在分子伴侣的协助下迅速完成的,分子伴侣包括结合蛋白,葡萄糖调节蛋白94,蛋白质二硫化物异构酶和钙联接蛋白。N-连接寡糖成熟后,通过高尔基网将特异的侧链羟基化、硫酸盐化和磷酸化,成熟蛋白分泌到循环中。
通过纤维蛋白肽A(FPA)和B(FPB)的凝血酶从Aα和Bβ链的N-末端分别除去Arg16- Gly17和Arg14- Gly15键后,纤维蛋白原转变成纤维蛋白。FPA比FPB发生得早和快,并足够形成血块。除去FPA后暴露了一个聚合位点(命名为EA),通过与一个组成性补充性结合的袋蛋白对接从而起始聚合作用,这个袋蛋白位于邻近分子的D结构域。一个分子的D结构域与邻近的纤维蛋白单体的中心的E结构域结合,从而产生两个分子的厚链或初原纤维。原纤维通过侧面结合产生多股的纤维,这些纤维组成了物理的凝块的网状组织。最后这些相关的不稳定的结构通过XⅢ因子介导的转谷氨酰胺酶转变成了由共价键相连的稳定的纤维蛋白凝块。
