多形性腺瘤(pleomorphic adenoma)又称混合瘤(mixed tumor),是最常见的唾液腺上皮性肿瘤。国内六所医学院校口腔病理23 010例唾液腺肿瘤中,多形性腺瘤为10 403例,占唾液腺上皮性肿瘤的45%,占全部良性肿瘤的72%。国外关于该瘤的发病率的数据为2. 4到3. 05/每十万人口。国内Tian等(2010)统计5002例大唾液腺上皮性肿瘤,多形性腺瘤为2609例(52. 2%);小唾液腺肿瘤1980例中,多形性腺瘤有670例(33. 8%)。Eneroth(1971)统计2328例大唾液腺上皮性肿瘤,多形性腺瘤占75. 6%。Chaudhry等(1961)统计小唾液腺上皮性肿瘤1320例,其中多形性腺瘤有占55. 7%。北大口腔病理(1993)统计了628例小唾液腺上皮性肿瘤,多形性腺瘤有239例,占上皮性肿瘤的38%,占良性肿瘤的79. 4%。
组织发生
多形性腺瘤之所以在以前称为混合瘤是基于肿瘤由上皮和黏液软骨样组织两种不同胚层组织混合构成的特点。其中黏液样组织和软骨样结构的组织来源也是以往争论的焦点。通过大量的研究证实,黏液软骨样组织均来自于肿瘤性肌上皮细胞。所以该肿瘤为纯的上皮性来源为目前所公认,而且多数人同意其来源于闰管。那么肿瘤是起源于闰管的腺上皮细胞还是肌上皮细胞或者其他的细胞?或者肿瘤是起源于单个多潜能的细胞还是有一个以上的“干细胞”参与了肿瘤的起源?此问题目前大家都感兴趣,也是仍在争论的问题。目前越来越多的证据显示肿瘤的腺上皮细胞和肌上皮细胞有相同的表型和基因型,支持多形性腺瘤起源的“变异肌上皮细胞模式”,如最近的研究显示,对有PLAG1重排的多形性腺瘤肿瘤中的上皮和肌上皮细胞分别进行8q12易位和PLAG1重排的遗传学表型分析,结果是这两种细胞类型均携带PLAG1的重排。免疫组化研究显示PLAG1主要表达在双层管外层变异肌上皮细胞,腔面细胞偶尔阳性。这些结果支持唾液腺肿瘤发生的多潜能单细胞理论,也支持PLAG1在良、恶性多形性腺瘤发生上的作用。
临床表现
多形性腺瘤80%~90%发生于腮腺,其次为下颌下腺,舌下腺罕见。在Eneroth报告的1760例中,腮腺1658例,下颌下腺102例。小唾液腺以腭腺最多见。Chaudhry等报告733例,腭部有476例,上唇为105例,磨牙后腺占第三位。肿瘤可发生于任何年龄,以30~60岁最多见,女性稍多于男性。多形性腺瘤也可发生在口腔邻近部位如鼻腔、鼻窦、咽部和皮肤(称软骨样汗腺瘤,chondroid syringoma),也可发生在发育过程中易位的唾液腺组织如副腺体、颈淋巴结、下颌骨中的易位腺体组织。
肿瘤生长缓慢,无任何自觉症状。原发瘤多位于腮腺浅叶,表现为以耳垂为中心或少数位于耳屏前方的肿物,多呈结节状生长。小肿物可呈圆形,触之软硬不等,从囊性感至软骨样硬度,可活动,与周围组织无粘连。较大肿物则常为不规则结节状。约10%的肿瘤发生于腮腺深部,位于下颌升支后内侧,活动度小,或向咽侧壁突出,易被认为咽旁肿物。小唾液腺发生的多形性腺瘤常为黏膜下无痛性肿物。发生于腭部者,多位于硬软腭交界处,或软腭,覆盖黏膜颜色正常,肿物较大时黏膜表面可形成创伤性溃疡。
多形性腺瘤可突然生长加快,但并不表示一定有癌变,当生长加快伴有疼痛时应考虑有恶性改变。北大口腔病理统计131例多形性腺瘤,其中19例有突然生长加快病史,但其组织像并未见恶性征象。
大体病理
肉眼观察多形性腺瘤多数为圆形或椭圆形,肿瘤大小不一,个别肿瘤可巨大。较小的肿瘤多位于腺体组织内,界限清楚,可见完整包膜,但也有部分肿瘤虽然界限清楚,但并无完整包膜或无包膜或者形态极不规则,呈结节样。较大的肿瘤多呈不规则结节状,结节的大小不等,有的有蒂,有的结节基底宽广。肿瘤剖面多呈灰白色,或灰黄色,多呈实性,部分可有白色致密索条。较多的肿瘤可见切面黏滑、呈半透明的区域,有的肿瘤可见浅蓝色透明的软骨样组织或黄色的小圆形角化物。部分肿瘤内可形成大小不等的囊腔,内含透明黏液。较大的肿瘤内偶见钙化,有骨样硬度。肿瘤周围有厚薄不一的包膜,分离时易与瘤体剥离(图7-1)。
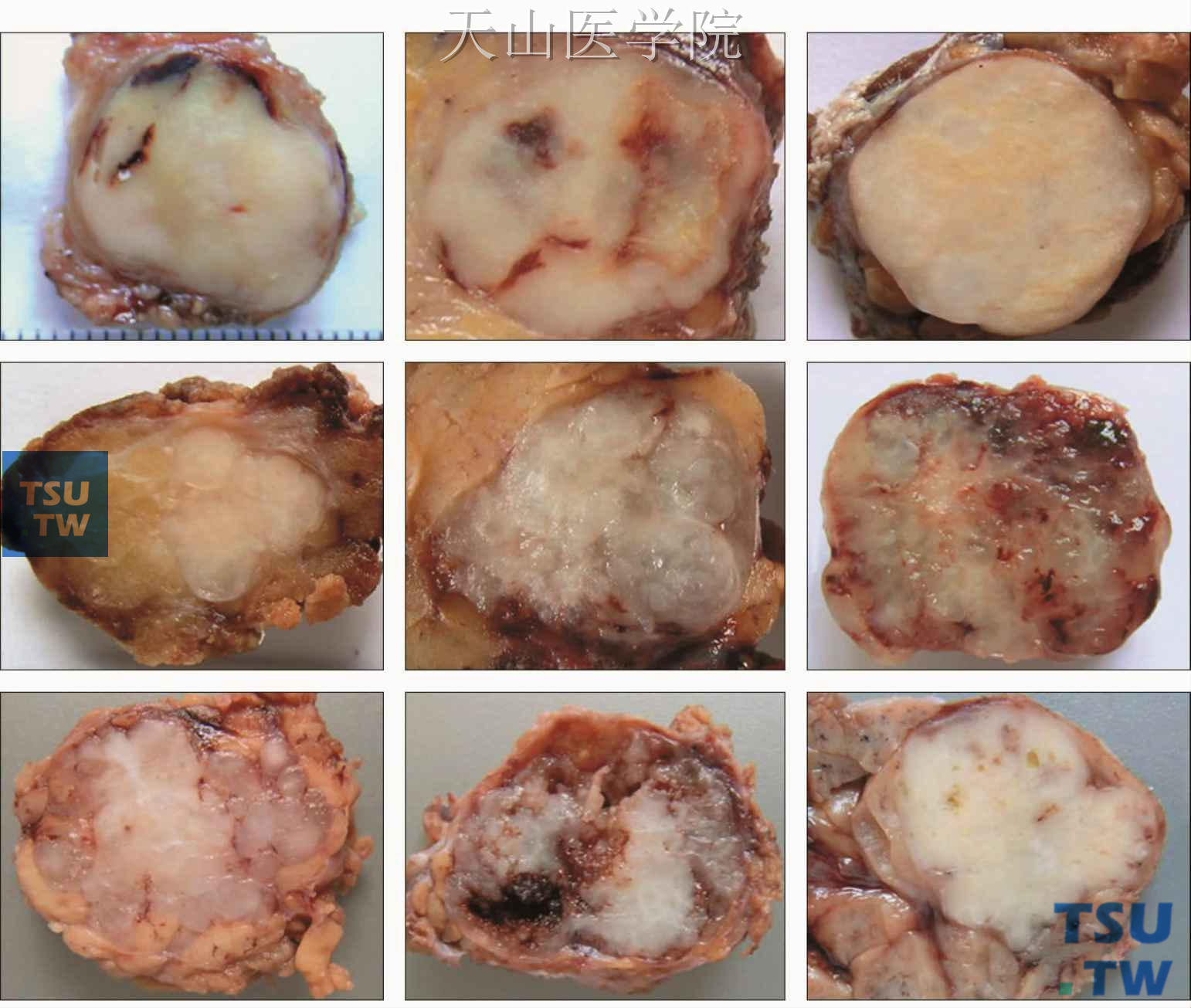
图7-1 多形性腺瘤的剖面(罗海燕分切、摄影)
组织病理
多形性腺瘤由上皮成分、黏液样组织和软骨样组织构成,因此也称为混合瘤。肿瘤中各种组织成分的比例有很大不同,细胞形态变化多样,导致肿瘤的组织结构复杂,具有结构上多形性的特点。各个肿瘤之间、同一肿瘤的不同部位之间的组织结构均不一致(图7-2)。
肿瘤性腺上皮和肌上皮细胞:肿瘤的上皮成分由导管上皮(或称腺上皮)细胞和变异肌上皮细胞构成。这些上皮细胞构成多形性腺瘤中的腺管样结构。典型的腺上皮细胞呈立方形或矮柱状,核圆形或卵圆形,呈空泡状,有或无核仁,胞质微嗜酸性,形成导管样结构的内衬上皮或称腔面上皮。腺管的外围为多角形或星形的肌上皮细胞,胞质少,多呈透明状,核染色深。这些细胞围绕腺上皮细胞形成的管腔,为一层或多层,其外层细胞与片状排列的肌上皮细胞或者黏液软骨样组织中的细胞相互延续、过渡,没有截然的界限。这种腺管结构说明肿瘤细胞试图形成类似于正常腺体的导管样(内层为导管上皮、外层为肌上皮)结构,即所谓的双层管结构。这种腺管样结构无一般腺体的腺管所具有的基底膜。管腔内有粉染的均质性物质,PAS染色呈阳性,奥辛蓝染色呈弱阳性,甲苯胺蓝不呈γ异染性。腺管样结构的腺腔大小不一,有的管腔扩张成囊腔样,腔面细胞受压变为扁平细胞;腺腔小时可能不易辨认。腺上皮有时也可表现为实性团块或索条状(图7-3)。
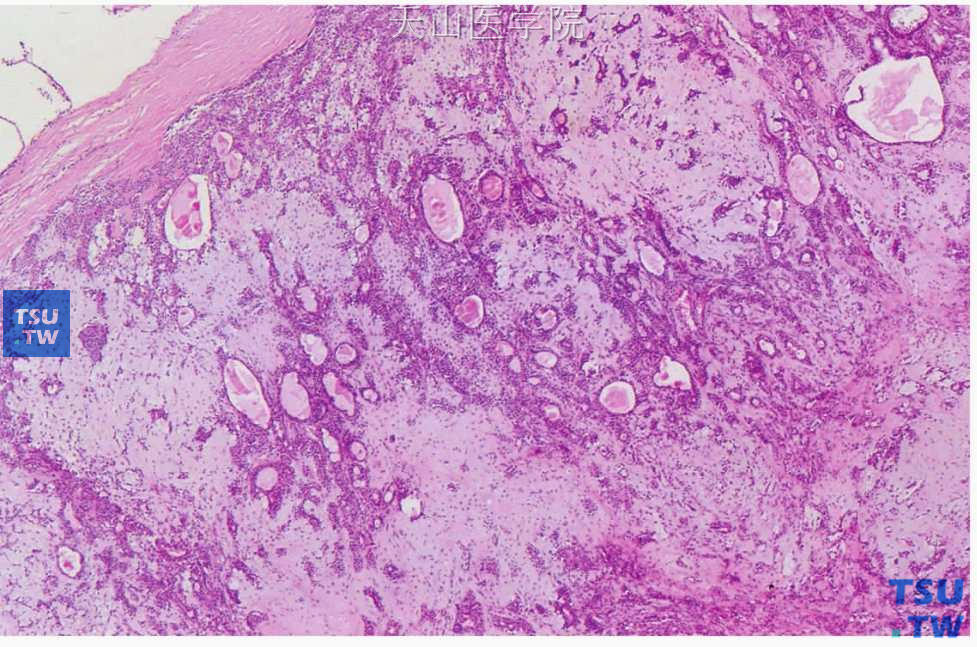
图7-2 多形性腺瘤
低倍镜下见肿物有包膜,肿瘤由含导管结构的上皮、黏液样组织和软骨样组织构成
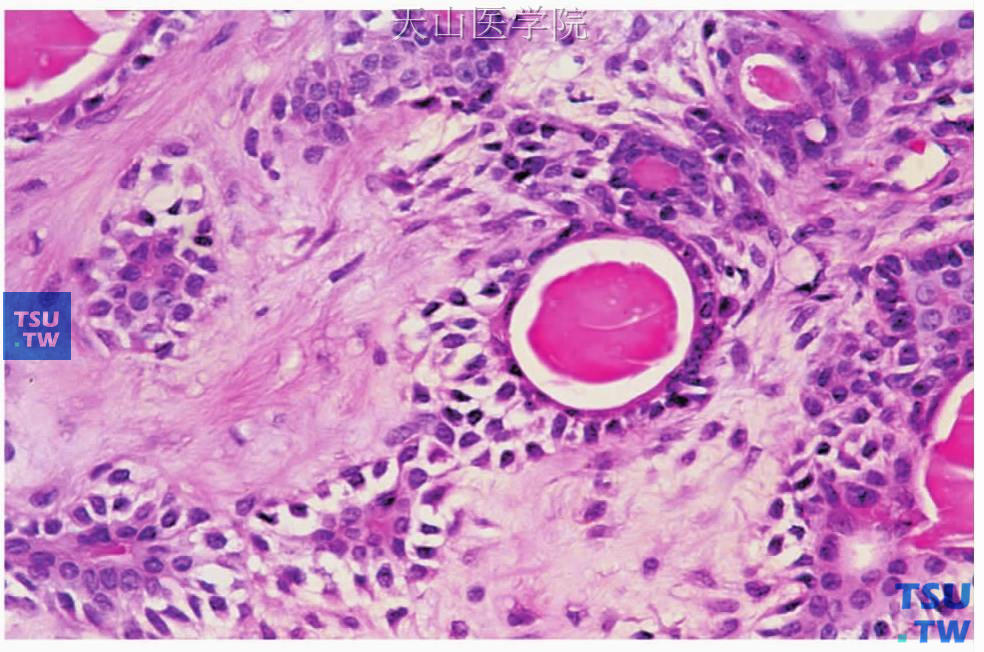
图7-3 多形性腺瘤
肿瘤的腺上皮成分排列成单层导管结构,内含嗜酸性分泌物;导管外层为透明的肌上皮细胞,数量不等
肿瘤的上皮细胞在非腺管样结构区由腺上皮细胞和变异的肌上皮细胞混合构成,主要是后者。这些上皮细胞排列成不规则片状、巢状或条索状,其间穿插分布多少不等的、由变异肌上皮细胞形成的黏液样组织和(或)软骨样组织(图7-4)。片状排列的细胞界限不清楚,有时较拥挤。细胞核圆形,呈泡状,染色质较细,分布不规则,有时见小核仁,有时核深染。在一些肿瘤中肌上皮细胞构成多形性腺瘤的主要成分。这些变异的肌上皮细胞形态可为浆细胞样、梭形、透明或腺上皮样表现(图7-5~图7-7)。浆细胞样成分较多见,呈片状或弥漫散在,细胞呈圆形或卵圆形,核偏位或中位,胞质嗜酸性呈均质状。梭形细胞类似于平滑肌细胞,常排列成束。有时梭形肌上皮细胞的生长、排列方式很似神经鞘瘤中Antoni A区的表现,应该注意鉴别。胞质透明的肌上皮细胞偶见。腺上皮样肌上皮细胞的形态与腺上皮在光镜下不易鉴别,但免疫组化染色前者有肌上皮细胞的特征。肿瘤的细胞成分的多少有较大的变异,有的肿瘤以黏液软骨样基质为主,细胞成分稀少散在;有的肿瘤细胞排列密集而黏液软骨样成分少,上皮成分大致占肿瘤的80%以上时可称富于细胞性多形性腺瘤。一般来说,细胞的丰富程度并不影响肿瘤的预后。肿瘤还可以发生较明显的囊性变,肿瘤性上皮细胞衬复囊壁。总体来看,大部分多形性腺瘤的细胞大小较一致,核分裂少见。然而有些肿瘤区域会出现细胞增生活跃的现象(后述)。
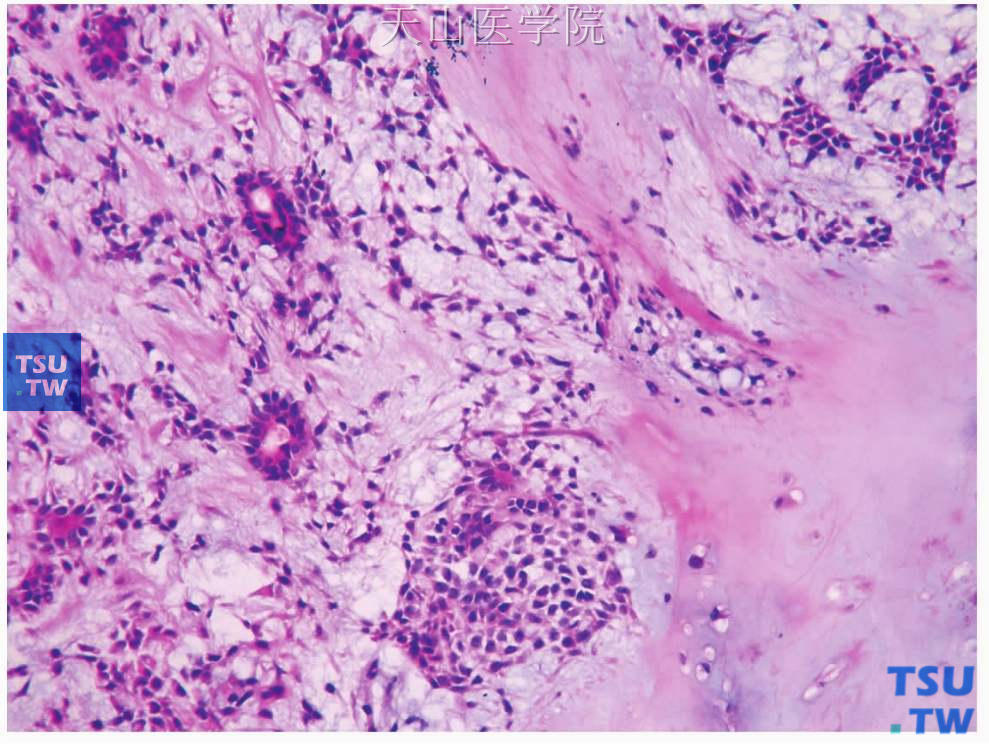
图7-4 多形性腺瘤
肿瘤中的黏液样、软骨样组织穿插在上皮成分间
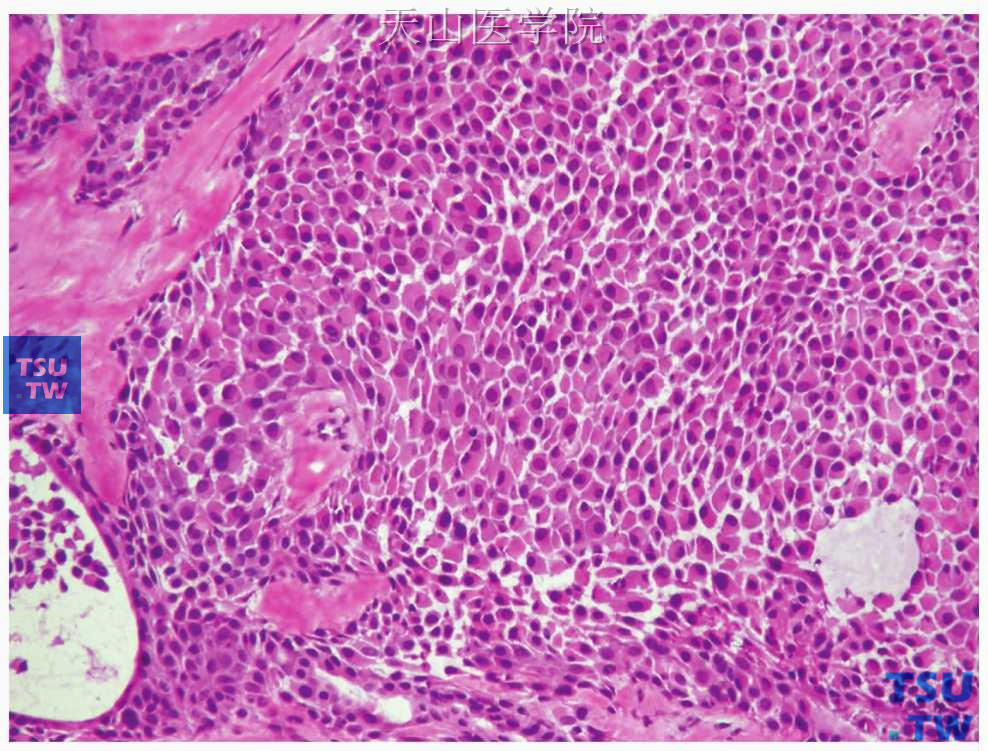
图7-5 多形性腺瘤
浆样肌上皮细胞,胞质丰富,胞核位于细胞一侧
黏液软骨样组织:所谓的混合瘤中的间叶样组织即黏液样组织和软骨样组织,在腺管及上皮条索间常见上皮细胞疏松排列,逐渐移行为黏液样组织和软骨样组织。黏液样组织中的细胞为肿瘤性肌上皮细胞,呈星形或梭形,借长突起与其他细胞相接触(图7-8),有时排列成细条索,相互连接成网状或者散在于黏液样组织中。在少数多形性腺瘤中黏液样组织可成为肿瘤的主要成分。有人认为黏液样成分为主时,肿瘤的包膜薄易破裂容易导致肿瘤的种植性复发。黏液样组织PAS呈弱阳性,奥辛蓝染色呈阳性,甲苯胺蓝呈γ异染性,经透明质酸酶消化异染性消失,显示为结缔组织性黏液。软骨样组织似透明软骨,软骨细胞大小不一,胞质呈空泡状,有的细胞位于软骨样陷窝之中,周围基质嗜碱性。Mallory染色呈蓝色,表现与结缔组织的染色反应一致。少见情况下,软骨样组织可以直接发生软骨内骨化而成骨或者由间质组织发生化生而形成骨,甚至可以伴发有骨髓形成(图7-9~7-10)。
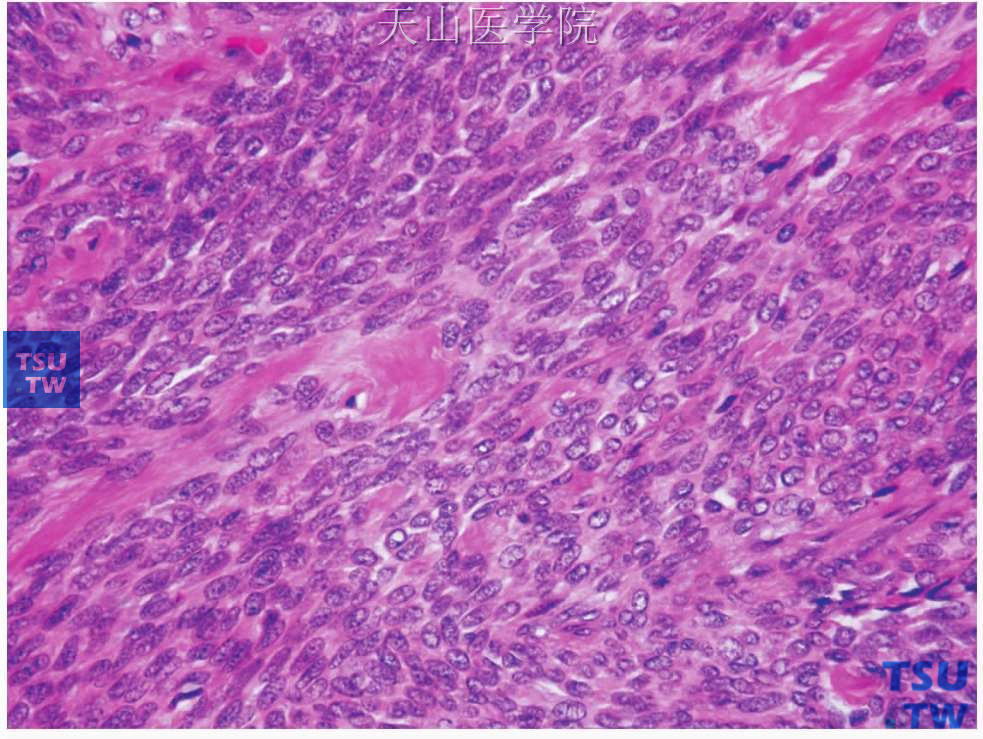
图7-6 多形性腺瘤
梭形肌上皮细胞
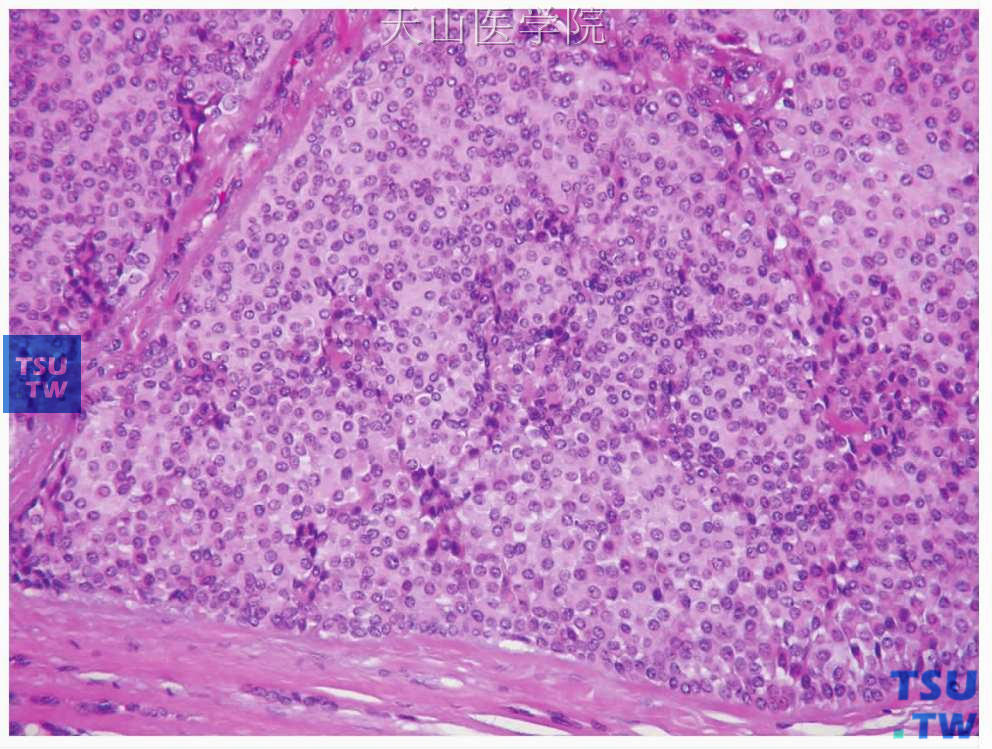
图7-7 多形性腺瘤
腺上皮样肌上皮细胞,细胞呈圆形或立方状
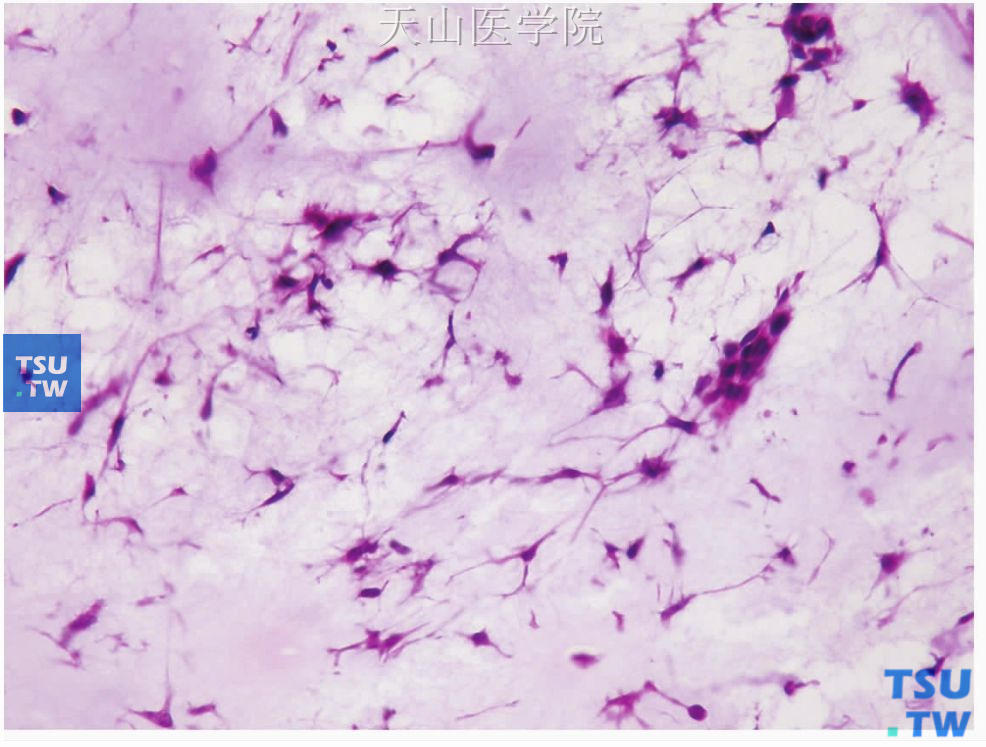
图7-8 多形性腺瘤
冰冻切片中见肌上皮细胞有长的突起
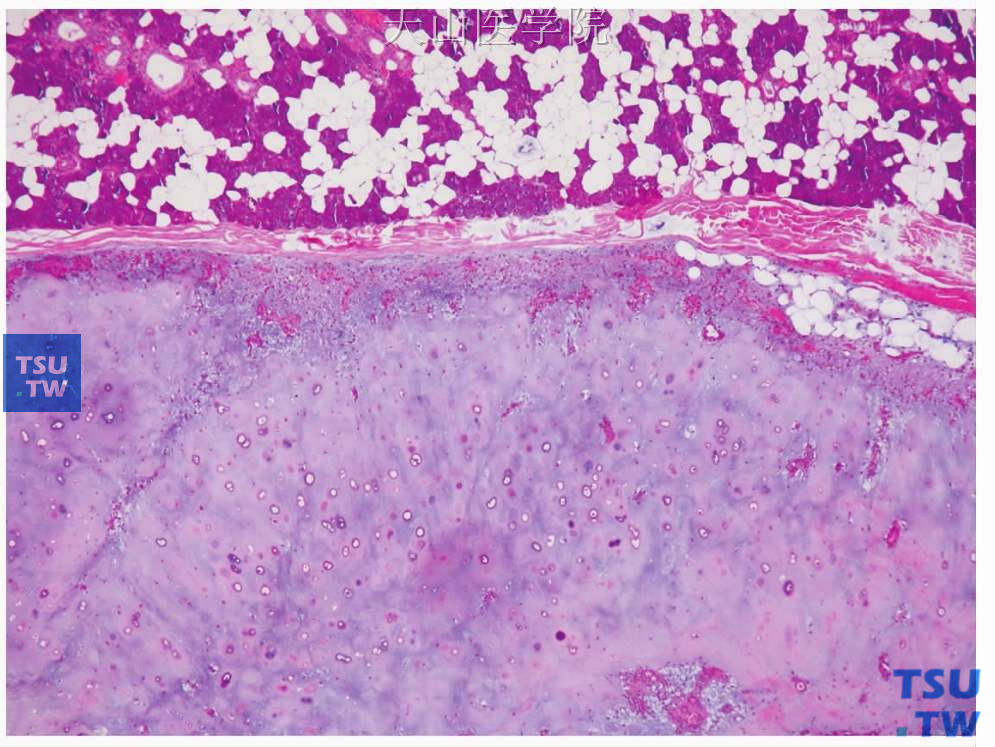
图7-9 多形性腺瘤
软骨样组织,呈较典型的透明软骨样结构
肿瘤包膜的厚度及是否完整有很大差别。有研究显示如果进行连续切片,几乎没有肿瘤有完整的包膜(图7-2)。大唾液腺的多形性腺瘤无包膜区多见于以黏液样组织为主区,此处的肿瘤组织与正常组织直接接触或者可见肿瘤组织与正常组织相互交错,也可见部分正常组织被包裹在肿瘤中(图7-11)。包膜为较致密的纤维组织,相当多的肿瘤包膜内可有肿瘤细胞侵入(图7-12),但这并不是恶性的生物学行为的指征,而与肿瘤的多结节性生长有关。这些侵入或穿过包膜的细胞形成新的肿瘤结节,有时在切面上显示与原来的肿瘤已分开即所谓的假卫星结节,实际上仍附着在肿瘤主体上或借狭小的蒂与原来的肿瘤相连。真正的多中心发生的多形性腺瘤罕见。有研究显示原发性多结节多形性腺瘤具有克隆相关性,不支持独立发生的观点,而且卫星瘤p53、Ki67与主瘤无不同,不能确定多灶肿瘤更具侵袭性。小唾液腺多形性腺瘤如发生在腭部者常常无包膜,肿瘤组织直接与宿主组织接触或局部长入邻近组织。在肿瘤包膜附近还经常见到区域性淋巴细胞聚集,一般不形成淋巴滤泡。聚集的淋巴组织可以在肿瘤包膜内,也可以在包膜外。可见邻近的肿瘤导管结构周围有胶原纤维围绕,类似于唾液腺慢性炎症中所见。部分多形性腺瘤包膜外的腺体组织可见慢性炎症改变,此种改变中有时炎症轻微,腺泡萎缩,闰管增生(图7-13)。
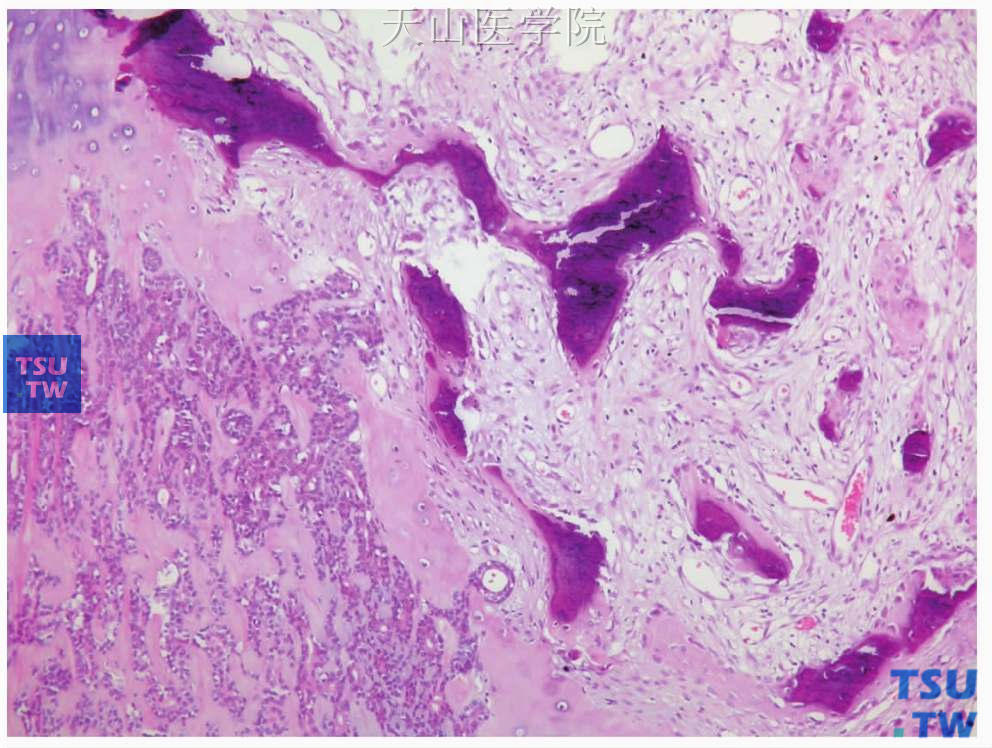
图7-10 多形性腺瘤
肿瘤中的骨组织,可能来自于软骨的骨化
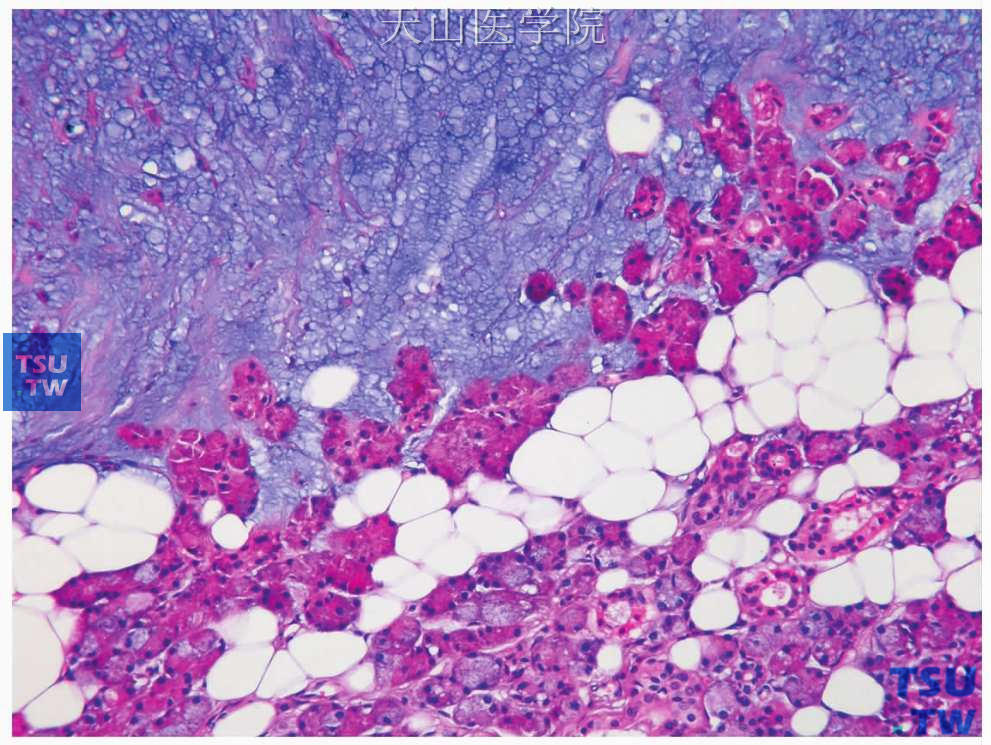
图7-11 多形性腺瘤
肿瘤无包膜,肿瘤成分与正常腺体混合存在
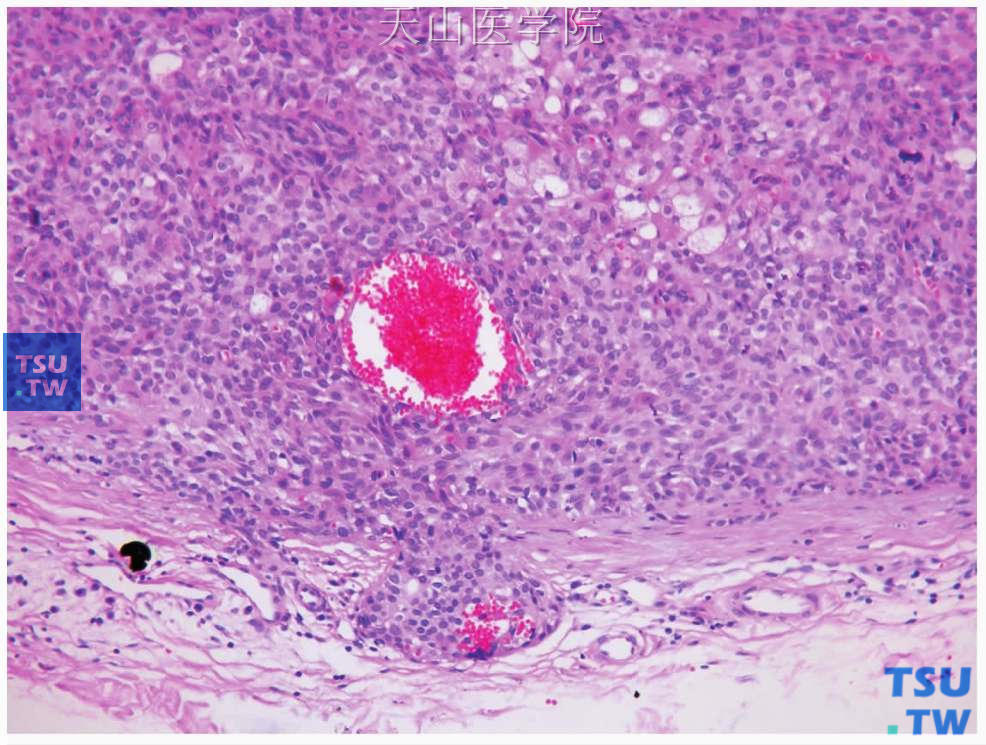
图7-12 多形性腺瘤
肿瘤的包膜浸润,形成包膜内结节
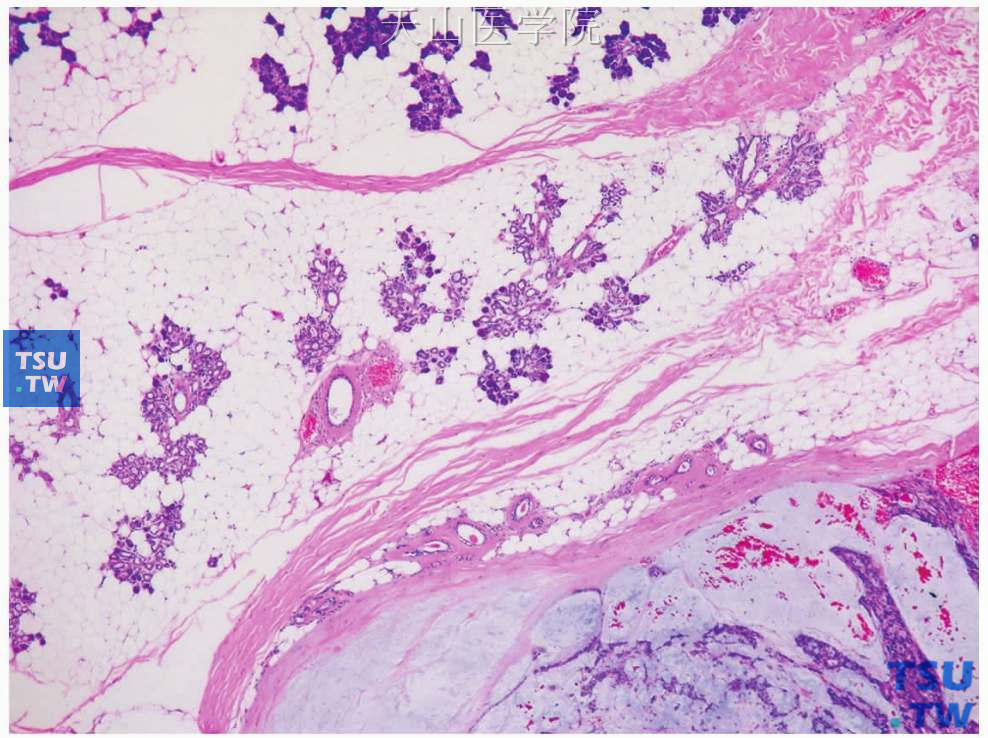
图7-13 多形性腺瘤
肿瘤邻近的腺体见导管增生、腺泡萎缩
化生和变异:肿瘤性肌上皮细胞有时形成一些细胞外均质玻璃样物质,呈圆形堆积在细胞外,连同受其挤压的细胞一起形成类似于筛孔样的结构,应注意与腺样囊性癌鉴别(图7-14)。肿瘤的腔面上皮细胞和肌上皮细胞区可发生鳞状化生,细胞呈巢状,出现明显的细胞间桥,上皮团中央多形成角化珠,角化脱落可形成囊腔,也有的角化区发生钙化(图7-15)。肿瘤细胞另一个较常见的变化是发生嗜酸性变,即胞质丰富,含嗜酸性细颗粒。该变化可见于导管样结构的腔面细胞(图7-16),也可见于肿瘤性肌上皮细胞。有时发生嗜酸性变的细胞具有一定的异型性。偶见肿瘤性肌上皮细胞发生所谓的类似于神经鞘瘤中的返古样变的多核细胞和其他形态怪异的细胞(图7-17),其Ki67的表达与无怪异细胞的多形性腺瘤无明显差别,提示这种改变不具有预后意义。
有时腺管样结构的腺腔中会出现一些泡沫样细胞,可充满于腺腔,有时还伴有腔面细胞发生鳞状化生,少见情况下腺管样结构区会同时发生鳞状化生、假复层柱状上皮及黏液细胞化生,应该与黏液表皮样癌中的黏液细胞鉴别(图7-16、7-18)。其他可见到的细胞还有汗腺样化生,腺管样结构的腔面细胞呈顶浆分泌样,这些细胞有时会形成小乳头样突入腔内(图7-16)。肿瘤中还可出现浆液性腺泡样分化,存在于肿瘤的某些区域。还可见呈片状分布的皮脂样细胞(图7-19)、散在的多核巨细胞(图7-20)。还有报道在上皮细胞中见含色素的黑色素细胞分布,黑色素也沉积在肿瘤性导管细胞中,管腔中见致密的含黑色素的分泌物。
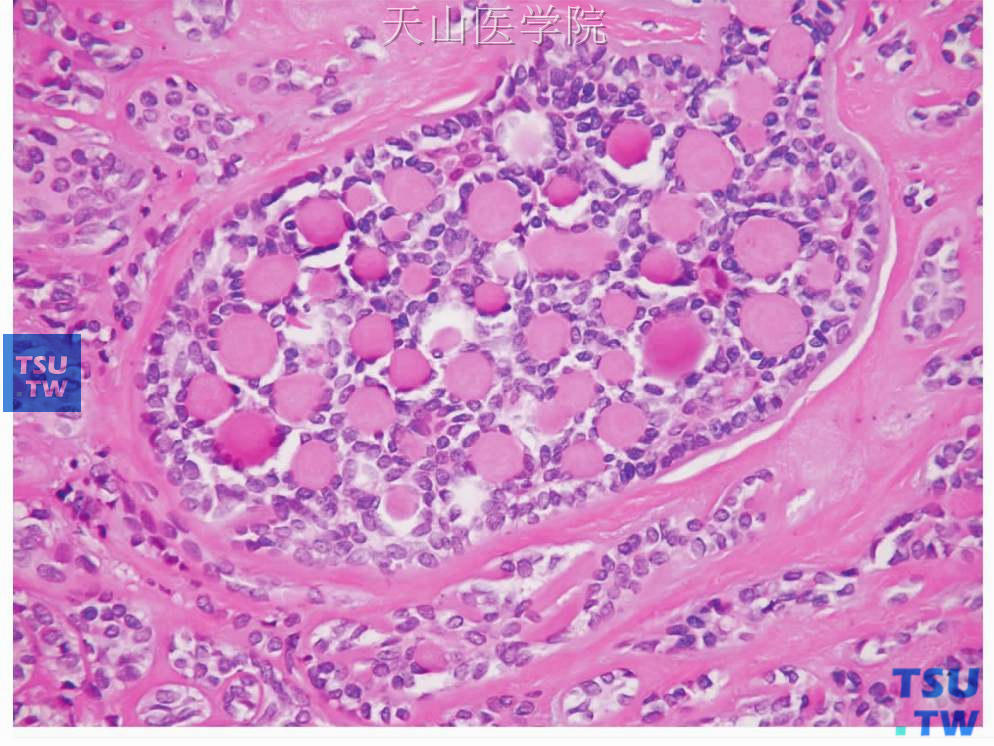
图7-14 多形性腺瘤
肿瘤性肌上皮细胞形成较多细胞外物质,类似于腺样囊性癌
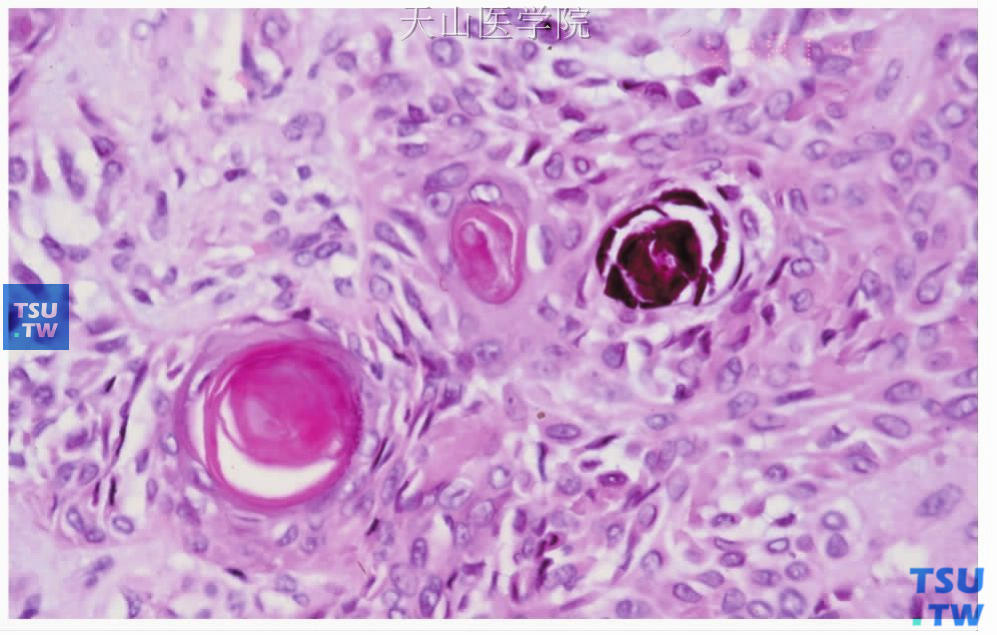
图7-15 多形性腺瘤
肿瘤内的鳞状化生及钙化
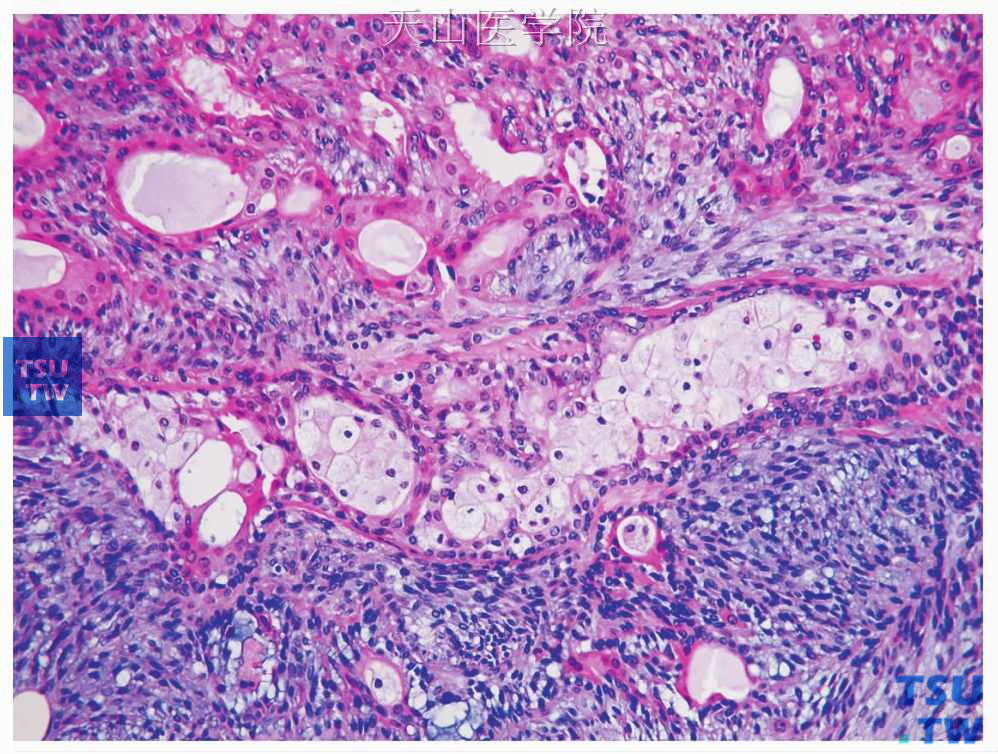
图7-16 多形性腺瘤
嗜酸细胞化生,见于图的上部分,可见顶浆分泌样表现;图的中部可见导管内含泡沫细胞,图的小部分为普通的多形性腺瘤表现的部分
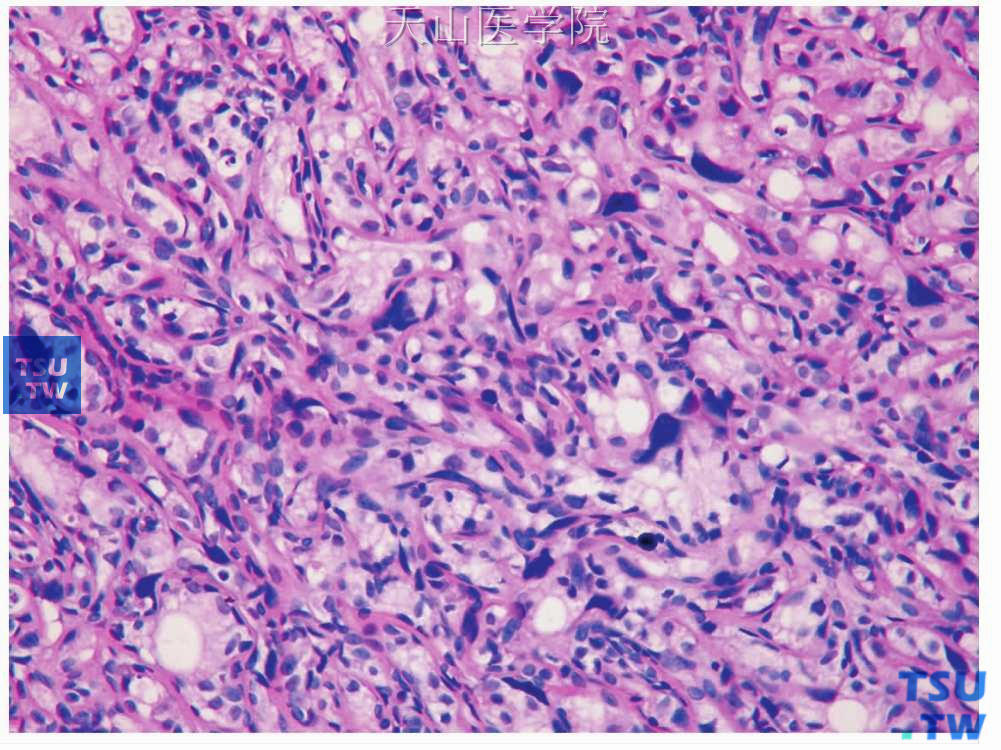
图7-17 多形性腺瘤
所谓的返古样变的形态怪异的细胞
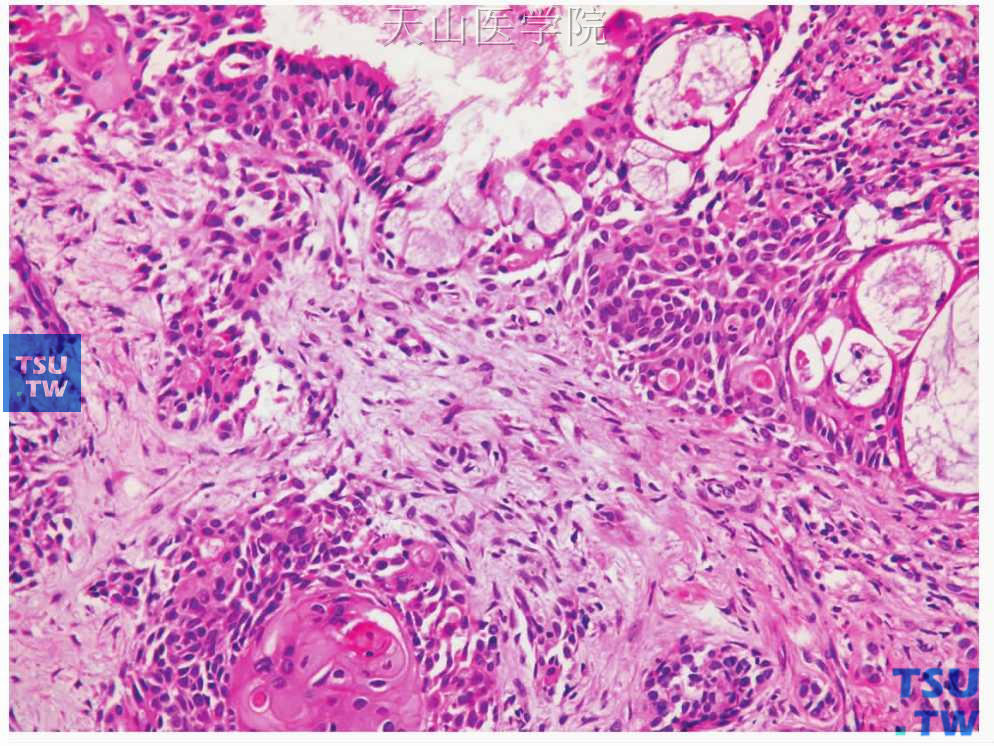
图7-18 多形性腺瘤
肿瘤中出现局部黏液样细胞分化
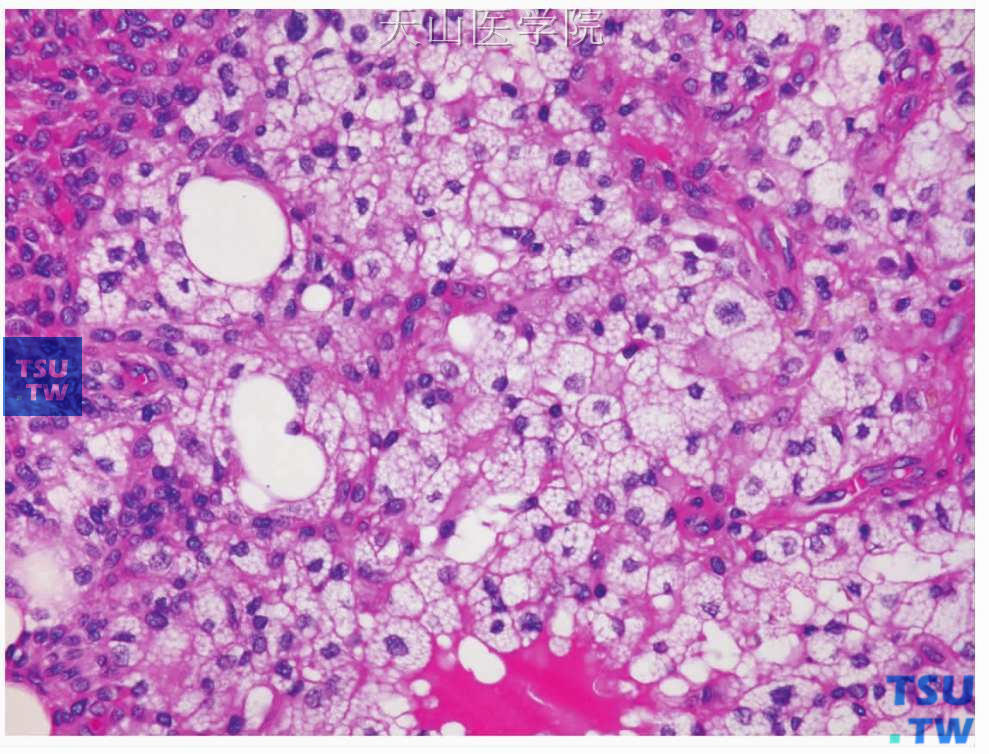
图7-19 多形性腺瘤
肿瘤中的皮脂样细胞
肿瘤上皮团或黏液样组织中有时可见晶状体结构,较常见的是所谓的胶原球,由胶原纤维呈圆形放射状排列而形成,含Ⅰ型和Ⅲ型胶原,其周围细胞表达层粘连蛋白和Ⅳ型胶原并且具有肌上皮细胞免疫特点。这种晶状体嗜酸性染色,有时似礼花状(图7-21)。还有一种晶状体称为富于酪氨酸晶状体,不均质嗜酸性染色,外形似花样(图7-22)。此外还可有草酸盐样晶体(图7-23)和淀粉样物质在肿瘤中沉积。
最近有学者描述了腭部和唇的多形性腺瘤中出现较明显的皮肤附属器结构的分化,而且所占的比例并不低,可达20%以上。常见的包括毛囊的外毛鞘、漏斗、伴有滤泡生发上皮、皮脂腺等。
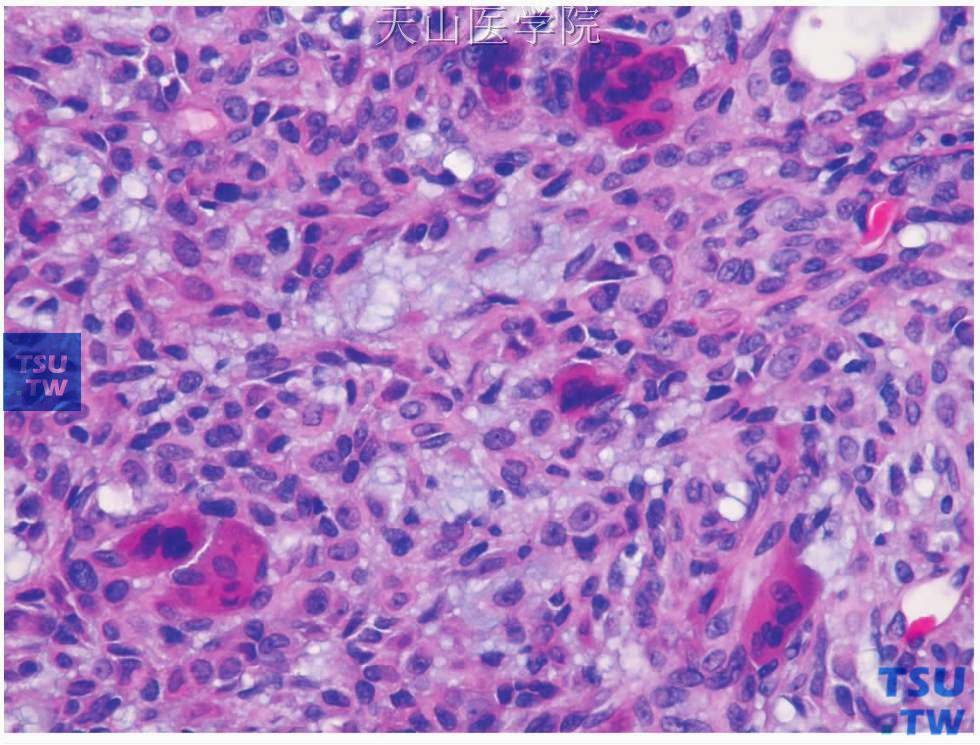
图7-20 多形性腺瘤
肿瘤中的多核巨细胞
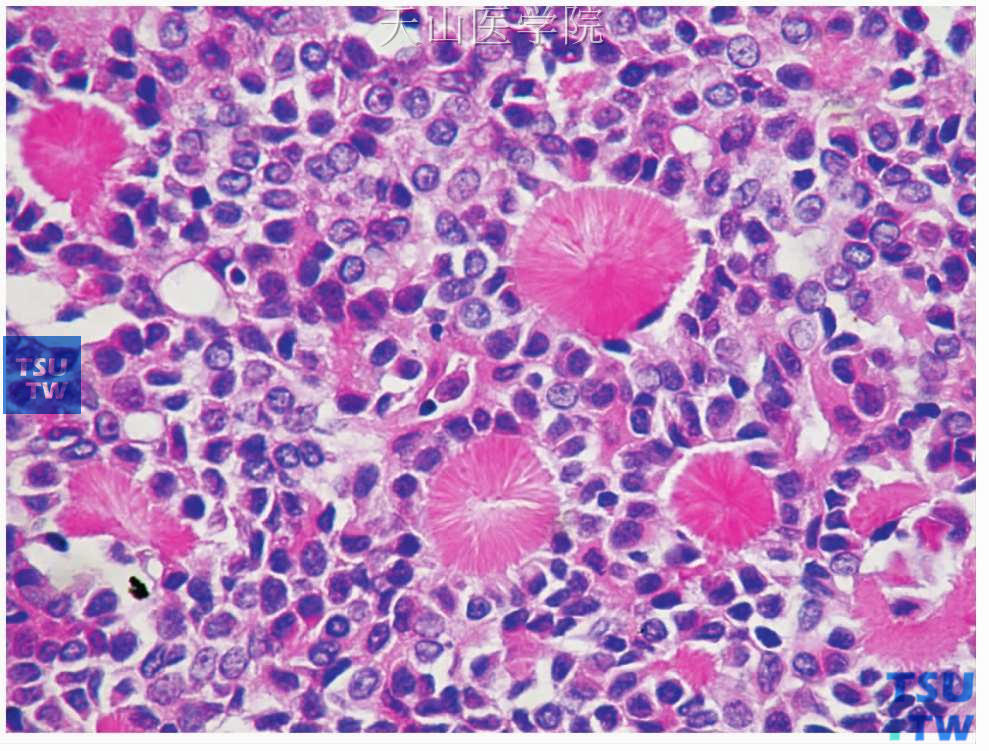
图7-21 多形性腺瘤
肿瘤中的晶状体(胶原球)
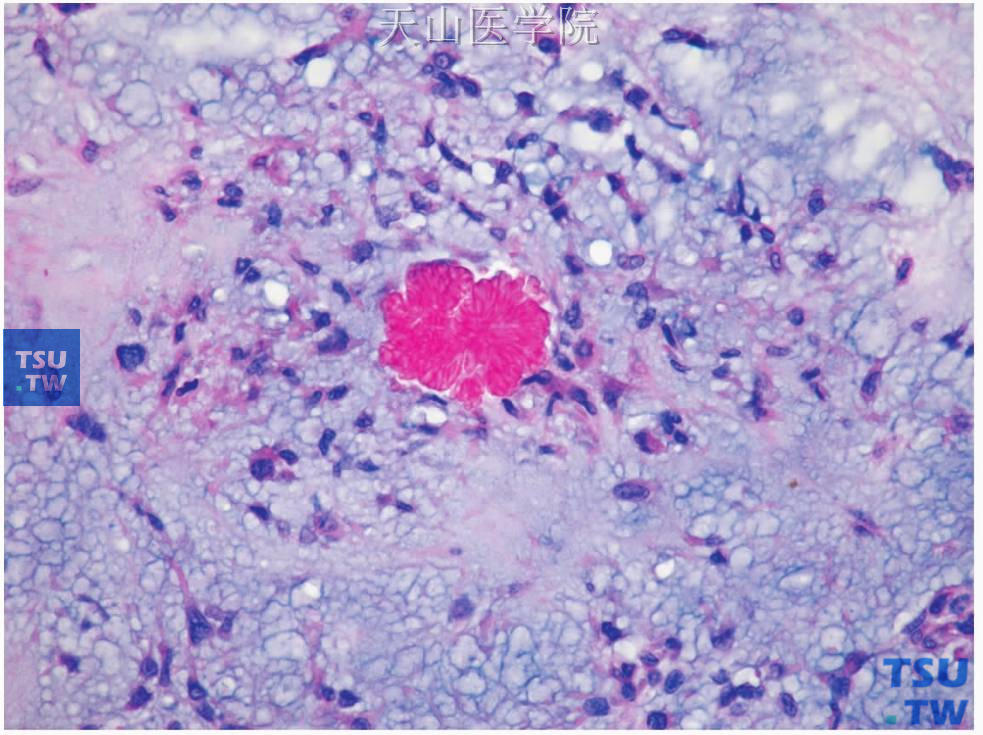
图7-22 多形性腺瘤
肿瘤中的晶状体(富于酪氨酸晶体)
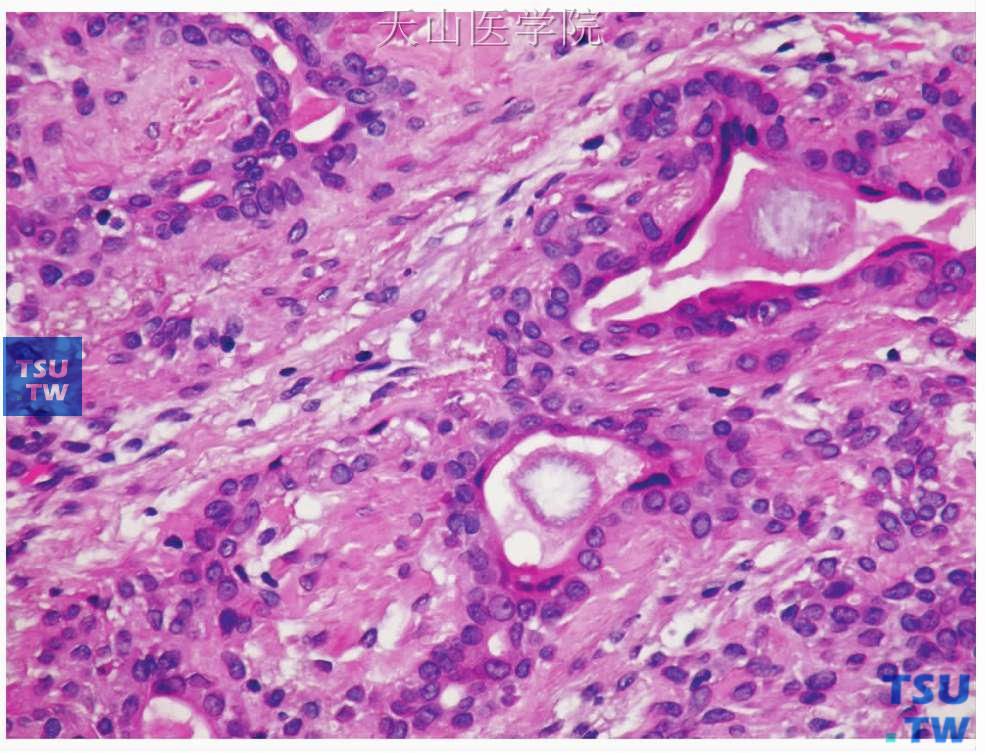
图7-23 多形性腺瘤
肿瘤中的晶状体(草酸盐晶体)
肿瘤中间充质较少,纤维组织常发生玻璃样变性。有时肿瘤中发生广泛的玻璃样变性,类似于瘢痕组织(图7-24),同时伴有肿瘤细胞成分减少。玻璃样变区域的残留肿瘤细胞常常增生活跃,并且可能与恶变有关。少数肿瘤还可见脂肪组织并且脂肪组织可以较多,当脂肪成分超过肿瘤成分90%时称为脂肪瘤性多形性腺瘤(图7-25)。多形性腺瘤侵及血管的情况少见,个别时在切片中的血管内可见肿瘤组织,这主要是肿瘤生长至血管间隙并且使血管外形发生改变造成的假象,并非真正侵入血管,所以不是恶性指征(图7-26)。在某些情况下肿瘤中可见坏死,如在进行针吸活检的部位,或者发生自发性梗死。梗死的范围可以很大,甚至导致整个肿瘤大部分坏死(图7-27),只有肿瘤的外周部分残留并且常常发生明显的鳞状化生。这样的肿瘤仍具有良性过程。还有肿瘤的坏死可能与肿瘤细胞生长快速、有恶变倾向有关。
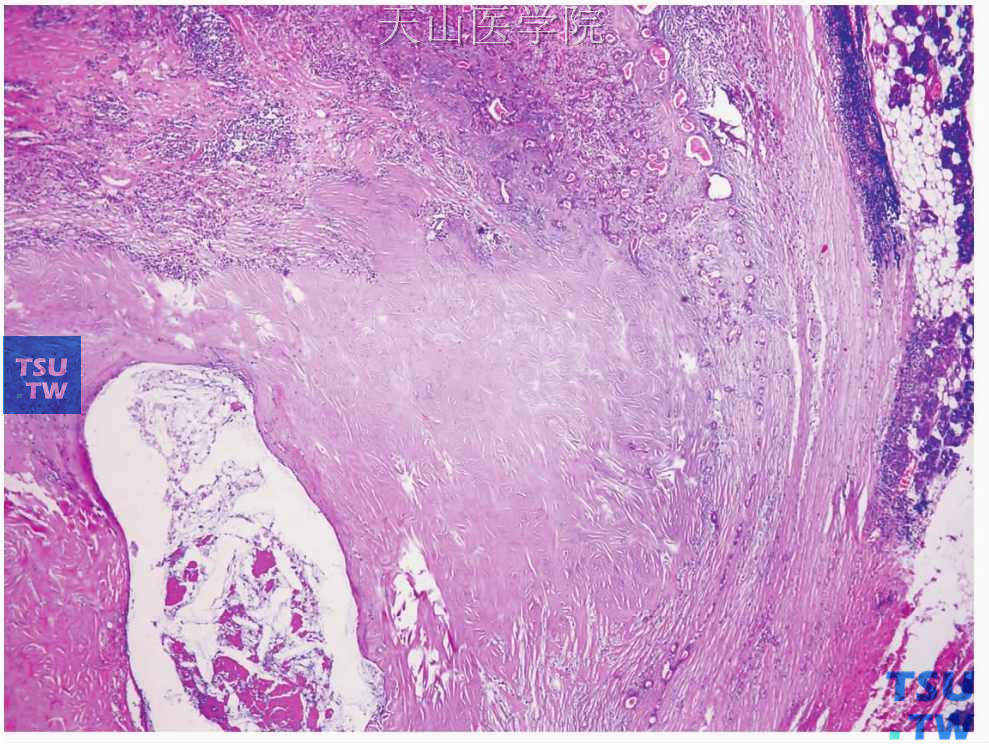
图7-24 多形性腺瘤
瘢痕样玻璃样变(患者的病史达20余年)
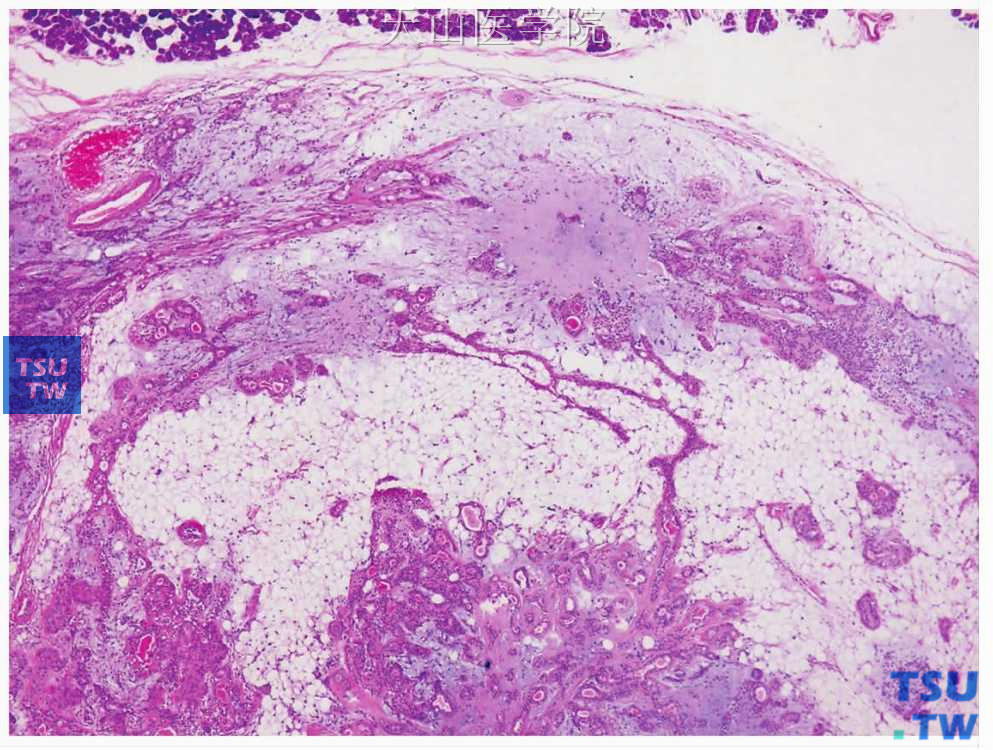
图7-25 多形性腺瘤
含脂肪成分的多形性腺瘤
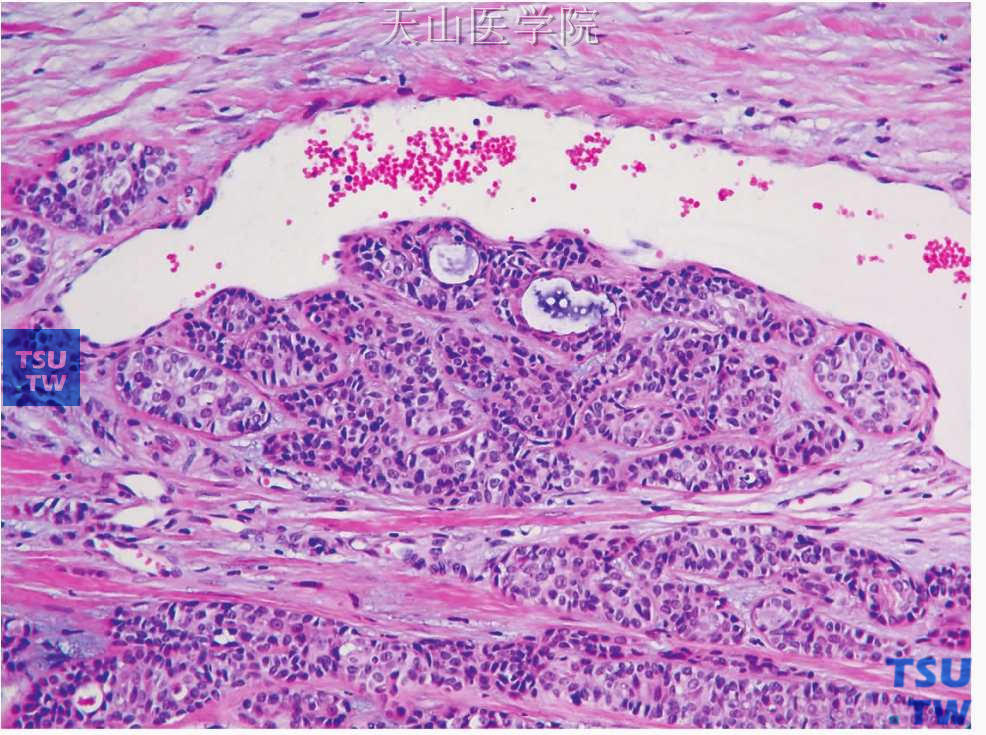
图7-26 多形性腺瘤
肿瘤的生长挤压血管
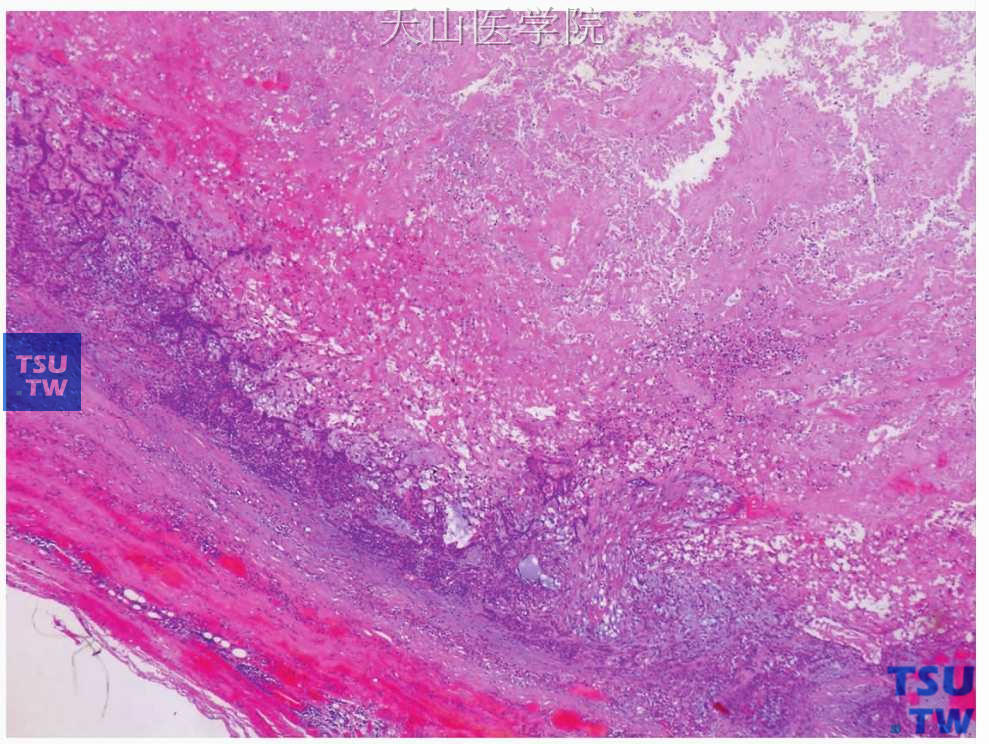
图7-27 多形性腺瘤
肿瘤的大部分发生坏死
多形性腺瘤中的一部分可能发生癌变。WHO1991年的唾液腺肿瘤分类中指出,在3%~4%的癌在多形性腺瘤中可同时观察到良、恶性成分。所以在未发生恶变的肿瘤中能否预测具有发生恶变倾向的肿瘤是大家感兴趣的问题。然而到目前为止还没有公认的预测恶变倾向的组织学指标。建议的指标有细胞的非典型性(图7-28)、核分裂数增加、包膜侵犯、细胞密集、玻璃样变或瘢痕化(图7-24)、坏死(图7-29)和局灶性钙化。但其中的非典型性、核分裂、包膜侵犯及细胞密集在典型的良性多形性腺瘤中也较常见。有的研究显示,上述变化中的玻璃样变性和中等程度以上的核分裂与恶变有关。有人则提出根据临床特点和组织学表现综合判断其恶变潜能。与恶变倾向有关的临床表现是病程长(大于60个月)、年龄大于45岁、肿瘤直径大于4. 5cm;组织学表现有:细胞密集而间质少、中至重度的细胞非典型性、中至重度的玻璃样变、有局灶钙化和坏死。具备上述变化中的1项临床、一项组织学改变或者单纯2项组织学改变者即为高危病例。即使这样,对于恶变倾向的判断及高危病例与原位早期恶变的判别如单纯依赖组织学标准还是非常困难。结合免疫组织化学和遗传学检测方法可能在这方面有所突破。
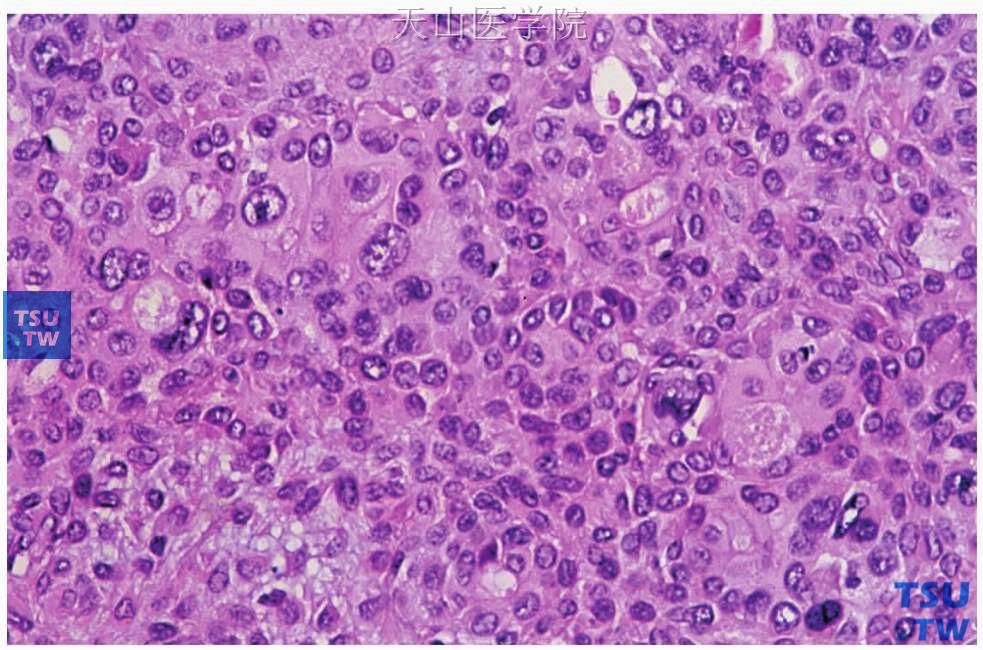
图7-28 多形性腺瘤
肿瘤细胞出现多形性
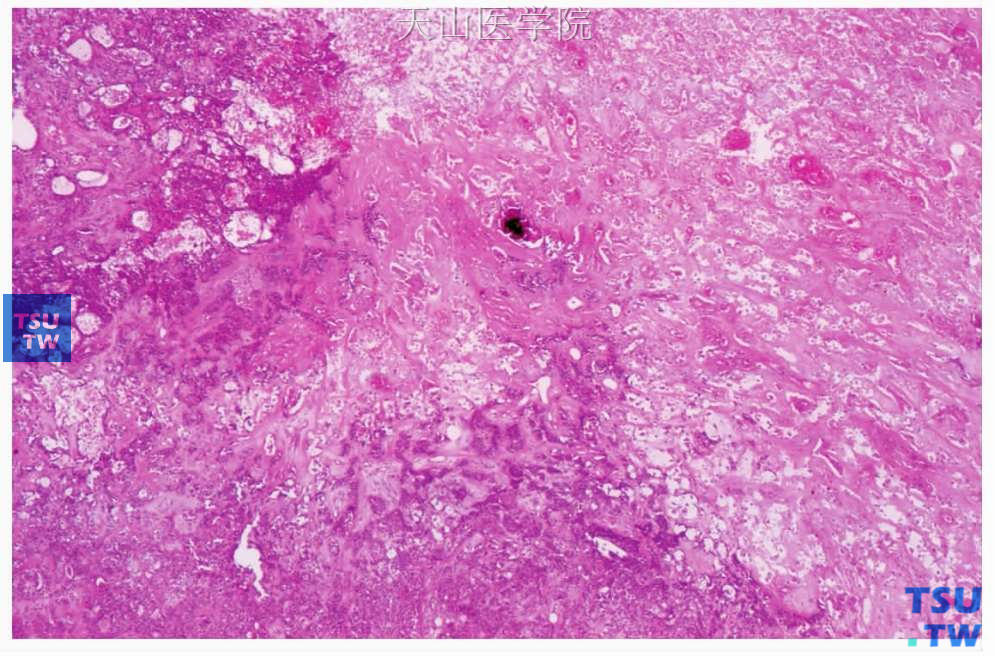
图7-29 多形性腺瘤
肿瘤的坏死成分
免疫组化
导管样结构的腔面细胞:AE1/AE3,CK7、CK8,CK18、CK19,CK20,EMA和CD117阳性;S-100A、TGF-β2、TGF-β3;BMP2、CEA,EGF、BMP6阳性;溶菌酶和乳铁蛋白在部分肿瘤中阳性,主要表达在导管样结构的腔面细胞。神经黏附分子在双层管内层上皮细胞表达强。
肌上皮细胞:较好的肌上皮细胞免疫标记为SMA和Calponin;最近的研究表明Wilms肿瘤基因1 (WT1)蛋白染肿瘤性肌上皮细胞而非正常肌上皮细胞,是肿瘤性肌上皮细胞的敏感标志。此外,肿瘤性肌上皮细胞还表达S-100B、Vimentin、CK14、GFAP、平滑肌肌球蛋白重链(SMMH)、纤维粘连蛋白(FN)、FGF-2、MMP-2和MMP-9、p63、CD10、maspin等。肌上皮细胞广泛表达CD44s和CD44v3和CD44v6。变异肌上皮细胞在免疫标记上有不同反应,如浆样肌上皮细胞表达CK19、BMP2和CK14,少许细胞表达CK18,不表达SMA、SMMHC、CK8,TGF-β3在实性肌上皮巢表达。导管非腔面细胞表达S-100B,而其他实性区、黏液软骨样区的肌上皮细胞S-100A1、S-100A4、S-100A6和S-100B均阳性。CK-1在肿瘤的鳞状化生区有较强表达。
黏液软骨样区的肿瘤性肌上皮细胞周围表达许多细胞外基质如糖氨聚糖(glycosaminoglycans,GAGs)、层粘连蛋白、Ⅳ型胶原、FN、腱蛋白(tenascin)、透明质酸(HA)、蛋白聚糖(aggrecan)、双糖链蛋白聚糖(biglycan)等,这些区域的肌上皮细胞也表达硫酸软骨素I、BMP2、FGF2、FN、Ⅱ型胶原、软骨形态发生蛋白1 (cartilage-derived morphogenic protein,CDMP-1)和GFAP等,提示变异的肌上皮细胞形成了肿瘤中的细胞外基质,参与形成黏液样组织和软骨样组织,与肿瘤的结构多样性有关。
Ki67在肿瘤细胞中的阳性率在大部分研究结果为0~5%,而且阳性细胞多散在于非腔面细胞。
一般来说,免疫组织化学染色在多形性腺瘤的鉴别诊断方面的价值有限。有研究强调GFAP在多形性腺瘤100%弥散性阳性,而多形性低度恶性腺癌肿瘤内只有少许或没有染色,因此GFAP有助于二者间的鉴别诊断。
超微结构
肿瘤中的腺上皮细胞可为呈柱状的导管样细胞、立方状闰管样细胞和呈锥形内含酶原样颗粒的腺泡状细胞。它们的细胞间有桥粒连接。肌上皮细胞的胞质内含直径5~6nm的肌微丝,细胞与间充质之间有基膜样物。其中导管样细胞和肌上皮细胞有形成正常导管腺泡的倾向。黏液样区的细胞为肌上皮细胞构成。软骨样细胞的胞质内可见直径6nm的微丝,粗面内质网扩张,并见囊泡。免疫电镜研究证实肌上皮细胞的胞质中有抗actin和抗myosin抗体标记的肌微丝;胞质内、胞核及核仁中含有S-100蛋白;黏液软骨样区域中,部分瘤细胞胞质内含vimentin和GFAP中间丝,GAGs和aggrecan多分布在非腔面细胞的细胞间隙及黏液样基质区,非腔面细胞细胞内含阳性小泡,一些为高尔基体来源。
遗传学
细胞遗传学发现多形性腺瘤有复杂的核型异常,约占70%的肿瘤。目前发现3种主要遗传学异常:伴8q12重排(39%)、伴12q13-15重排(8%)、不累及8q12或12q13-15的散发性、克隆性变化(23%)。8q12异常的靶基因是PLAG1,编码一种发育调节的、SUMO化(SUMOylated)和磷酸化锌指转录因子,通过识别一种双向共同序列调节多个靶基因的表达。累及8q12的易位多由于启动子交换导致PLGA1激活过表达,使PLAG靶基因表达失调。最近一项基因组范围小RNA表达研究发现,多形性腺瘤中的小RNA表达明显上调。其中有5个基因上调小RNA与肿瘤相关基因组区接近。过表达的小RNA靶基因预测分析显示其多数与肿瘤发生相关的信号通路如WNT,MAPK和JAK-STAT相关。尤为重要的是本组病例有PLAG1基因过表达,而且可能被这些小RNA调节。
肿瘤中12q14-15重排的靶基因是高迁移率族蛋白基因(high mobility group protein gene,HMGA2),HMGA2编码一种结构转录因子,通过修饰DNA的构型启动基因表达。多数HMGA2的断裂点在第三大内含子内,导致DNA结合域和高度酸性的羧基末端结合域分离。在含ins(9;12)和t(3;12)的多形性腺瘤中,已经鉴定了两个融合基因HMGA2-NFIB和HMGA2-FHIT。最近在多形性腺瘤研究中发现WNT抑制因子1(WIF1)基因是一个新的HMGA2融合的伴侣基因,融合后导致HMGA2过表达、WIF1低表达。而在正常唾液腺组织WIF1高表达、HMGA2不表达。提示多形性腺瘤的发生可能与该两个基因的表达失调有关。还有的研究显示多形性腺瘤中扩增基因常为HMGA2和MDM2,并且二者均有高表达。这种扩增和高表达连同其他的细胞遗传学异常一起与多形性腺瘤恶变有关。
目前鉴定的一些含PLGA1和HMGA2融合的基因都是肿瘤特异性的,因此可能作为多形性腺瘤的诊断标志。这些融合可用RT-PCR或者间期荧光原位杂交检测。
近来在4种组蛋白赖氨酸甲基化转移酶(HMT)的研究还发现有三种(SETB1,Eu-HMTase和SET08)在肿瘤组织中较邻近正常组织水平高。此外,还发现部分肿瘤出现p16启动子甲基化,提示甲基化在PA的发生上可能起作用。另外在多形性腺瘤标本中检测到特殊SV40序列,PCR检测阳性者再通过免疫组化检测到多形性腺瘤细胞核表达SV40 Tag抗原,结果提示该病毒在多形性腺瘤发生上起一定作用。人防御素1(human beta-defensin,hBD-1)在多形性腺瘤表达明显较正常腺体低,提示其可能是潜在的抑癌基因。
P53突变在多形性腺瘤不常见,但在恶性多形性腺瘤中较多见。p53蛋白阳性病例数从阴性至30%不等,大部分较低。多数多形性腺瘤的DNA含量为二倍体,异倍体较少见。
鉴别诊断
肌上皮瘤:多形性腺瘤以肌上皮细胞成分为主时,二者鉴别较困难。肌上皮瘤是由单一的肌上皮构成,不出现腺管样分化,黏液样组织较少,与肿瘤细胞索条之间有清楚界限。
文献报道多形性腺瘤中可出现一定程度的细胞大小不一、核深染和核分裂增多等细胞非典型性表现,与癌在多形性腺瘤中的早期非侵袭性癌很难鉴别,二者之间的界限难以划分,目前尚无公认的鉴别标准。有的作者将灶性的非典型性细胞增生与早期的癌在多形性腺瘤中等同看待。所幸的是早期非侵袭性癌的预后很好。一些作者尝试用组织学形态学以外的辅助方法如免疫组织化学来确定多形性腺瘤早期癌变,可能会对鉴别有所帮助。研究显示癌变区Ki67、HER-2/neu、p53蛋白和雄性激素受体表达较多形性腺瘤区强。
对于小的活检标本应注意与多形性低度恶性腺癌、腺样囊性癌鉴别。
富于细胞型多形性腺瘤有时需要与基底细胞腺瘤相鉴别。仔细寻找能发现黏液样区,另外多形性腺瘤的细胞团片大部分无基底膜结构,肌上皮细胞与间质成分呈逐渐过度表现。基底细胞腺瘤的管、团、条索都与间质成分界限清楚,有基底膜。
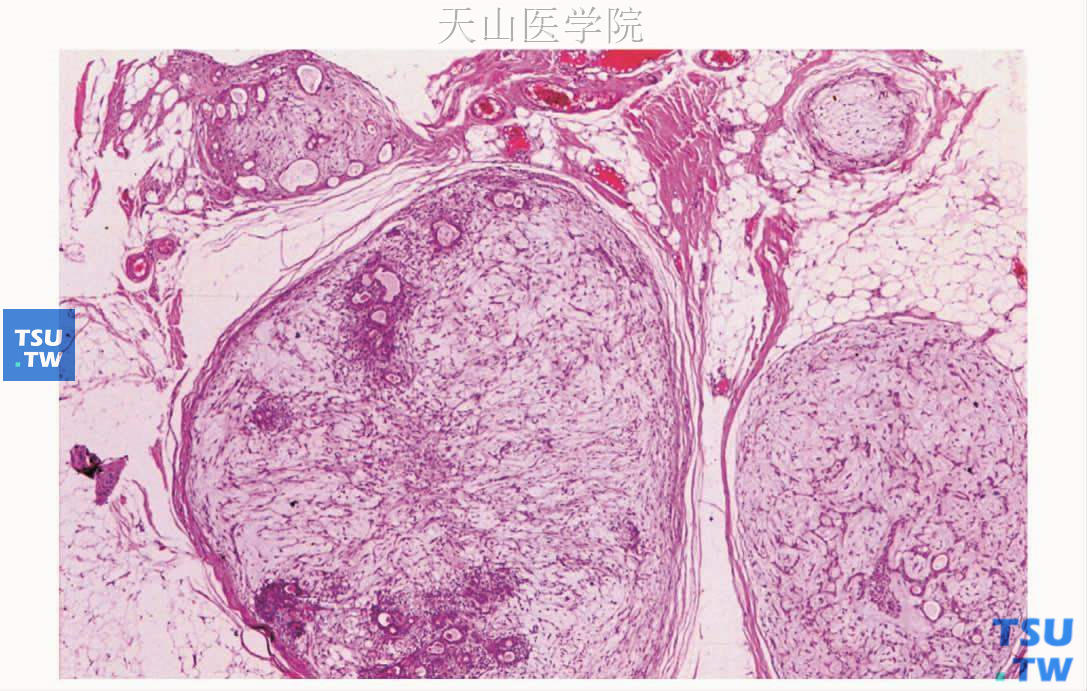
图7-30 多形性腺瘤:肿瘤的种植性复发,多中心生长
预后
多形性腺瘤为良性肿瘤,可有包膜,但包膜内常有瘤细胞侵入,术后易复发,可发生癌变是此瘤的特点。复发率在不同的研究中有很大不同,与治疗方式有关。切除肿瘤的复发率较低,仅摘除肿瘤复发率较高。从复发后形成的多个肿瘤结节看,肿瘤复发与瘤细胞易种植有关,而因此不主张术前切取活检。WHO分类中认为肿瘤易复发的自身原因有:①以黏液样物质为主要成分时,易流散;②有或无包膜或包膜厚薄不一及肿瘤侵犯包膜的倾向;③肿瘤出现包膜下裂隙;④肿瘤结节穿破包膜;⑤肿瘤细胞可能的生物学需要,使细胞本身在进入手术部位时可以生存。
许多复发性多形性腺瘤是多灶性的(图7-30),有时分布非常广泛,以至于不可控制。复发性多形性腺瘤的组织学表现一般与原发性肿瘤无大区别。有极个别的病例报道,原发性单形性腺瘤切除后,原位再次有多中心肿瘤生长,但切除后见多灶性基底细胞腺瘤和淋巴上皮囊肿。复发的多形性腺瘤其生物学行为是否发生改变也受到关注。研究结果有两种:一是与原发性肿瘤较一致、一是生物学行为发生改变。发生改变主要有复发的结节包膜薄而不完整、黏液样亚型为主、小结节的增殖活性相似于或高于大结节、孕激素表达在复发组较对照组高、复发性多形性腺瘤异倍体较多、S期分数高、复发性肿瘤钙依赖性黏附蛋白11(cadherin-11)表达增强和CD44v6的表达在复发前后有变化。多次复发可能使恶变概率加大。
肿瘤生长多年后可发生癌变,癌变表现有多种组织类型,其预后差别较大(详见恶性多形性腺瘤)。
