糖尿病肾脏疾病的主要防治目标是防止DKD的发生和发展,重在预防。一级预防是指防止正常白蛋白尿进展到微量白蛋白尿的防治措施;二级预防是指防止微量蛋白尿进展到临床DKD的防治措施;三级预防是指防止肾衰竭的发生与发展。对DKD应特别强调早期预防,一旦进入临床DKD,其病变往往呈不可逆发展。治疗的目的主要是延缓其发展,降低病死率。根据指南的框架,宏观上DKD的治疗原则如下:
- 严格控制高血糖:达到糖化血红蛋白(HbA1c)<7. 0%;
- 积极控制高血压:CKD1~4期糖尿病患者血压控制目标是低于130/80mmHg。一般用血管紧张素转换酶抑制剂(ACEI)或血管紧张素Ⅱ受体拮抗剂(ARB),可联合利尿剂治疗;
- 适当调节异常血脂:CKD1~4期糖尿病患者LDL-C应低于100mg/dl;
- 降低尿白蛋白:无论血压正常与否,均推荐使用ACEI和ARB;
- 充足的营养摄入:适宜的营养摄入能延缓CKD的进程,对于CKD1~4期糖尿病患者推荐蛋白质摄入量(RDA)为0. 8g/(kg·d);
- 维持适宜体重:罹患糖尿病的CKD患者的目标体重指数应处于正常范围内(18. 5~24. 9kg/m2);
- 特殊情况特殊对待:对于青少年、老年、孕产妇等特殊群体,应采取特殊治疗方案;
- 倡导健康生活方式:包括各层次各阶段的健康卫生教育及适宜的运动等。
严格控制高血糖
无论是否存在CKD,糖尿病患者血糖控制的目标为HbA1c<7. 0%。美国“糖尿病控制与并发症实验研究”(DCCT试验)的结果表明,强化胰岛素治疗使血糖长期控制在接近正常水平能够减少1型糖尿病患者肾病的发生率和延缓其发展。“英国前瞻性糖尿病研究”(UKPDS试验)显示,长期严格控制高血糖,同样可减少2型糖尿病患者DKD的发生。对于1型或2型糖尿病患者,DCCT、UKPDS等大规模临床研究提示严格的血糖控制(HbA1c<7. 0%)可以降低微量蛋白尿的产生以及微量蛋白尿进展至大量蛋白尿的风险和GFR下降的速度。但糖尿病强化治疗易伴发低血糖。一组经降糖治疗,当HbA1c为5. 5% 及10. 5%时,低血糖发生率分别为105次/(100患者·年)与7. 5次/(100患者·年)。糖尿病肾功能不全时更易发生低血糖,且多无典型表现,可以仅有意识淡漠,局限性肢体瘫痪、抽搐、甚至昏迷等。因此,血糖的控制水平应根据患者的受教育程度、年龄、是否可经常检测血糖和对低血糖的自我救护能力等情况综合考虑后再作出恰当的决定。
一旦临床确诊为DKD,为避免口服抗糖尿病药物对肾脏的不良反应,一般主张应使用胰岛素控制血糖,如有困难且GFR尚高于30ml/min者,也可使用格列喹酮(糖适平),因其主要从胆道排泄,仅5%由肾脏排泄。α糖苷酶抑制剂主要竞争性抑制小肠内多糖分解为单糖,适用于餐后高血糖,尤其有反复低血糖发作的患者。另外,一些小规模的短期临床试验提示与饮食控制、磺脲类降糖药、双胍类降糖药物相比,噻唑烷二酮类降糖药能降低尿蛋白,但这是否得益于噻唑烷二酮类降糖药更好的血糖、血压控制,还需要更大规模的临床试验证实。
美国糖尿病协会(American Diabetes Association,ADA)指南认为为了减少糖尿病并发症,HbA1c应小于7. 0%或在不出现低血糖的情况下尽可能使HbA1c接近正常。美国临床内分泌协会、国际糖尿病联盟(IDF)的全球指南、欧洲NIDDM工作组以及中国糖尿病学会等组织均提出HbA1c控制目标应小于6. 5%。以上结论与K/DOQI指南相似,但均未针对DKD提出具体血糖控制目标。
严格控制HbA1c<7. 0%的主要风险是发生低血糖,特别是使用胰岛素治疗的1型和2型糖尿病患者。另外,UKPDS研究使用磺脲类降糖药也会带来低血糖发生的风险。CKD3~5期的患者有更高的低血糖风险,这主要是由胰岛素和口服抗糖尿病药物在肾脏清除率下降及肾脏糖异生功能受损两方面原因造成的。1/3的胰岛素在肾脏降解,肾功能的损害会导致胰岛素半衰期的延长。1型糖尿病使用胰岛素治疗的患者,当血肌酐水平升高(平均2. 2mg/dl)时,其发生严重低血糖的风险增加5倍。另外,肾脏糖异生功能的降低,使患者抵抗由于相对过多的应用胰岛素或口服抗糖尿病药物所造成低血糖的能力随之降低。因此,针对此类患者应加强血糖监测,根据病情及时调整药物剂量。第一代磺脲类降糖药(包括氯磺丙脲、妥拉磺脲、甲苯磺丁脲)的原药及其活性代谢产物均通过肾脏代谢,药物在CKD患者体内代谢半衰期延长,药物蓄积及低血糖的风险大大增加。在第二代磺脲类降糖药(格列吡嗪、格列齐特、格列本脲、格列美脲)中,格列吡嗪和格列齐特在体内无活性代谢产物且不易增加低血糖的风险,CKD患者可以适当选用。那格列奈在CKD患者体内的活性代谢产物增加,而瑞格列奈则无此现象。二甲双胍类药物应避免应用于Scr≥1. 5mg/L(男)或Scr≥1. 4mg/L(女)的患者,因其主要依靠肾脏清除,CKD患者体内二甲双胍药物蓄积会造成乳酸性酸中毒。罗格列酮主要通过肝脏代谢,在CKD患者其剂量不用调整。胰岛素类药物应根据血糖检测的结果调整用量,并不单纯依靠肾功能水平进行调整。另外,临床上还应注意抗糖尿病药物与其他药物(如调脂药物、抗心律失常药物、镇静药物、抗凝药物等)的相互作用,酌情调整剂量。
有一些因素可能会影响DKD患者HbA1c测量的准确性。红细胞寿命的缩短、溶血、铁缺乏均可过低估计实际HbA1c水平,而血红蛋白的氨甲酰化和酸中毒会过低估计实际HbA1c水平。因此,肾衰竭患者与肾功能正常患者体内糖化血红蛋白与血糖水平间的关系并不相同,血液透析和腹膜透析均会影响HbA1c水平。维持性透析的患者,严格控制血糖的目的并非延缓肾功能的恶化,而是延缓视网膜病变、神经病变、大血管病变的进展。良好的血糖控制能提高血透、腹透患者的生存率,HbA1c水平是生存率的重要预测指标。下表是ADA推荐的针对血糖控制的评估标准。
评估血糖控制的ADA标准

积极控制高血压
绝大多数DKD患者均患有高血压,JNC 7指南认为,糖尿病及CKD患者血压高于130/80mmHg即为高血压,血压水平越高,肾脏恶化速度越快,与舒张压、脉压相比收缩压的升高程度更为重要。
高血压是加速肾衰竭进程的最重要因素,抗高血压治疗在DKD早期可减少蛋白尿和延缓GFR下降。一般认为DM患者血压应控制在130/80mmHg以下,进入临床肾病期的患者更应注意严格控制血压,当蛋白尿>1. 0g/24h时,血压控制应<125/ 75mmHg。UKPDS在专文分析中指出,降血压治疗与降血糖相比,成本低而效益高。美国一项2型糖尿病比较强化血糖控制、强化高血压控制及降低血清胆固醇费用-效益分析也显示,按年生活质量改善指标计算,降脂费用最高,降压费用最低。
循证医学已证实ACEI和ARB在DKD患者控制高血压,减少蛋白尿,延缓肾功能进展中的作用。在DKD降压中,ACEI或ARB作为首选药物。因此,综合大量临床试验(CGS、RENAAL、IDNT、ALLHAT等)的结果,NKF指南(2007年)认为:
- 伴有高血压的1型和2型糖尿病合并微量蛋白尿,ACEI及ARB均能延缓DKD进展至大量蛋白尿期;
- 伴有高血压的1型糖尿病合并大量蛋白尿,ACEI能延缓DKD进展和肾衰竭的发生,ARB可能有类似的作用;
- 伴有高血压的2型糖尿病患者合并大量蛋白尿,ARB能延缓DKD进展和肾衰竭的发生,ACEI可能有类似的作用。将ACEI和ARB合用,其降尿蛋白的作用大于单用其中的任何一种药,特别是持续表现为大量蛋白尿或ACR大于500mg/g的患者。
目前ACEI制剂类型很多,根据在肝脏活化或代谢可分为三种类型:①不需活化又不代谢者,如赖诺普利;②需先激活为活性药物并经肝脏代谢者,如依那普利;③经肝脏代谢的活性药,如卡托普利。按结构所含成分不同来区分者:①含SH基者,如卡托普利;②含COOH基者,如赖诺普利、依那普利、贝那普利;③含磷酰基者,如福辛普利。其中福辛普利、贝那普利均具有双通道排泄功能,在肾功能不全时可经肝脏排泄,不易发生蓄积作用。
ACEI的副作用:
- 肾功能降低:ACEI可使肾小球内灌注压下降,对于肾功能不全者可进一步恶化。JNC认为Scr<3mg/dl时可安全使用,如Scr >1. 5mg/dl时需减量使用,并定期观察肾功能变化,患者如并发肾动脉硬化和狭窄时需慎用。
- 干咳:发生率为0. 1%~33%,ACE被抑制后,缓激肽不能被降解而在体内蓄积,严重干扰生活者需停药。
- 急性间质性肾炎、膜性肾病:表现为蛋白尿加重,应用含SH基ACEI时易并发。
- 高钾血症:发生率0. 1%~0. 7%,糖尿病时多合并低肾素低醛固酮血症,在肾功能不全、合用保钾利尿剂、β受体阻滞剂、吲哚美辛等时更易发生。
- 血管神经性水肿:发生率0. 1%,严重者可发生咽喉水肿,甚至窒息。
- 低血糖反应:可使耐胰岛素的糖尿病患者敏感性增强,而诱发低血糖反应。
- 味觉异常、皮疹、血白细胞升高:应用含SH基制剂时易发生。
- HD时如应用带负电荷的透析器,可吸附较多的缓激肽,并诱发过敏反应。
ARB可与血管紧张素Ⅱ受体1亚型特异性结合,因而具有与ACEI同样的降低血管紧张素Ⅱ活性的降压作用,且不干扰缓激肽的降解,而无干咳和皮下水肿的副作用。而血管紧张素Ⅱ受体2亚型不受影响,能有效抑制心、肾细胞的增殖,有利于心、肾等器官重构效应。
利尿剂可有效降低高血容量性高血压,且能增加ACEI降压效果。在限制饮食中水分和钠盐后仍有持续性水肿的患者应适当使用利尿剂,但需除外心力衰竭和局部原因造成的水肿。使用中应从小剂量开始,逐渐加量。利尿剂,特别是噻嗪类利尿剂可加重糖尿病患者的糖代谢、脂代谢紊乱,故利尿剂不作为糖尿病患者高血压的首选药物。DKD患者,特别是已出现肾功能不全或水肿者,高血压较顽固,多需联合用药,才能达到130/80mmHg的降压目标。NKF指南(2007年)认为大多数此类患者应在ACEI或ARB治疗的基础上合用利尿剂。另外,螺内酯还具有降低蛋白尿的作用,其机制可能为拮抗醛固酮,从而降低TGF-β1、胶原Ⅰ和纤维结合蛋白的表达,减轻肾脏微血管壁损伤,但高血钾的风险增加。
对糖尿病高血压患者,也可选用钙通道阻滞剂,但其肾脏保护作用目前还有争论。非二氢吡啶类钙离子拮抗剂在降低尿蛋白方面优于二氢吡啶类钙离子拮抗剂,可延缓尿蛋白大于300mg/d的DKD患者肾功能的下降,降低心血管事件的发生率。但近来BENEDICT研究显示单独使用非二氢吡啶类钙离子拮抗剂并没有降低2型糖尿病伴高血压患者微量蛋白尿的产生,在与ACEI合用时也没有增加其减少微量蛋白尿的作用。大量研究显示DKD患者使用二氢吡啶类钙离子拮抗剂降低尿蛋白的作用弱于ACEI、ARB及非二氢吡啶类钙离子拮抗剂。IDNT试验显示二氢吡啶类钙离子拮抗剂氨氯地平延缓肾脏疾病进展的作用低于ARB的厄贝沙坦,其作用类似于利尿剂和β受体阻滞剂。因此,NKF指南(2007年)认为DKD患者可将二氢吡啶类钙离子拮抗剂和ACEI或ARB联合使用,而不建议单独使用。
一般认为,β受体阻滞剂可能影响血脂代谢、加重外周血管病、降低胰岛素敏感性和抑制低血糖反应,还可能增加糖尿病的发生率。然而,UKPDS研究未能发现卡托普利和阿替洛尔在减少微量蛋白尿和延缓肾功能恶化方面的差异有统计学意义。在另一项对1型糖尿病合并高血压及蛋白尿的患者进行的短期研究中发现,阿替洛尔和依那普利均可以显著降低白蛋白尿,但前者却不能抑制GFR的下降。可见选择性β1受体阻滞剂可适用于DKD。因此,ADA推荐β受体阻滞剂作为治疗DKD的二线降压药之一。然而,由于UKPDS研究人群中DKD的患病率较低,该研究是否有足够样本量来说明两类药对肾保护作用的差异尚难以定论。GEMINI试验显示2型糖尿病合并高血压患者将卡维地洛与ACEI或ARB合用后,能稳定血糖水平、改善胰岛素抵抗,优于美托洛尔,而且微量蛋白尿的新发率比美托洛尔组低48%。
DKD患者血压的控制水平是十分重要的,NKF指南(2007年)认为持续大量蛋白尿的DKD患者(ACR>500mg/g)收缩压应控制在130mmHg以下,而高于110mmHg。下表1为该指南推荐的DKD患者血压控制目标及药物的选择。降压药物(包括ACEI、ARB)应逐渐加量,直至血压达标。表2和表3为指南推荐的降压治疗的随访计划。GFR下降的危险因素包括使用肾毒性药物(非甾体类抗炎药包括COX-2抑制剂、氨基糖苷类抗生素、两性霉素B、静脉用含碘的造影剂、环孢素、他克莫司),血容量不足,肥胖,睡眠呼吸暂停,吸烟,酗酒及临床心血管病(包括脑、心、腹部、下肢)。
表1:DKD患者血压控制目标及药物的选择
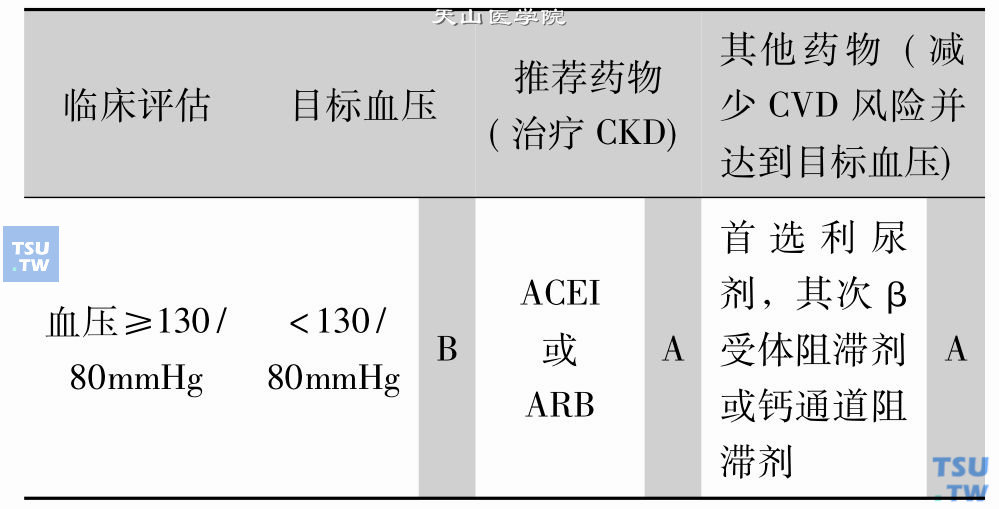
注:阴影内字母代表推荐强度
表2:开始或改变降压治疗后的血压随访间期

表3:血压已经达标且药物剂量稳定时的随访间期

适当调节异常血脂
糖尿病和CKD患者多伴有血脂异常,心血管事件的发生率明显升高,80%的糖尿病患者会进展为或死于心血管疾病,根据美国国家胆固醇教育计划(NCEP)成人治疗组第3次指南(ATPⅢ),糖尿病已被视为冠心病的等危症,此类患者应按高危人群进行治疗。糖尿病和CKD患者通常高密度脂蛋白水平降低,甘油三酯水平升高,小而密的低密度脂蛋白颗粒增加,易导致动脉硬化。伴有微量蛋白尿或大量蛋白尿的2型糖尿病患者,其心血管事件的发生率是尿蛋白阴性患者的2~4倍。因此,CKD可被认为是心血管事件的危险因素。
综合目前大规模临床试验(WOSCOP、CARE、LIPID等)的结果,NKF工作组认为糖尿病和CKD1~4期患者均应降低低密度脂蛋白的治疗,当LDL-C大于2. 60mmol/L(100mg/dl)应开始治疗。根据美国糖尿病学会的推荐,DKD患者当LDL-C>3. 38mmol/L,TG>2. 26mmol/L时应开始治疗。治疗目标为LDL<2. 60mmol/L,TG<1. 70mmol/L。对LDL-C处于2. 60~3. 38mmol/L者,加强生活方式干预。对LDL-C≥3. 38mmol/L者,同时加强生活方式干预及应用降LDL-C药物。药物首选他汀类,次选结合胆酸树脂或非诺贝特。LDL-C已达标,而TG介于5. 2~13. 0mmol/L,可考虑加大他汀类剂量,或加用烟酸或贝特类;如TG≥13. 0mmol/L,为了防止出现胰腺炎发作,应先用贝特类或烟酸以降低TG,待TG<13. 0mmol/ L,再转向降低LDL-C治疗。近来TNT(treat to new targets)研究结果显示阿托伐他汀强化治疗(80mg每日1次)组,其平均LDL-C水平降低为2. 0mmol/L(77mg/dl),对于稳定型冠心病患者的获益显著高于阿托伐他汀常规治疗(10mg每日1次)组。因此,NKF工作组建议高危人群(包括2型糖尿病和CKD1~4期患者)LDL-C的治疗目标为1. 82mmol/L(70mg/dl)。部分调脂药物应用于CKD患者时应根据肾功能水平调整剂量。
血脂异常能影响肾脏局部血流动力学,促进肾小球硬化,且糖尿病血脂异常可加速DKD的进展。但调脂治疗是否能延缓DKD进展目前尚无定论,还需要大规模的双盲、随机、对照临床试验证实。因此,预防心血管事件仍是目前糖尿病和CKD患者评价和调整血脂治疗的主要原因。大量关于他汀类药物和安慰剂的对照研究证实,不需要常规监测肝功能和肌酶,除非患者存在以下情况:①出现临床症状;②合并肌病;③基础肝功能异常;④同时服用其他增加他汀类药物副作用的相关药物。
NKF指南(2007年)推荐CKD1~4期患者至少每年检测一次血脂水平(包括总胆固醇、高密度脂蛋白-胆固醇、甘油三酯、低密度脂蛋白-胆固醇、非高密度脂蛋白-胆固醇),治疗方案调整或临床情况改变时每2~3个月监测一次。
降低尿蛋白
动物实验和临床证据均表明,控制血糖、降低血压是预防和治疗DKD蛋白尿的基础。许多证据也显示,ACEI不仅能降压,而且可以降低DKD患者的尿蛋白,这是独立于降压之外的作用。此外,ACEI和ARB还有保护血管内皮细胞功能、减轻肾组织病变、延缓肾功能不全进展的作用。氯沙坦减少2型糖尿病肾病终点研究及厄贝沙坦DKD研究(irbesartandiabetic nephropathy trial,IDNT)两项大型多中心临床研究显示,氯沙坦及厄贝沙坦能减少DKD的显性蛋白尿,延缓2型糖尿病肾病的进展。厄贝沙坦对2型DM微量蛋白尿影响的研究(irbesartan in patients with type 2 diabetes and microalbuminuriastudy,IRMA2)证实,厄贝沙坦能减少早期2型糖尿病肾病进展至显性DN的机会。2002年的缬沙坦减少微量蛋白尿研究(microalbuminuria reduction with valsartan,MARVAL)证实,无论是否伴有高血压,缬沙坦均能有效减少2型糖尿病肾病的微量蛋白尿,说明ARB 对DKD具独立于降压外的肾脏保护作用。NKF指南(2007年)建议,血压正常的糖尿病患者出现大量白蛋白尿时应该使用ACEI或ARB治疗;减少白蛋白尿应定为糖尿病肾病的一个治疗目标。目前小样本研究表明罗格列酮可降低2型糖尿病患者的蛋白尿,但有待进一步研究证实。
此外,有研究显示蛋白尿的排泄与血、尿肿瘤坏死因子-α(TNF-α)呈正相关,血、尿TNF-α可以作为DKD病情活动的一项重要指标,己酮可可碱(PTX)能降低血、尿TNF-α,减少DKD蛋白尿的排泄,且短期内对肾功能无影响,可延缓肾功能损害的进程。PTX可扩张肾血管,增加肾脏血流,改善糖尿病的血液高凝状态,从而减少尿蛋白,改善肾脏的功能,但缺乏大样本、多中心的研究证实。
充足的营养摄入
大量蛋白质的摄入,可增加肾小球灌注,促使肾功能恶化;然而过度控制蛋白质,胰岛素分泌减少,且蛋白质分解代谢增加,促进负氮平衡,导致营养不良。传统观念只注重血糖控制,限制蛋白摄入对合并CKD1~4期糖尿病患者同样重要。低蛋白饮食能降低肾功能恶化和尿蛋白增加的风险,特别是1型糖尿病DKD患者。低蛋白饮食治疗还可减轻胰岛素抵抗,改善糖、脂肪、蛋白质三大物质代谢,降低血浆肿瘤坏死因子和瘦素水平。研究显示高蛋白饮食(大于20%每日总热量)会增加肾功能恶化和尿蛋白增加的风险。
ADA及《中国糖尿病防治指南》推荐DKD患者蛋白质摄入量为0. 8g/(kg·d);在GFR下降后,蛋白质摄入量应进一步限制至0. 6g/(kg·d)。NKF指南(2007年)建议,每天蛋白质的摄入小于每日总热量的20%,每天每千克体重(理想体重)摄入0. 8g蛋白质食物蛋白,其中50%~70%应以高生物利用度的优质蛋白为主(包括瘦型家禽、鱼类、大豆、蔬菜来源的蛋白质)。在限制蛋白质的同时应适量增加碳水化合物(低糖指数食物为主)和(或)脂肪(ω-3和单不饱和脂肪)摄入以保证足够的热量。ADA推荐碳水化合物应主要来源于谷类,水果,蔬菜和脱脂、低脂乳制品,这些低糖指数食物能降低餐后血糖,从而改善整体血糖水平。另外,膳食纤维有利于糖类和脂类的代谢。糖尿病和CKD患者的饮食较为复杂,每日所需营养素包括蛋白质、碳水化合物、脂肪、钾、钠、磷等。鼓励患者接受经过专业培训的注册营养师指导,对饮食中各种营养成分进行个体化配比。下表为DASH(dietary approaches to stop hypertension)和NKF-KDOQI CPGs(clinical practice guideline)推荐每日营养素的摄入量。
CKD患者每日营养素摄入量
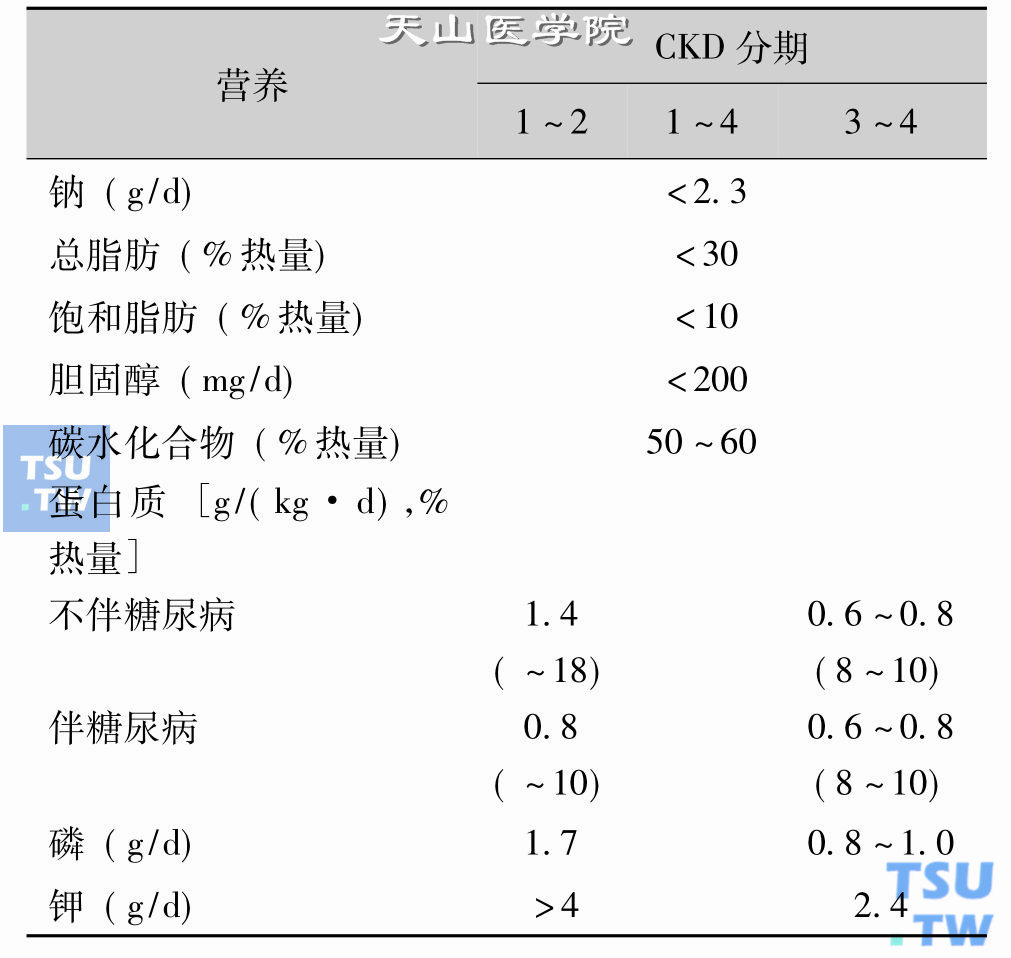
维持适宜体重
NHANES(National Health and Nutrition Examination Survey)显示31%的美国人属于肥胖人群(BMI>30kg/m2)。肥胖是糖尿病、高血压、心血管疾病的高危因素。现在越来越多的证据表明肥胖也是CKD的高危因素,它是否独立于糖尿病、高血压或其他因素目前还无定论。肥胖与慢性肾脏病相关的可能机制包括:①内脏肥胖直接压迫肾脏;②RAS激活;③高胰岛素血症;④交感神经系统激活;⑤营养过剩;⑥肾小球高滤过;⑦蛋白尿相关性肾脏损害;⑧血压升高。
糖尿病和慢性肾脏病患者的目标体重指数(BMI)控制在正常范围(18. 5~24. 9kg/m2)能降低发生CKD及CVD的风险。体重减轻应主要通过合理膳食和适当运动来实现。
特殊情况特殊对待
对特定群体糖尿病和慢性肾脏病的治疗原则与普通人群相同,但在处理儿童、青少年、老人和孕妇时有特别注意事项。
随着儿童、青少年肥胖发生率的增加,其2型糖尿病的发病率也逐年增加。在美国,2~5岁儿童肥胖率大于10%,6~19岁青少年肥胖率大于15%。同时,5岁以下儿童1型糖尿病的发病率也在增加。由于糖尿病的患病时间是DKD的危险因素,儿童、青少年糖尿病发病率的增加必然会导致DKD发病率的增加。由于此类人群低血糖的风险及生长发育的特殊性,ADA推荐儿童和青少年的1型糖尿病和CKD患儿的血糖控制目标不同于成人(下表)。对于2型糖尿病患儿,生活方式的干预是首要的,若生活方式的干预仍不能使糖化血红蛋白小于7%,则需要药物治疗。虽然ADA推荐口服药物是儿童、青少年2型糖尿病的一线治疗药物,但目前只有二甲双胍通过了FDA(Food and Drug Administration)的认证,而且只能用于10岁以上的青少年。有糖尿病和CKD的患儿应避免使用二甲双胍类药物。噻唑烷二酮类药物由于其肝毒性不推荐使用。NKF指南(2007年)推荐儿童、青少年糖尿病和CKD患者血压的控制目标为相同年龄、性别、身高的儿童及青少年血压的第90百分位数或130/80mmHg中较低的一个。虽然还没有通过FDA的认证,NKF和ADA推荐使用ACEI为糖尿病患儿的降压药,若不能耐受可选用ARB。使用ACEI或ARB治疗的青春期少女应注意避孕,一旦怀疑妊娠立即停药。在严格控制血糖和改善生活方式后血脂水平仍很高(甘油三酯>500mg/dl,低密度脂蛋白-胆固醇>160mg/dl)应药物治疗。烟酸衍生物是治疗高甘油三酯血症的有效药物,但目前还未被FDA批准应用于儿童和青少年。他汀类药物是降低低密度脂蛋白-胆固醇的首选药物,阿托伐他汀已被FDA认可应用于儿童和青少年家族性高胆固醇血症患者。ADA推荐儿童和青少年糖尿病患者低密度脂蛋白-胆固醇的治疗目标为100mg/dl。同样,使用他汀类治疗的青春期少女应注意避孕,一旦怀疑妊娠立即停药。儿童和青少年糖尿病和CKD患者应接受经过专业培训的注册营养师指导,避免过高蛋白饮食(蛋白质大于总热量的20%),但考虑到生长发育的需要,同时要避免过低蛋白饮食(蛋白质小于总热量的10%)。
ADA推荐儿童和青少年1型糖尿病和CKD患儿血糖控制目标

老年糖尿病和CKD患者往往存在许多并发症,特别是心血管疾病,同时易出现低血糖、低血压。此类患者降糖、降压、降脂药物的应用适宜从小剂量开始,逐渐加量,严密观察疗效和副作用。老年糖尿病患者尿蛋白的增加不一定与肾功能进展相关,GFR可能是更特异的评价DKD的指标。
患有1型糖尿病伴微量蛋白尿的孕妇,其先兆子痫和早产的风险将增加至8倍,若出现大量蛋白尿其风险将增至30倍;同时,围产期的死亡率也会增加。妊娠前3个月较高的糖化血红蛋白水平,可导致分娩畸形儿的可能。因此,患有糖尿病和CKD的孕妇应按高危人群进行检测和治疗。虽然2型糖尿病孕妇的相关数据目前尚欠缺,NKF指南(2007年)仍建议与1型糖尿病孕妇采用相同的处理原则。
NKF指南(2007年)建议针对糖尿病和慢性肾脏病孕妇的降糖、降压、降脂及营养治疗进行调整(下表)。
糖尿病和慢性肾脏病孕妇的治疗

倡导健康的生活方式
针对多种行为的自我控制策略是多途径治疗方案的关键组成部分,包括监测和控制血糖、血压、营养、戒烟、运动和坚持服药。由于糖尿病和慢性肾脏病行为自我管理方案的复杂性,患者的依从性往往很差,且不能通过说教式教育改善。医生可以给患者设定治疗目标,帮助解决实际问题,并逐步纠正不良生活方式。
糖尿病肾病治疗展望
近来越来越多的学者参与了DKD的基础和临床研究,新的治疗靶点和药物相继推出。
一、改善肾小球通透性:舒洛地特(sulodexide)可通过抑制凝血因子(主要是Ⅹa)和血小板聚集、激活循环中和血管壁的纤溶系统发挥作用。该药口服具有较长的半衰期。它能有效降低DKD患者的蛋白尿,其机制可能是通过恢复肾小球基底膜结构和电荷选择性,最终改善肾小球通透性。2002年,欧洲四国进行了糖尿病患者应用舒洛地特降低尿蛋白的临床试验。该研究共纳入1型和2型糖尿病患者223例,结果表明舒洛地特可显著降低尿蛋白。
二、抗肾小球纤维化:吡非尼酮(pirfenidone)是一种新型广谱抗纤维化药物,具有抗肺、肝、肾、心和腹膜纤维化的作用。动物实验证实其具有可以减轻博来霉素和环磷酰胺引起的肺纤维化。其作用机制可能包括抑制脂质过氧化,减少TGF-β和血小板源性生长因子的生成,从而减轻炎症反应。TGF-β、结缔组织生长因子均为促进肾脏纤维化进程的重要因子。目前重组TGF-β抗体治疗特发性肺纤维化已进入临床研究阶段,而用于DKD的研究只进行到Ⅰb期。抗结缔组织生长因子似乎也能改善肾脏功能。
三、糖基化终末产物抑制剂:目前认为糖基化终末产物是DKD发病的主要因素之一。吡多胺(pyridoxamine,Vit B6)可抑制糖基化终末产物的生成,目前该药用于DKD已进入Ⅱ期临床研究。另外,研究表明DKD患者近端肾小管上皮细胞凋亡与CD36密切相关,而糖基化终末产物可增加CD36表达,因此,CD36抑制剂可能也是一种具有潜力的DKD治疗方法。
四、蛋白激酶C抑制剂:蛋白激酶C激活可促进肾小球毛细血管基底膜增厚,细胞外基质进行性积聚,血管通透性增加,从而促进DKD的发展。甲磺酸水合物(ruboxistaurin)是一种口服的蛋白激酶C抑制剂,目前在DKD研究中的应用已完成了Ⅱ期临床研究,表明该药在2型糖尿病患者中具有明显降低尿蛋白及延缓eGFR下降的作用。
五、过氧化物酶体增殖因子活化受体γ激动剂:既往研究表明噻唑烷二酮药物可降低胰岛素抵抗,改善糖尿病患者高血糖及脂代谢异常,从而间接改善DKD中肾小球功能异常,延缓DKD的发生和发展。而最近研究表明,噻唑烷二酮药物还具有不依赖于胰岛素增敏的直接肾脏保护作用。它通过激活过氧化物酶体增殖因子活化受体γ,发挥改善内皮功能、抗增殖、抗炎、影响RAS、减少细胞内脂质聚集、降低内皮素-1等多种功能,是一类作用广泛、潜力巨大的药物。许多动物实验和临床研究提示此类药物能减少DKD尿蛋白排泄率,延缓肾脏病变的发生发展,但目前还缺乏有力的循证医学证据。
六、肠促胰岛素:1979年,Greutzfeldz将肠促胰岛素(incretin)定义为葡萄糖依赖性、促进胰岛素分泌、起源于肠道的内分泌激素,在营养物特别是碳水化合物刺激下能释放入血,即当血糖升高时会促进胰腺分泌胰岛素。现已证明肠促胰岛素包括葡萄糖依赖性促胰岛素分泌多肽和胰高血糖素样肽1。肠促胰岛素对2型糖尿病具有良好的治疗作用,且有助于治疗肥胖症。然而外源性的肠促胰岛素在体内易被二肽酰肽酶-4很快降解,二肽酰肽酶-4抑制剂将延长肠促胰岛素的体内半衰期,真正起到治疗作用,目前这类药物已进入临床研究阶段。
