老年AML的治疗主要包括:①支持治疗;②传统的强烈化疗:采用类似年轻患者的方案,剂量和年轻患者一样。目的是争取达CR,改善长生存;③低剂量诱导化疗(如小剂量阿糖胞苷,LD-Ara-C);④非骨髓抑制性药物(适合于多数老年患者);⑤临床试验(尤其是一些新药的试用);⑥干细胞移植。
2002年Menzin等曾分析2657例65岁以上的老年AML患者。只有30%的患者(65~74岁的患者占44%,75~84岁的患者占24%,85岁以上只占6%)在诊断后2年内接受了不同形式的静脉化疗。诊断后1年和2年内的死亡率分别为86%、94%。
即使接受化疗,老年AML预后也较差,尽管约50%的患者可以达完全缓解,但复发率很高(正常染色体核型的患者复发率可达80%,复杂核型患者可以高达90%以上),5年总生存一般不到10%。东部肿瘤协作组(ECOG)回顾总结了2882例AML长生存的情况,中位生存期为11个月,55岁以上的患者中位生存期为6个月,5年生存率仅为7. 6%。癌症和白血病B组(CALGB)报道400例老年AML的5年生存率也仅为5%。其他一些报告也显示60岁以上的AML完全缓解率≤60%,3年无病生存(DFS)率<10%,总的中位生存期<12个月。老年AML的治疗及预后现状可见下表。
老年AML的疗效现状
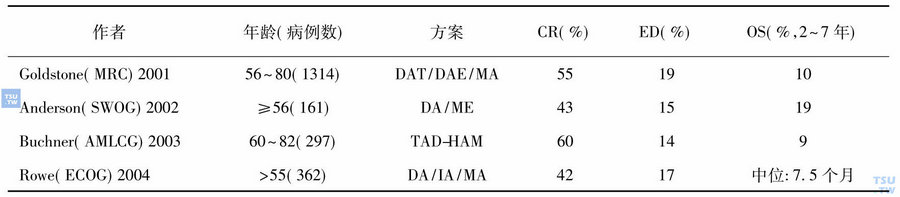
注:CR,完全缓解;ED,早期死亡;OS,总生存。D,柔红霉素;A,阿糖胞苷;T,硫鸟嘌呤;E,依托泊苷;I,去甲氧柔红霉素;M,米托蒽醌
支持治疗
包括血制品输注、抗生素的应用及必要时采用羟基脲控制白细胞数。2006年Menzin等报道的SEER资料分析了3317例老年AML,化疗治疗者的中位生存6. 1个月,而单纯支持治疗者仅为1. 7个月。
传统化疗
诱导治疗
AML诱导治疗的目的是重建骨髓正常造血功能、达到CR,继而通过巩固治疗以求延长生存或治愈。AML的缓解率基本和年龄呈负相关,Johnson等曾报道成人AML的治疗结果:50岁以下的成人AML CR率达70%,50~59岁为68%,60 ~69岁为52%,70~75岁为39%,75岁以上仅为22%。
一、标准剂量诱导缓解治疗
目前临床上应用较多的诱导治疗方案仍是以DA3+7为基础的方案,柔红霉素(DNR)45~60mg/(m2•d)×3天,Ara-C 100mg/(m2•d)×7天(连续静脉输注),但各研究组掌握的用药剂量有所不同。Johnson和Liu等综合15个中心2255例老年AML,以常规剂量的蒽环(蒽醌)类+Ara-C方案诱导治疗,中位缓解率46%(28% ~58%),CR期10. 5(8~16)个月,生存期3(1. 5~9)个月;中位毒性相关死亡率为30%(11%~48%)。这些结果明显不如年轻患者,治疗失败的主要原因为毒性相关死亡和白血病耐药。说明老年AML采用标准剂量阿糖胞苷和蒽环类药物组成方案治疗的效果并不理想,治疗相关死亡率可能超过有效率。
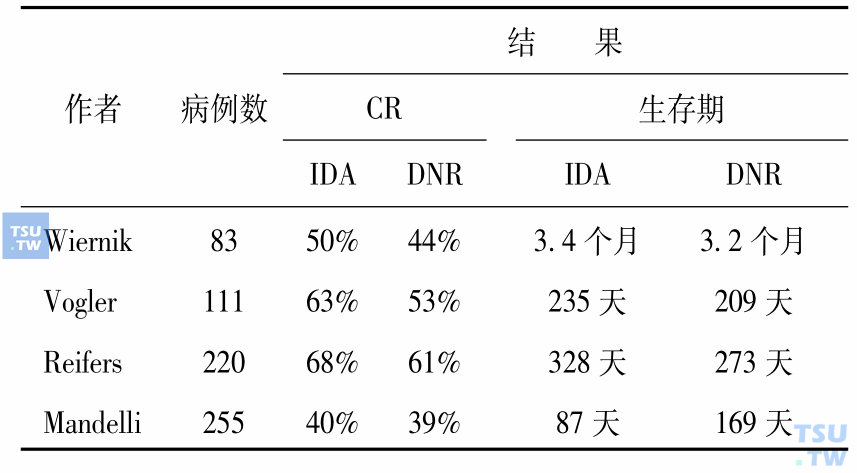
如何提高疗效和降低治疗相关毒性一直是学者们研究的重点。4-去甲氧基柔红霉素(IDA)是一个较DNR更为有效的蒽环类化疗药[常用剂量为8~12mg/(m2•d)×3天],目前有许多关于标准剂量DNR+Ara-C和IDA+Ara-C治疗老年AML的对照报道(下表),多数结果表明在老年AML的治疗中IDA较DNR无明显优势。但也发现DNR组易发生耐药,而IDA组毒性相关死亡增加。
IDA和DNR治疗老年AML的疗效比较
米托蒽醌(MTZ)也被用来替代DNR治疗老年AML。某些非随机治疗结果如Liu等评价了MTZ [10mg/(m2•d)×3天]+Ara-C[200mg/(m2•d)×5天]治疗104例老年AML的结果,CR率为58%,DNR + Ara-C组为64%。Bow等用MTZ[10mg/(m2•d)×5天]+VP-16[100mg/(m2•d)×5天]治疗67例老年AML患者,55%的病例达CR,相关死亡率为12%。
脂溶性DNR已进入临床Ⅲ期试验。GIMEMA 2008年报道的GSI 103 AMLE临床试验随机比较了脂质体柔红霉素(DaunoXome,DNX)与DNR联合阿糖胞苷方案治疗老年AML的结果。DNR(45mg/ m2,d1~3)、DNX(80mg/m2,d1~3)、Ara-C(100mg/ m2,d1~7)。DNR组CR率为78/153(51. 0%)、难治病例发生率55/153(35. 9%)、治疗相关死亡率13. 1%;DNX组CR率73/148(49. 3%)、难治病例发生率31. 8%、治疗相关死亡率18. 9%。CR患者24个月时的复发率分别为78%(DNR)和59%(DNX)。
另外,还有多家大系列、不同诱导治疗方案的报道,完全缓解率40%~62%,诱导相关死亡率14%~26%。见下表。
老年AML传统诱导治疗方案及疗效
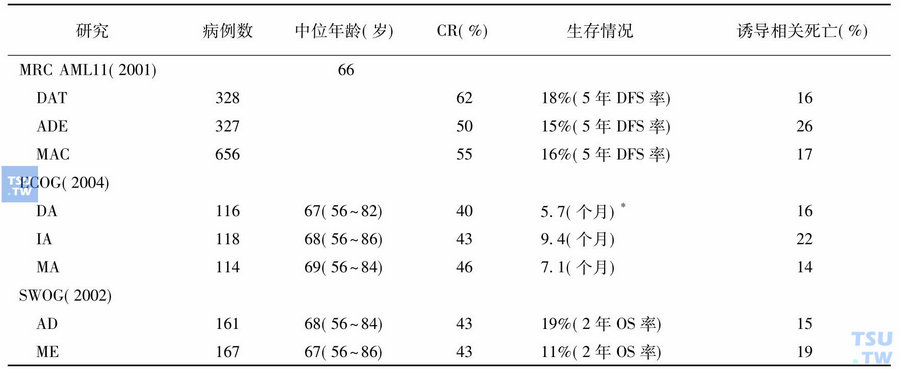
注:DAT,DNR、Ara-C、硫鸟嘌呤;ADE,Ara-C、DNR、依托泊苷;MAC(或MA),米托蒽醌、Ara-C;AD(或DA),Ara-C、DNR;ME,米托蒽醌、依托泊苷;IA,去甲氧柔红霉素、Ara-C
*中位无病生存
随机比较65岁以上人群行强化疗和单纯支持治疗,多数研究结果认为化疗的疗效较好。欧洲肿瘤白血病治疗研究组(EORTC)的早期研究结果将65岁以上老年AML分为两组:①诱导治疗组:DNR 30mg/(m2•d)×3天,Ara-C 100mg/(m2•d)×7天,长春新碱2mg(第1天);②观察组:病情发展时予羟基脲、皮下注射Ara-C等姑息性治疗。两组的CR率分别为58%:0%,中位生存21周:11周,2. 5年生存率13%:0%。也有研究认为强烈诱导治疗与小剂量Ara-C比较无优势可言。
二、降低剂量的诱导缓解治疗
由于毒副作用相对较少,目前有相当比例的学者采用减低剂量的化疗治疗老年AML。Yates等报道采用减少剂量的DNR[30mg/(m2•d)×3天]取得了较高的缓解率(47%),毒性相关死亡率下降(41%)[同期采用DNR 45mg/(m2•d)×3天治疗的患者CR率为31%,相关死亡率为54%]。Kahn采用减少剂量的DAT方案治疗老年AML相关死亡率为15%,而标准剂量的DAT方案相关死亡率为55%,所获完全缓解率相似(30%:25%)。
小剂量Ara-C(LD-Ara-C)是较受欢迎的治疗MDS和老年AML的方案,体外研究证明小剂量Ara-C可以诱导白血病细胞分化。文献报道LDAra-C治疗老年AML的CR率为16%~50%,但在多数患者未能发现LD-Ara-C诱导白血病细胞分化的现象,却注意到LD-Ara-C依然有毒性作用,仍需住院和相应的支持治疗。Tilly等进行了一项多中心的LD-Ara-C和标准强化疗的随机对照研究:LD-Ara-C 为20mg/(m2•d)×21天,对照为佐柔比星(rubidazone)+Ara-C 200mg/(m2•d)×7天;CR率为32%:52%,PR为22%:2%;毒性相关死亡率为10%:31%;两种方案治疗的患者总生存情况无显著差别(8. 8个月:12. 8个月),LD-Ara-C治疗组输血较少、住院日短。英国医学研究委员会(MRC)最近在不适合化疗的老年AML完成了低剂量皮下注射Ara-C (20mg,2次/天,10天/4~6周)与口服羟基脲的比较,低剂量Ara-C可与维A酸联合应用(有研究认为维A酸可以增强AML细胞对Ara-C的敏感性)。217例患者中,低剂量Ara-C治疗者18%达CR,中位CR时间为82周;均明显优于羟基脲治疗组(1%,10周)。维A酸的应用对疗效无影响。其他小剂量化疗包括小剂量三尖杉酯碱、小剂量阿柔比星等,疗效也不尽如人意。
近几年,以CAG(粒细胞生长因子、阿柔比星、阿糖胞苷)或CHG(粒细胞生长因子、高三尖杉酯碱、阿糖胞苷)等为代表的预激方案在老年AML中应用较多,取得了一定疗效,但缺乏随机的、多中心的资料。钱思轩等2008年报道采用CAG方案治疗50例老年AML的疗效,具体方案为Ara-C 10mg/ m2,q12h,皮下注射,d1~14;阿柔比星10mg/d×8天;G-CSF 200μg/(m2•d)×14天(WBC>20×109/L时停药)。CR率为29/50(58%),总有效率为72%;初治病例CR率为23/35(65. 8%),复发难治病例为6/15(40%);中位总生存达14个月。
三、口服诱导缓解治疗
蒽环类药物是AML诱导缓解治疗的基本药物,IDA是目前唯一可口服给药的蒽环类药物,生物利用度可达30%,其生物利用度应同时考虑IDA和其有效代谢产物(idarubicinol)。口服IDA单一用药[20~30mg/(m2•d)× 3天]可取得40%左右的CR,加用LD-Ara-C并不增加疗效。值得注意的是尽管口服IDA治疗的非血液学毒性很小,但仍会导致骨髓抑制。口服IDA [20mg/(m2•d)×3天],加用标准剂量的Ara-C有可能提高疗效。
还有作者采用口服IDA+VP-16治疗老年AML。1994年Ruutu等报道采用口服ETI方案[VP-16,80mg/(m2•d)×5天;6-TG,200mg/(m2•d)×5天;IDA,15mg/(m2•d)×3天]治疗25例老年AML患者,获得60%CR率。缓解后予原方案巩固治疗,中位生存期9. 9个月。同期采用标准剂量TAD5+1方案治疗的患者CR率仅为23%,中位生存期3. 7个月。
四、新药的应用
还有一些新的治疗药物可选择。地西他滨(decitabine)是一种DNA甲基转移酶抑制剂,美国FDA已同意用于MDS的治疗。该药也开始用于老年AML的诱导治疗[20mg/(m2•d),5天一疗程],CR率达29%,有部分染色体核型不良的患者也取得了CR。
克罗拉滨(clofarabine,CaFDA)是第二代核酸类似物。基于CaFDA联合Ara-C有良好的抗白血病作用及可接受的毒性,该方案在老年AML的研究已见报道。MDACC对60例年龄≥50岁的初治老年AML和高危MDS患者应用CaFDA联合Ara-C进行了临床研究,中位年龄61(50~74)岁,AML 54例(90%),RAEB-Ⅱ/CMML 6例(10%)。治疗方案:CaFDA 40mg/(m2•d)×5天(第2~6天,1小时输注),4小时后静滴Ara-C 1g/(m2•d)×5天(第1~5天,2小时输注)。有效者最多可接受6个疗程的维持治疗,维持治疗中CaFDA、Ara-C均改为第1~3天用药。总体反应率为60%(CR率52%、CRp率8%——血小板未恢复正常),均为1~2个疗程取得疗效,诱导相关死亡4例(7%)。CRp患者中位缓解期只有1. 8个月,CR患者的中位总生存期为23. 5个月。副作用包括不超过2级的腹泻、恶心、呕吐、黏膜炎、皮肤反应、肝功能检查异常以及与输注有关的面色潮红、头痛。可见,CaFDA与Ara-C联合化疗对于老年白血病缓解率较高,副作用也是可以接受的,遗憾的是缓解期、总体生存率与其他诱导方案相比较并未得到明显改善。Burnett等对治疗方案进行了修改,单独应用小剂量CaFDA治疗初治老年AML(60岁以上且不适于联合化疗),具体用法为CaFDA 30mg/(m2•d),连续应用5天,每28天重复一次。在可评价疗效的27例患者中,16例(59%)获得了CR。
五、老年AML治疗中应强调的问题
老年AML治疗中的争议之一是,为争取8~12个月短暂的缓解期进行强化疗是否值得?什么情况下值得强烈诱导?MDACC总结了1980~2004年间,采用Ara-C为基础的联合方案治疗的998例65岁以上老年AML患者。54%的患者具有不良的染色体核型(28%为复杂核型),1/3的患者有肿瘤病史或化疗史。45%的患者达CR,诱导治疗相关死亡率为29%,中位生存期为5. 4个月,1年生存率30%,2年生存率16%。多变量分析发现:年龄75岁以上、不良的染色体核型、较差的身体状态、血肌酐超过115μmol/L(1. 3mg/dl)、前驱血液病病史超过6个月、非层流病房治疗、有其他肿瘤病史、白细胞计数≥2. 5×109/L、血红蛋白≤80g/L等为不良的预后因素。约20%左右的患者无或只有1个不良预后因素,CR率达60%以上、1年生存率50%以上;具有4个以上不良预后因素的患者CR率不到20%,1年生存率不足10%。可以说,对诱导化疗反应较好的患者长期疗效最好;标准强化疗仅适合于无或只有一个不良预后因素的患者。
许多老年AML患者以全血细胞减少起病,骨髓中度受累(原始细胞20%~40%)。如果临床稳定,这些患者应等待细胞遗传学资料回报后再做治疗决定。复杂核型异常的患者,采用蒽环类药物+阿糖胞苷的诱导治疗缓解率约为25%(与30天内的死亡率类似),NCCN建议这部分患者参加临床试验。正常核型的老年AML采用去甲氧柔红霉素(或柔红霉素、米托蒽醌)联合阿糖胞苷的诱导治疗,CR率可达40%~50%;NCCN建议这部分患者参加临床试验或采用标准化疗。
在老年AML的诱导治疗中还注意到,由于老年AML多少会具有前期MDS病史,即使骨髓幼稚细胞清除后外周血细胞计数仍可能恢复不到正常水平。因此,许多Ⅰ/Ⅱ期临床试验中疗效判断采用CRi(骨髓幼稚细胞比例<5%,仍存在血细胞减少)。
缓解后治疗
由于老年患者耐受性较差、并发症多,不能耐受反复的强化巩固治疗,限制了强化疗和干细胞移植的应用。而且,目前的资料显示无论采用什么样的缓解后治疗,老年AML的中位DFS和总的生存期一般<12个月。因此,一般认为老年AML采用标准诱导化疗达CR后,应采用原来的药物进行巩固治疗。
德国急性白血病协作组(GALG)报道,强烈巩固治疗后加或不加维持治疗的3年DFS率分别为30%和17%。维持治疗可用6-MP、6-TG、甲氨蝶呤(MTX)或LD-Ara-C等。Bassan等对老年缓解患者用原方案巩固加6-MP和LD-Ara-C维持,平均CR 期12个月,2年生存率24%。法国急性白血病98临床试验[ALFA9803,诱导治疗为4+7方案:DNR 45mg/(m2•d)或IDA 9mg/(m2•d),第1~4天;阿糖胞苷200mg/(m2•d),连续输注,第1~7天;CR 率57%]将取得CR的老年AML患者随机分为两组进行缓解后治疗,一组接受1疗程的标准剂量阿糖胞苷(200mg/m2×7天)+蒽环类药物(IDA 9mg/m2× 4天或DNR 45mg/m2×4天)强化治疗,另一组每月化疗1疗程(阿糖胞苷60mg/m2,q12h×5天,IDA 9mg/m2×1天或DNR 45mg/m2×1天;连用6疗程)。前者的2年DFS率为17%,后者为28%。多疗程巩固组总的住院周期短于强化治疗组、血小板输注少于强化治疗组。
也有报道老年AML缓解后采用HD-Ara-C治疗可以延长生存。Ferrant等对32例缓解的老年AML使用HD-Ara-C(2g/m2,q12h×4天)治疗,3年生存率41%,3年DFS率29%,中位生存期22个月。ECOG采用12个剂量的HD-Ara-C(1. 5g/m2)治疗300余例老年AML患者取得了2年中位生存率30%的疗效,相关死亡率仅2%。而Mayer等对照了标准剂量Ara-C(100mg/m2)、ID-Ara-C(400mg/ m2)、HD-Ara-C(3g/m2)作为老年AML缓解后治疗的结果,没有发现差异。因此,HD-Ara-C一般不作为老年AML患者的常规缓解后治疗方案。
减低预处理剂量的异基因造血干细胞移植由于并发症很多,在老年AML治疗中作用有限。2年总生存率40%~60%,非复发死亡率达20%。NCCN建议在下述两种情况下减低预处理剂量的异基因造血干细胞移植可作为老年AML的治疗措施:①诱导缓解治疗已取得CR,作为缓解后治疗手段;②诱导缓解失败,但肿瘤负荷较低。尽管老年AML患者也开展了自身外周血干细胞移植,但成功的报道很少。
3.造血生长因子的应用
老年AML治疗中应用的造血生长因子主要为粒细胞生长因子(G-CSF 或GM-CSF)。造血生长因子的应用主要有两个目的:①化疗后应用主要是缩短中性粒细胞缺乏时间,减少严重感染的发生率及感染相关死亡。顾虑主要是刺激白血病克隆生长的问题;②化疗前或化疗同时应用是为了促使静止期白血病细胞进入细胞周期,增强S期特异细胞毒药物(如Ara-C)的杀伤作用,提高疗效。
多数研究结果表明生长因子的应用可以缩短化疗后中性粒细胞减少(<1×109/L)的时间,但没有明显降低感染发生和诱导相关死亡率。结果也显示生长因子的应用可以提高缓解率,延长生存期或对治疗结果无显著影响。有些结果提示(如Dombret等的报道)诱导缓解期应用生长因子可以明显改善伴预后不良染色体改变患者的疗效。
近几年来,以CAG(粒细胞生长因子、阿柔比星、阿糖胞苷)或CHG(粒细胞生长因子、高三尖杉酯碱、阿糖胞苷)等为代表的预激治疗方案是造血生长因子应用的较有代表性的例子,在老年AML中应用较多,取得了一定疗效,但缺乏随机、多中心的资料。
免疫治疗
免疫治疗骨髓抑制较轻,这种治疗方法在老年AML应用较广。目前常用的免疫治疗用药主要有白细胞介素2(IL-2),单克隆抗体(抗CD33抗体等)及FLT3配体等。
IL-2用于临床已有很长时间,成为AML缓解后治疗的重要免疫调节剂,但到目前为止其疗效尚无定论。FLT3配体用于肿瘤、白血病治疗主要基于其扩增功能性树突细胞、增加肿瘤相关抗原的摄入和递呈的机制,疗效正在观察中。
几乎90%的AML患者髓系原始细胞表达CD33,抗CD33单克隆抗体作为AML的靶向治疗也已试用于老年AML,由于其对骨髓抑制较轻,Estey认为可降低早期死亡率,适用于具有高危死亡危险因素的患者。GO是一种人源化CD33抗体与强效抗肿瘤抗生素——乙酰刺胞霉素偶联物,与白血病细胞表面CD33抗原结合,进入细胞后释放刺胞霉素,对白血病细胞有明显的杀灭作用。GO在美国获批的适应证为第一次复发或不宜接受强烈化疗的60岁以上AML患者,单药治疗的推荐剂量为9mg/ m2,静脉输注2周1次,共2次。两项GO治疗第一次复发AML的Ⅱ期临床研究中,中位年龄均为61岁,CR+CRp率分别为26%和29%。Larson等报道227例患者的中位OS为4. 9个月,治疗有效者达12. 6个月。GO联合不同化疗方案治疗初发或复发难治老年AML显示了较单药更高的有效性。Ⅱ期临床试验中,GO多采用3mg/m2、6mg/m2或9mg/ m2,2周1次,共1次或2次。初发者的有效率为35%~91%,复发难治者为12%~76%。目前,GO联合标准剂量化疗诱导初发AML的Ⅲ期随机研究正在进行中,MRC AML-15试验的最新结果显示,患者复发率降低,无病生存期延长,受益者多为染色体核型为良好和中等预后者。GO联合白介素11、Bcl-2反义寡核苷酸根纳三思(Genasense)、5-氮杂胞苷(azacytidine)等新药的治疗也在探索中。
其他
环磷酰胺+Ara-C+拓扑替康(topotecan)±维A酸,bcl-2反义核酸+Ara-C+IDA,细胞周期界点调节剂UCN-01+Ara-C治疗老年AML的临床试验正在进行中。
老年AML选择何种治疗要综合考虑患者的预后、一般情况。Latagliata等提出的老年AML强化疗排除标准,不失为有益的参考依据:
- 年龄超过75岁。
- 临床状况评分≥3分。
- 患有需治疗的活动性心脏病或心功能异常(左室射血分数<50%)。
- 肝或肾功能异常:血肌酐或血清胆红素和(或)GPT升高1. 5~4倍。
- 有些临床试验中,有MDS病史或其他前驱血液病史者需排除,尤其是MDS病史超过6个月者。
