单核吞噬细胞具有上百种不同的受体,这可使其接受范围广泛的免疫学上或自身稳定的分子信息。这些受体中有少数是在细胞内,但绝大多数分布在细胞膜上。由于通过占据这些受体而传递信号的转导系统,受体可与该细胞结构的其他部分联系起来,所以单核吞噬细胞能对具有修饰行为的外来信号和生物合成反应剂起反应,即一旦某个配体与其受体结合,单核吞噬细胞就以某种方式,如通过改变其细胞基因的表达、诱导分泌作用或改变其外形等发挥作用。尤其是单核吞噬细胞的有些受体能使其黏附到其他细胞和细胞外基质上,有些细胞结合并消化微生物,能识别经补体调理的细菌代谢分子,并且能对绝大多数细胞因子和生长因子起反应。应用特异性单克隆抗体的结合作用,单核细胞和巨噬细胞的表面受体已经得到阐明。
下表列出了这些受体,它们被作为单核细胞和巨噬细胞的生长、分化、激活、识别、移动以及与其他功能有关的标记。为描述方便可将这些受体分成三类;即介导微生物和颗粒物摄取的受体、介导细胞-细胞间接触的受体和模式识别受体(pattern recognition receptor,PRR)。事实上,其中许多受体具有多重的功能。
单核细胞和巨噬细胞的表面受体

资料引自:Weinberg JB 1999和Faller DV,Mentzer SJ 2000
介导摄取微生物和颗粒物的受体
清道夫受体(MSR)
它能结合和内吞低密度脂蛋白(LDL),特别是脱离接触血管壁成分而被氧化的LDL。脂蛋白受体控制着这些蛋白及其相关脂质进入单核吞噬细胞胞内。一致的看法是单核吞噬细胞可参与动脉粥样硬化斑的形成。这些斑块中含大量的充满胆固醇的单核吞噬细胞,即泡沫细胞。人单核细胞具有许多LDL和乙酰化LDL受体,在体外培养的单核细胞其乙酰化LDL受体(即所谓的MSR)数量明显增加。这种结合胆固醇酯的乙酰化LDL与单核吞噬细胞上的受体结合(不同于LDL的一种受体)并被内在化而进入溶酶体池,经一种酸性脂酶的作用产生游离的胆固醇。这种游离的胆固醇又可被重新酯化成为胆固醇酯,以脂滴形式储存在胞质里。与LDL受体不同,乙酰化LDL受体的水平不受细胞内胆固醇或胆固酰水平的调节。结果上述过程可导致巨噬细胞脂质过饱和,变成泡沫细胞。纯合子家族性高胆固醇血症的病人虽缺乏LDL受体,但却具有正常数量的乙酰化LDL受体。除了乙酰化LDL受体外,单核巨噬细胞还可识别丙二醛化LDL或马来酰化(maleylated)LDL。
单核巨噬细胞和内皮细胞两者均能将LDL变成能被乙酰化LDL受体识别的形式。一个能被乙酰化LDL受体识别的形式是β- VLDL,这可能是其天然配体。β- VLDL见于高胆固醇膳食的动物血浆或血脂蛋白代谢障碍的病人。只有当脱脂化作用产生游离的胆固醇,随后被高密度脂蛋白(HDL)清除,胆固醇才能从单核巨噬细胞中被清除掉。单核巨噬细胞产生和分泌呈磷脂盘(disc)形式的载脂蛋白E。有人认为这些颗粒是由于受卵磷脂-胆固醇酰基转化酶的作用与胆固醇酯一道形成的,在细胞外被装配成一个大球形颗粒,含有一个胆固醇酯的核心和一个含载脂蛋白A1和E的外壳。这种颗粒可能是HDL- C,它转运这种胆固醇到肝脏并在这里进行代谢。在巨噬细胞的各亚型中这类受体的表达各异,而且其中有的还能结合细胞外基质蛋白和菌壁蛋白,诸如磷壁酸、LPS和其他一些物质。
免疫球蛋白Fcγ受体(FcγR)
单核细胞、巨噬细胞、粒细胞以及血小板上均表达IgG的FcγR。现知存在三种性质不同的FcγR,即FcγRⅠ、FcγRⅡ和FcγRⅢ,它们在不同细胞上的表达有很大的差异。FcγRⅠ(CD64)是单核细胞、巨噬细胞以及激活的中性粒细胞上表达的一种FcγR,它通过IgG分子的Fc片段与单体的IgG结合。在激活的单核细胞和巨噬细胞上它表达增加,因此在抗体依赖的细胞毒反应中可能起着中心作用。FcγRⅡ(CD32)是一种广泛分布的受体,它在许多细胞上包括单核细胞、血小板、中性粒细胞、B细胞、某些T细胞以及毛细血管内皮细胞上均有表达。FcγRⅡ能与多聚体IgG,而不是单体IgG结合,参与T细胞的增殖反应以及作为天然杀伤细胞的靶点。FcγRⅢ(CD16)则主要与IgG的免疫复合物结合。该受体存在于中性粒细胞、天然杀伤细胞以及组织巨噬细胞上,它显然是在单核吞噬细胞分化的晚期才出现,因为外周血单核细胞不表达此受体。
所有这三种FcγR特异结合人IgG亚类IgG1和IgG3。巨噬细胞上FcγR与免疫复合物相互作用导致细胞“激活”伴有增强吞噬作用,释放许多产物包括超氧化物、TNF、组织型纤溶酶原激活剂、前列腺素以及白三烯等,并触发呼吸爆发。特发性血小板减少性紫癜(ITP)的主要发病机制是患者体内存在抗血小板抗体,包括血小板相关IgG、IgA和IgM,结果血小板被单核-吞噬细胞系统通过其表面的Fc受体所破坏清除,静脉注射免疫球蛋白(IVIg)对ITP治疗有效的作用机制就是对单核巨噬细胞表面的Fc受体有暂时封闭作用,从而减少血小板破坏,抑制抗体的生成。
补体受体(CR)和gC1qR
补体系统的激活可导致释放许多能特异性结合单核吞噬细胞受体的配体。有四种受体已被证实能与补体C3成分的片段结合。补体受体1(CR1或CD35)与二聚体C3bi结合,补体受体3(CR3或CD11b)与补体C3b片段结合,两者在单核和巨噬细胞上均已被发现。CR3是一种异二聚体的糖蛋白,由两个非共价连接的多肽组成。该多肽的α链的Mr为185 000,β亚单位的Mr为95 000。CR3与白细胞抗原LFA- 1(淋巴细胞功能相关抗原CD11a)和p150,95(CD11c)组成一个共享β亚单位的(CD18)异二聚体的家族,被命名为整合素β2亚家族。这些异二聚体涉及细胞和细胞间的相互作用,并参与结合调理化的颗粒和血浆蛋白以及对各种物质的黏附反应,它们可能也修饰细胞间的黏附。补体片段不仅可识别潜在的病原体感染,而且可促进单核吞噬细胞对病原体的吞噬。但是,由于通过CR的内吞途径能绕过氧化爆发,因而这条途径常被细胞内寄生物,如分枝杆菌(Mycobacteria)、军团菌(Legionella)和利什曼原虫(Leishmania)所利用。
单核巨噬细胞表面还表达一种能与补体成分C1q分子的球状头部(globular head)结合的分子量为33kD的受体,命名为gC1qR,HIV- 1的gp- 120可与gC1qR结合,因此,HIV- 1除了通过CD4分子感染单核巨噬细胞外,也可能通过gC1qR感染单核巨噬细胞。
CD14及其他受体
单核巨噬细胞表面表达CD14分子,CD14能结合LPS和携带多价阴离子的微生物。单核巨噬细胞还具有乳铁蛋白的特异受体。在急性内毒素血症或细菌血症,脱铁的乳铁蛋白由于IL- 1的作用从特异的颗粒中释放出来。这种脱铁的乳铁蛋白,在竞争性结合铁后,可被单核吞噬细胞受体内在化,因此,很可能与类似情况下低铁血症的发生有关。单核吞噬细胞可合成特异的、高亲和力的趋化肽受体,如N-甲酰化的异亮氨酸-亮氨酸-杂丙氨酸-酪氨酸-赖氨酸和N-甲基化的甲硫氨酸-亮氨酸-杂丙氨酸的受体。这些肽不仅能诱导单核吞噬细胞的方向性运动,而且也能引起溶酶体酶的释放和反应性氧族的产生。单核吞噬细胞也同除红细胞以外的所有其他造血细胞一样,可能有促癌剂佛波酯(咐醇酯,PMA)的特异性受体。这些与蛋白激酶C共纯化的受体介导对单核吞噬细胞多重效应。几种不同的激素,即胰岛素、胰高血糖素、甲状腺素、生长激素、前列腺素E、地塞米松、双氢烯丙洛尔(dihydroalprenolol)、1,25二羟维生素D3和卵泡刺激素等对单核吞噬细胞的作用,很可能也是通过特异性受体介导的。此外,单核细胞和巨噬细胞也表达凝血因子Ⅶ和Ⅶa、内啡肽等。
细胞和细胞间的黏附受体
巨噬细胞具有丰富的细胞和细胞间的黏附受体及其配体,能介导巨噬细胞向炎症组织趋化或与其他免疫细胞相互作用。这些受体可分为三大家族,即整合素、免疫球蛋白家族和选择素。单核细胞和巨噬细胞上的主要整合素按它们的共同β链分类是β1和β2亚家族。β1家族(VLA分子)介导单核细胞和巨噬细胞同细胞外基质的结合作用,而且诱导血小板反应蛋白(thrombospondin)、Fn和层连蛋白。β2家族由三个白细胞限制的整合素LFA- 1(CD11a/CD18)、CR3 (Mac- 1,CD11b/CD18)和P150/95(CD11c/CD18)组成。免疫球蛋白超家族成员包括细胞间黏附因子- 1 (ICAM- 1/CD54)、ICAM- 2(CD102)和ICAM- 3 (CD50)以及LFA- 3(CD50)和PECAM(CD31)。LFA- 3同淋巴细胞上的CD2结合。PECAM对单核细胞的渗出活动是必需的。选择素包括L-选择素(CD62L)、E-选择素(CD62E)和P-选择素(CD62P),它们识别单核细胞和巨噬细胞上的寡糖配体,如CD15和CD15s。这些凝集素受体在巨噬细胞识别微生物中似乎也起一定作用。LFA- 1 (CD11C/CD18)及其配体之一ICAM- 1两者均存在于单核细胞上,并介导同型细胞间的相互作用,也包括单核细胞同内皮细胞以及携带相应的受体/配体的淋巴细胞之间的黏附,因此促进抗原的提呈。Mac- 1(CD11b/CD18)在单核细胞的黏附和经受刺激活化的内皮细胞的外渗中显然起着重要的作用。
许多炎性细胞因子,诸如TNF和IL- 1诱导内皮细胞表达ICAM- 1、VCAM- 1和ECAM- 1。VLA-4和单核细胞膜上的其他配体介导同内皮细胞的VCAM- 1和ECAM- 1结合,促进单核细胞向炎症部位的补充。整合素的黏附分子也有转导信号的功能。细胞的激活显然是由同细胞外基质蛋白Ⅳ型胶原和Fn结合的巨噬细胞触发的。其他的黏附分子,包括同CD44分子结合的透明质酸和同CD36分子结合的血小板反应蛋白。唾液酸黏附素(sialoadhesin,CD22)是一种由基质巨噬细胞表达的结合有唾液酸的凝集素,它介导巨噬细胞同骨髓的造血细胞结合,允许关键细胞接触而不激活吞噬作用。
模式识别受体(PRR)
机体免疫系统由两部分组成:先天免疫和适应性免疫。适应性免疫(又称为获得性免疫)应答依赖于对特定抗原具有特异性的B和T淋巴细胞,该系统涉及B细胞的克隆选择,B细胞借此产生抗体来有效地应答外来抗原,但因此过程耗时4~7天,其间病原体完全可击垮宿主,所以,费时长、反应较慢是适应性免疫的主要缺陷。相反,先天免疫系统却能即刻对威胁投入战斗,不必通过复杂的机制来选择对外来或自身物质反应的细胞,也不必通过记忆机制来应对相同威胁的第二次或第三次进犯,先天免疫系统而是通过模式识别受体(PRR)来应答绝大多数病原体享有的共同结构来发挥作用。这些共同的恒定分子结构(invariant molecular signatures)被称为病原体相关的分子模式(pathogen- associated molecular pattern,PAMP)。
PRR为在进化上高度保守的胚系(germline)编码的膜结合或可溶性蛋白的统称,包括Toll样受体(Toll- like receptor,TLR)、胞液内NOD(nucleotide oligomerization domain)样受体(NOD- like receptor,NLR)和RIG- 1样受体(RIG- 1- like receptor,RLR)以及C型凝集素样受体(C- type lectin- like receptor,CLR)等。正是PAMP/PRR的相互作用触发了先天免疫系统。虽然有关TLR的描述可以上溯到100年前,但大多数开创性的研究工作蓬勃兴起于约15年前,如今,对各型PRR及其信号转导途径的研究始终处于免疫学研究的前沿和热点。
Toll样受体(TLR)
TLR为先天免疫细胞表达的跨膜蛋白,可识别入侵微生物,激活信号转导途径,启动免疫和炎症反应,以摧毁入侵者。Toll受体首先在果蝇发现,哺乳动物的TLR家族包括11种蛋白(TLR1~TLR11),最近,两个新成员TLR12 和TLR13在小鼠细胞上被发现,但对它们的了解并不深入。TLR由三部分组成:胞外富亮氨酸重复序列区(LRR)、跨膜区和被称为TIR(Toll- interleukin- 1 receptor)同源结构域的胞质尾巴。不同的TLR充当各种配体的受体,这些配体包括细菌细胞壁成分、病毒单链或双链RNA以及小分子抗病毒或免疫调节复合物等。
TLR、病原体及其衍生物
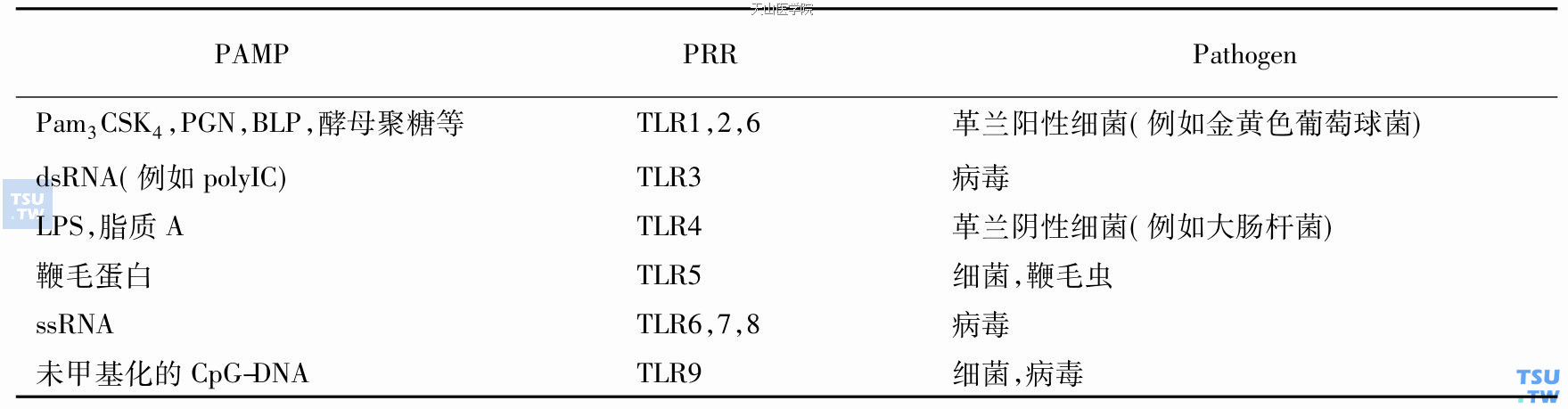
注:BLP:bacterial lipopeptide,细菌脂肽;PGN:peptidoglycan,肽聚糖
一旦TLR的胞外LRR与其相应的配体结合,TLR就被激活。人TLR1、2、4、5和6位于细胞膜上,主要对细菌表面相关的PAMP起反应。而TLR3、7、8和9则位于内体(endosome)表面,其配体主要为源自于细菌和病毒的核酸PAMP。TLR主要激活两条信号途径,其中之核心信号途径,经过接头蛋白MyD88(myeloid differentiation factor 88)或TRIF(TIR domain- containing adaptor inducing IFN-β)传递信号,导致转录因子NF-κB(nuclear factor-κB)以及包括p38和JNK(c- Jun N- terminal kinase)在内的MAPK (mitogen- activated protein kinase)的活化。涉及TLR3和TLR4的第二条信号途径则导致NF-κB和另一个转录因子IRF3(interferon regulatory factor- 3)的活化,结果诱导大量的免疫和炎症蛋白包括细胞因子和趋化因子基因的表达,如抗病毒细胞因子IFN-β等,或许最重要的早期表达基因是趋化因子,因它能把吞噬细胞吸引到感染部位来。
先天免疫应答是机体逐渐进化而成的一组复杂的相互作用机制,从而使机体清除病原体的反应臻于完善,以最大限度地保护机体免遭外周环境中各种病原体的侵袭,严密地组成了机体抵御病原体的第一道防线。TLR4是革兰阴性细菌毒素脂多糖(LPS)的受体,LPS激活TLR4所引发的信号转导途径是研究得最清楚的膜结合TLR的典型代表。单核巨噬细胞、DC和肥大细胞组成了先天免疫的三种前哨细胞,TLR也主要表达在这三种细胞上。然而,TLR在人类细胞上的表达具有高度异质性,这与遗传和个体发育的不同阶段有关,可影响个体对感染、炎症性疾病、过敏以及自身免疫病的易感性。另一方面,病原体无节制地激活TLR反而又会导致严重的临床后果,如休克、炎症性疾病和自身免疫病,因而在多个不同的水平上存在许多TLR活化的负性调节蛋白,如TAM(Tyro3/Axl/Mer)受体酪氨酸激酶蛋白家族即是最近发现的其中之一。值得注意的是,PRR/ PAMP相互作用并非仅限于先天免疫,其在机体先天免疫向适应性免疫过渡中也起着重要的作用,如早期的细胞因子信号可以激活抗原递呈细胞以及辅助Th1细胞的分化和调节等。因此,TLR及其信号分子已成为寻找新的感染、过敏、自身免疫病甚至肿瘤治疗剂的新的靶标。
C型凝集素样受体(CLR)
CLR这一术语是指以钙离子依赖方式结合配体的糖结合分子,即这种受体结合其配体——糖时必须有钙离子存在。巨噬细胞和DC表达的CLR以Ⅱ型跨膜受体为主,并且仅包含一个糖识别结构域(CRD)如DC- SIGN (CD209)、SIGNR1-4、dectin- 2、朗格汉斯细胞特异蛋白(langerin,CD207)和血液DC抗原- 2(BDCA- 2)。此外,也存在Ⅰ型跨膜CLR,如MMR(CD206)和DEC- 205(CD205),它们包含有多个凝集素样结构域,但仅部分CRD具有糖识别功能。下面重点介绍MMR和dectin- 1。
巨噬细胞甘露糖受体(MMR)为识别甘露糖/岩藻糖- N-乙酰葡糖胺化糖蛋白的受体,该受体已被命名为CD206。MMR为分子量175kD的Ⅰ型跨膜分子,存在于成熟的非活化的巨噬细胞上,其在摄食酵母细胞壁颗粒(如酵母聚糖zymosan)和卡氏肺孢子虫过程中,MMR可介导巨噬细胞内吞、吞噬和依赖ROI的细胞毒性。这些受体由钙依赖的重复结构域即C-型结构域组成。现今已报道的这类受体还包括由8个和10个连续的C-型植物凝集素结构域组成的受体DEC- 205(dendritic cell receptor for endocytosis- 205)。
dectin- 1因首先在DC表面发现而得名DC相关性C型植物凝集素- 1(DC- associated C- type lectin-1),属于Ⅱ型CLR,仅包含有一个CRD,且因其结合配体时并不依赖钙离子而不同于传统的CLR如DC- SIGN,而是更类似于NK细胞表达的结合MHC-Ⅰ和MHC-Ⅰ样反受体(counter- receptor)的CLR。dectin- 1的主要表达细胞包括单核细胞、巨噬细胞和DC等。dectin- 1的配体为(1→3)-β- D-葡聚糖(glucan),简称β-葡聚糖,β-葡聚糖为真菌、某些细菌,尤其是真菌细胞壁的主要成分。真菌感染患者血液中会出现β-葡聚糖,被称为葡聚糖血症(glucanemia),目前国际上多家公司开发的诊断真菌感染的试剂盒,如Fungitec test,就是检测患者血液中β-葡聚糖的含量,被称为G试验。日益增多的证据提示,β-葡聚糖- dectin- 1介导巨噬细胞对真菌的吞噬活性、炎症反应包括促炎细胞因子和反应性氧素的产生。β-葡聚糖- dectin- 1信号转导途径正在得到阐明。随着癌症化疗、免疫抑制剂的应用、AIDS等免疫受损患者(ICH)的不断增多,真菌感染已成为日益严峻的医疗挑战,β-葡聚糖- dectin- 1信号转导途径的阐明可为真菌感染带来全新的治疗模式。
