多元醇通道活性增加与myo-肌醇储备耗竭
多元醇通道是葡萄糖代谢的一种途径,葡萄糖在磷酸葡萄糖氧化系统及还原型辅酶E(NADPH)的参与下,经醛糖还原酶催化转变为山梨醇,再通过山梨醇脱氢酶在辅酶Ⅰ(NAD)的参与下氧化为果糖。这个过程还涉及若干酶系统及氧化还原系统,比较复杂。从目前的研究结果来看,通道的前半部即由葡萄糖转变为山梨醇的阶段比较重要,因为它涉及谷胱甘肽的氧化还原过程、NO合成酶及myo-肌醇-磷酸肌醇代谢系统。除了葡萄糖外,其他醛糖如半乳糖,也能被醛糖还原酶催化转变为半乳糖醇。后半部山梨醇转变为果糖过程中,有辅酶Ⅰ参加,随着反应的进行,还原型辅酶Ⅰ(NADH)增加,NADH/NAD的比值增大,它在高血糖假性缺氧(hyperglycemic pseudohypoxia)中起着关键性的作用。此外,果糖比葡萄糖更容易被氧化,产生更多的AGE(下图)。
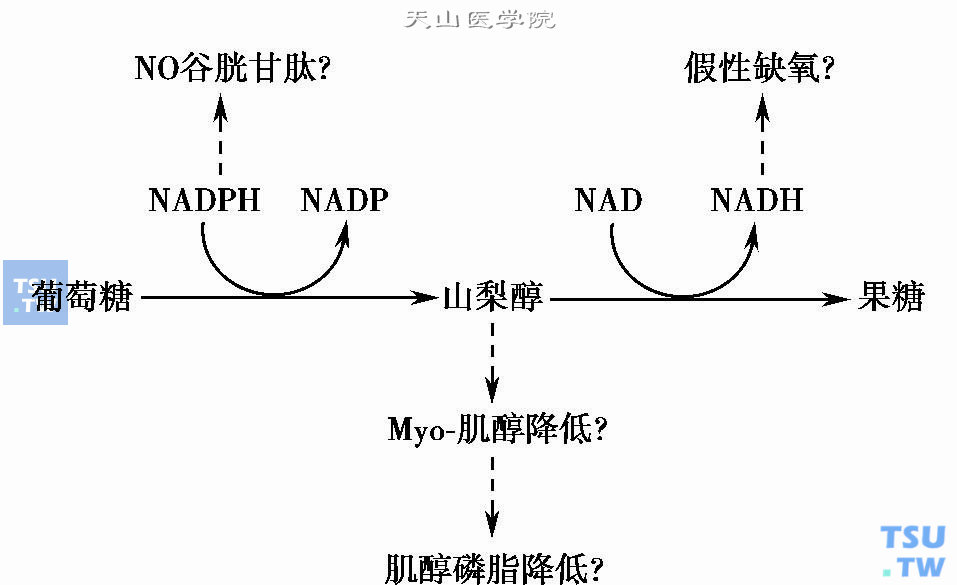
多元醇通道及其影响(Norman E. 1997)
高血糖状态时,多元醇通道活性增加,导致细胞内山梨醇的增多,细胞膜上Na+-K+ATP酶活性降低,并使细胞外液中myo-肌醇(以下简称肌醇)进入细胞受到抑制,细胞内肌醇储备逐渐耗竭,尿中肌醇排出量增多。肌醇是构成肌醇磷脂的主要成分。肌醇磷脂是一个非常重要的信息传递者,主要将细胞膜上得到的信息传递到细胞内。
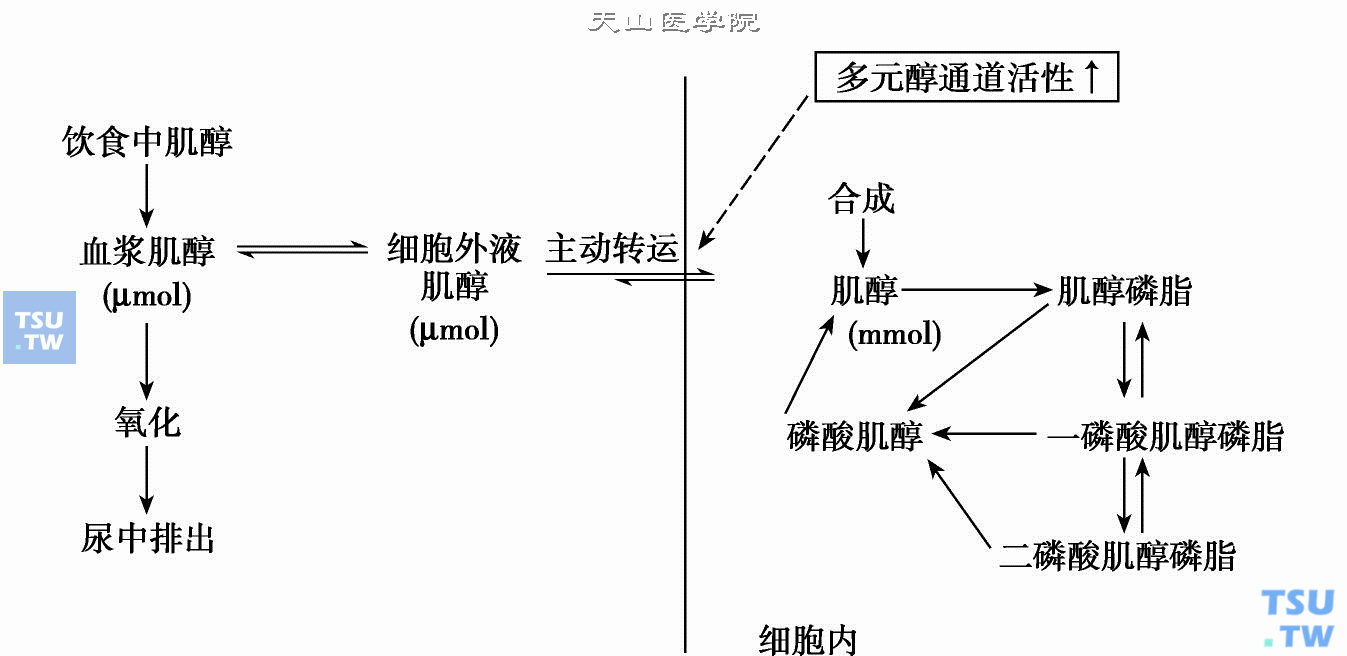
肌醇代谢示意图(虚线代表抑制作用)
上图大致表达了这一过程。当细胞上的受体接受信息后,激活了磷酸酯酶C,在它的作用下,二磷酸肌醇磷脂分解为二酰甘油及三磷酸肌醇,前者可以激活蛋白激酶C,与广泛的蛋白质磷酸化过程相联系;后者可以启动钙库,促进钙的释放。在这两方面反应的协同作用下,引起生理反应。肌醇主要来源于食物,血浆中肌醇到达细胞外液后再转运进入细胞内。这是一个主动转运过程,因为细胞内肌醇的浓度要高出细胞外液数百倍。多元醇通道活性增加,可抑制这一转运过程(下图)。
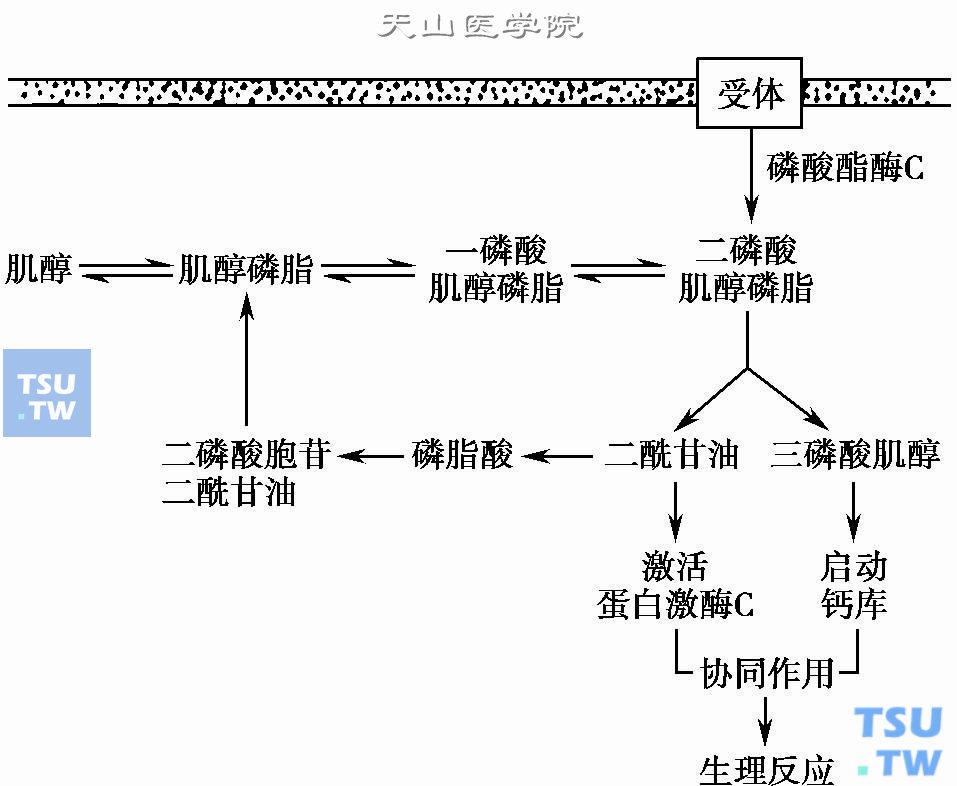
肌醇-肌醇磷脂与生理反应
在细胞内肌醇及肌醇磷脂都有一定的储备库,可能是维持正常生理功能的物质基础,它们的减少与耗竭显然会对生理功能造成影响。目前还不清楚究竟有哪些生理功能会受到影响,以往一直认为Na+-K+ATP酶活性降低及神经传导速度减慢与此有关,然而近几年的一些研究结果与这种看法并不一致。例如以myo-肌醇喂饲糖尿病鼠,使其神经组织中肌醇含量得以纠正,但神经传导速度并不能恢复。Loy等曾测定了实验性糖尿病兔角膜各个组织层,主动脉肌内膜,左心室及窦房结,视网膜及肾脏中的葡萄糖、山梨醇及肌醇含量,发现在角膜、主动脉肌内膜中肌醇的水平不是下降而是升高,在视网膜及肾脏中,也不是每一个解剖部位组织中的肌醇量都是降低的;视网膜色素上皮层中肌醇量是降低的,但脉络膜血管层的肌醇量并没有改变;肾小球的肌醇量降低,但肾乳头的肌醇量却升高。从多年的糖尿病患者的神经穿刺取样的标本中,也未见到肌醇量有所改变。这些实验结果说明,多元醇通道及myo-肌醇耗竭的假说,还存在不少需要澄清的问题,仍然有待进一步的研究工作予以阐明。
多元醇通道活性增加与组织损伤
早在30多年前,就发现糖尿病鼠的晶状体中有过多的山梨醇堆积。此后的研究工作陆续报道了实验性糖尿病动物的外周神经、视网膜微血管基底膜、晶状体及红细胞等都有较高的山梨醇水平及低水平的肌醇,与此同时,动物的神经传导速度减慢,并有白内障及微血管病变发生。还有实验表明,如果以半乳糖喂饲动物产生高半乳糖血症时,也能使犬或大鼠发生白内障,视网膜毛细血管基底膜增厚及周边细胞消失等病变;在神经组织中有半乳糖醇蓄积,也会引起神经传导速度减慢。所有这些组织损伤及功能减退的情况都与糖尿病患者所表现的症状相似。在研究多元醇通道与组织损伤的关系中发现,通道的前半部似乎更为重要,因为使用醛糖还原酶抑制剂,可以使糖尿病鼠的神经传导速度减慢得以改善,并能增加神经内膜的血流供应,提高细胞Na+-K+ATP酶的活性;而使用山梨醇脱氢酶抑制剂则不能显示这些效果。另一方面,用高半乳糖血症鼠的实验结果也说明了这一点。半乳糖可以通过通道的前半部,而生成半乳糖醇,但它却不能通过后半部,因为半乳糖醇不是山梨醇脱氢酶的底物,所以高半乳糖血症鼠的神经传导功能仍然可以受到影响。研究工作还发现,糖尿病神经病变主要是由于神经的血液供应不良所造成,因为血管扩张药可以增加糖尿病鼠的神经血流供应,也能改善神经传导功能的损伤。醛糖还原酶抑制剂所具有的改善糖尿病动物神经病变的作用,也与它能改善神经内膜的血流供应有关。
这是因为在葡萄糖转变为山梨醇的过程中需要有NADPH参与,NADPH不仅是多元醇通道中醛糖还原酶催化反应的辅酶因子,而且也是NO合成酶的辅助因子。在高血糖状态时,多元醇通道活性增高,加快了葡萄糖的转化过程,同时也消耗了较多的NADPH,竞争性地使NO合成受到抑制,NO生成的减少造成血管收缩,组织缺血及神经传导速度减慢。醛糖还原酶抑制剂使葡萄糖转化受阻,同时也减少了与NO合成酶之间对NADPH的竞争,使血管及神经功能的改变得以恢复。另一方面,如果在应用醛糖还原酶抑制剂以后,再应用NO合成酶抑制剂,则糖尿病动物由醛糖还原酶抑制剂改善的神经功能(如神经传导速度加快及Na+-K+ATP酶活性的增加等)又再度受到抑制,但神经细胞中的山梨醇及肌醇的含量则未受到影响,进一步证实了山梨醇通道与NO合成酶之间的关系。NADPH还涉及另一个酶系统,即谷胱甘肽氧化还原的酶系统。NADPH是谷胱甘肽还原酶的辅助因子,在NADPH的辅助下,谷胱甘肽由氧化型转变为还原型(GSH),后者是消除体内氧自由基的重要物质。已经知道氧自由基对血管内皮及NO均有直接作用,除了能降低NO对血管平滑肌的松弛作用外,还能直接损伤血管内皮细胞。在内皮细胞培养实验中可以看到,在高浓度的葡萄糖条件下,谷胱甘肽的氧化还原系统受到影响,致使GSH及NADPH都明显减少。还有的研究证明糖尿病鼠在给予GSH后也能增加神经内膜的血流量,并使神经传导速度减慢也获得改善。
醛糖还原酶抑制剂
在多元醇通道假说中,醛糖还原酶抑制剂的应用不仅对糖尿病所造成的组织损伤给予理论上的说明,而且也证实了它能有效地改善糖尿病动物所造成的血管及神经病变。醛糖还原酶抑制剂用于临床已有多年的历史,常用的品种有ponalrestat、alrestatin、sorbinil、tolrestat、epalrestat等,它们大都是羧酸类衍生物。这些药物开始广泛用于糖尿病患者的神经、肾脏及视网膜病变,也有用于白内障及角膜愈合等的治疗,但效果并不满意。近几年来大多数临床试验集中在用于糖尿病神经病变方面的观察。试验设计多考虑到随机、双盲及对照等原则,观察时间大都在一年以上。从这些临床报告看,结果各有所异。有的报告认为患者应用药物后,可以使疼痛、震颤阈以及感觉、运动神经传导速度均有所改善,明显优于对照品。但也有不少否定的报告。因此还不能完全肯定药物的有效性,仍有待进一步肯定。Pfeifer等认为在临床试验中应该注意一些容易忽视的问题,这对得到一个明确的药物评价非常重要。
- 在病例选择上应考虑病变的严重程度,以中度的、诊断明确的神经病变为宜。
- 有较长的观察时间可以观察到治疗及对照组都有一明显的病情变化过程。
- 要有能够进行统计学处理的足够病例及观察数据。
- 在实验方法学上需要规范化,并注意监测质量。
- 对所用药物应有药代动力学的资料,特别是要了解药物在神经组织中的分布情况。(张铁梅 南国柱)
