糖尿病患者并发和合并大、小血管病变与血液高凝状态有着密切关系。病情未控制好的糖尿病患者除了高血糖和血脂代谢异常外,由于血小板膜上胶原纤维葡萄糖苷转移酶活力增强,促使血小板与胶原纤维相互黏附;因生长激素的影响刺激血管内皮细胞释放第Ⅷ因子中vWF因子而在血液中的浓度增多,促使血小板易于黏附于已损伤的血管内皮下层,并使其对ADP及肾上腺素产生的血小板聚集反应增强;糖尿病患者存在内皮细胞损伤使内皮素产生增加、NO及前列环素合成减少;血小板功能亢进使血栓素A2(TXA2)合成增强,血小板第Ⅳ因子、α颗粒蛋白-140及β-血小板球蛋白释放增加;糖尿病患者纤溶酶原激活物释放减少,使纤溶酶原生成纤溶酶降低,则血管内防止凝血作用下降,易于形成血栓;红细胞黏附性增强和变形能力降低以及凝血酶活性增强而抗凝血酶Ⅲ活性降低等综合因素,往往促使糖尿病患者血液黏稠度增强而处于高凝状态,易于导致大、小血管并发症和合并症的发生。
糖尿病患者血液中存在的高凝状态与血小板的功能异常关系密切。所以,降低血液高黏稠度状态的抗血小板药物已在临床上广泛应用,其中小剂量阿司匹林是目前临床上常用的一种较安全、有效而又廉价的抗血液高凝状态的药物。阿司匹林是一种环氧化酶抑制剂,使该酶第530位的丝氨酸残基乙酰化,破坏了酶活化中心,从而阻断了TXA2的合成。阿司匹林使用的剂量问题一直存在着争论,由于抑制TXA2所需要的阿司匹林浓度低于PGI2,其原则是选择一种对PGI2形成影响最小而又能完全抑制TXA2形成的阿司匹林剂量,以提高其抗血栓作用而减轻副作用。ADA推荐服用阿司匹林80~325mg/d的剂量作为任何有大血管病变证据患者的二级预防。将阿司匹林保持一定的血药浓度,可以抑制血小板TXA2的合成,以降低血液黏稠度。我国的相关实验结果表明,国人服用阿司匹林60~100mg/d的剂量可以达到这一作用。
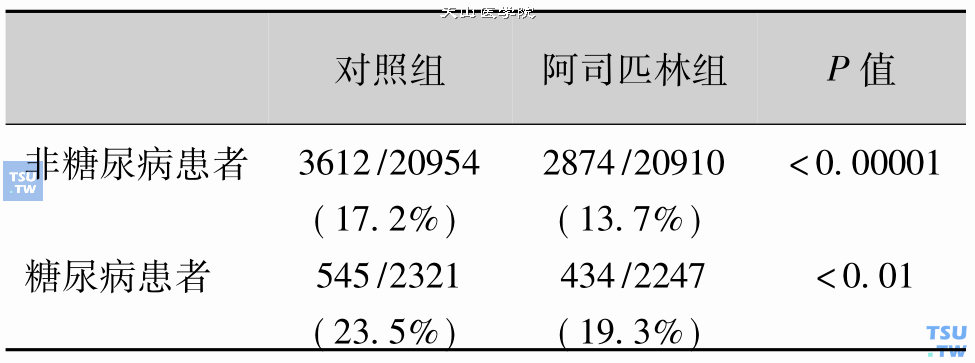
临床上已有血管疾病的糖尿病患者,长期服用阿司匹林可降低心肌梗死,脑卒中、血管性死亡发生的危险性。有报道可降低血管性疾病发生率约1/4、非致死性心肌梗死和脑卒中发生率大约1/3、血管性死亡大约1/6,而非血管性死亡没有增加。表46-8是阿司匹林抗血小板作用的血管性事件发生的对比研究结果。
阿司匹林抗血小板作用血管事件发生率
“阿司匹林对健康研究的报告”(SCPHSRG亚组分析)是选择成年男性无血管并发症和合并症的糖尿病患者533例为研究对象,随机、双盲、安慰剂对照试验分为试验组275例隔日口服阿司匹林325mg,对照组258例口服安慰剂。平均随访5年。其结果显示,服用阿司匹林组心肌梗死发生率为4. 0%(11/275),危险性39%;安慰剂组心肌梗死发生率为10. 1%(25/258),危险性58%,前者明显低于后者。另有一份报告“糖尿病视网膜病变早期治疗的研究:阿司匹林对糖尿病患者死亡率和发病率的影响”(ETDRS),选择有糖尿病性视网膜病变和部分患者有心血管合并症或有心血管疾病危险性的糖尿病患者3711例,随机、安慰剂、对照试验,分为试验组口服阿司匹林650mg/d,对照组口服安慰剂。平均随访5年。结果显示,服用阿司匹林组患者的总死亡率虽有降低,但无统计学差异,但致死性和非致死性心肌梗死在服用阿司匹林组有289例(16%),对照组为336例(18%)(P=0. 038)。大剂量阿司匹林未增加已有视网膜病变恶化和玻璃体积血的危险性,也未增加胃肠道出血或出血性脑卒中的危险性。
糖尿病患者使用阿司匹林的指征:
在临床治疗中,所有的糖尿病患者都可以使用阿司匹林治疗,以降低血液黏稠度。但有下列情况之一者可考虑不用:
- 1型糖尿病患者无任何能诱发血管性疾病并发症的危险因素;
- 2型糖尿病患者无任何能诱发血管性疾病并发症或合并症的危险因素;
- 对阿司匹林过敏、胃肠道出血、溃疡性疾病、出血性体质及其他临床上对阿司匹林有禁忌的患者。
临床综合评价,有下列糖尿病性血管并发症或合并症危险因素之一者,可考虑加用阿司匹林治疗:
- 肥胖者:体重超过标准体重的20%;
- 高血压患者:血压>18. 7/12kPa;
- 过去或现在仍吸烟者;
- HbA1c>8%;
- 尿白蛋白排泄率≥30mg/24h;
- 血清LDL-C>3. 36mmol/L;
- 血清TG>2. 8mmol/L;
- 血清HDL-C男性<1. 0mmol/L或女性<1. 3mmol/L;
- 血液纤维蛋白原大于正常上限水平的25%;
- 血液PAI-1大于正常上限水平的25%。
