应用解剖
肝脏韧带
(1)镰状韧带将肝的膈面分成左右两部分,是左叶间裂表面的标志,其下端与肝圆韧带相连,上端向后延伸与两侧的冠状韧带相连。
(2)肝圆韧带自脐而达肝圆韧带切迹,经镰状韧带游离缘的两层腹膜间达脐静脉窝止于门静脉左支的囊部并与静脉韧带相连,是脐静脉闭锁所形成的纤维索带。
(3)冠状韧带系肝膈面与脏面被膜返折至膈所形成,有左、右冠状韧带。左冠状韧带分前、后两层,右冠状韧带分上、下两层。两层之间为肝裸区。
(4)三角韧带之左三角韧带有较大血管和迷走胆管,手术切断后要妥善处理。
(5)肝胃韧带中有时胃左动脉发出的副肝左动脉经此韧带入肝,供血给左外叶或左半肝。
(6)肝十二指肠韧带左缘与肝胃韧带相连,右缘游离,后方有胃网膜孔,其内有肝固有动脉、门静脉主干、胆总管、神经和淋巴管,称为肝蒂。手术时可在此处阻断入肝的血流。
(7)肝肾韧带由右冠状韧带下层绕过右肝的脏面和右肾前面而形成,其内有右肾上腺静脉。
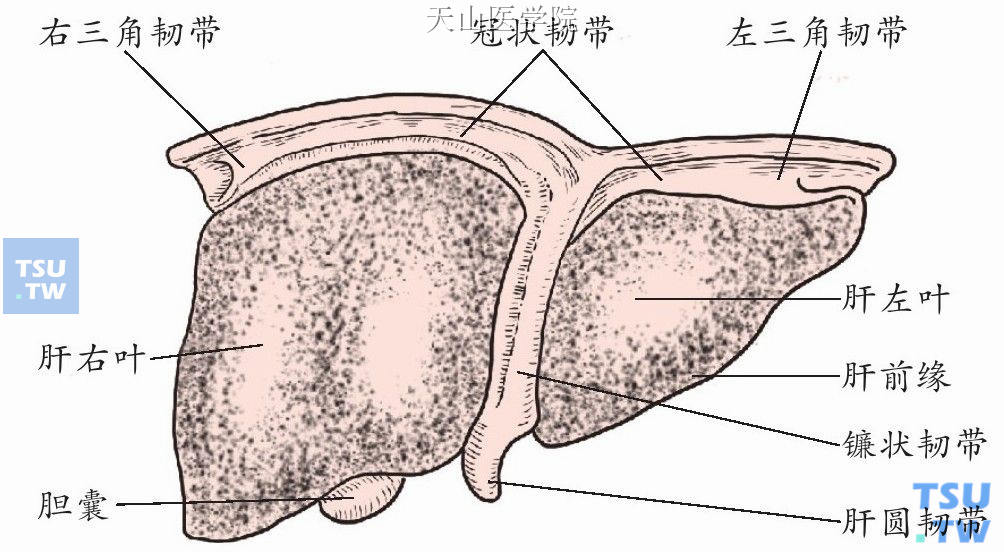
图9-1-1 (1)肝脏韧带(膈面)
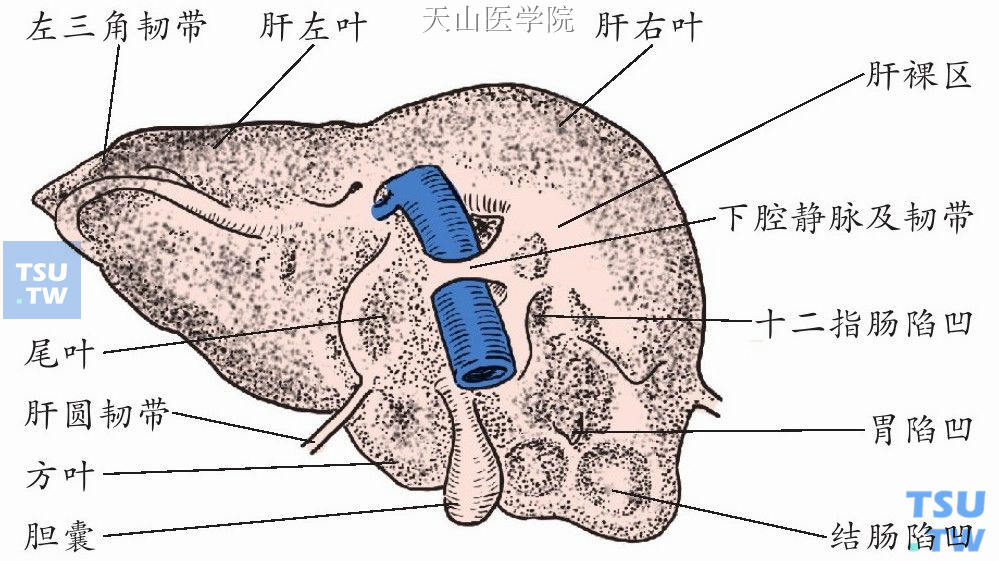
图9-1-1 (2)肝脏韧带(脏面)
肝脏分叶分段
肝脏主要有三个主裂、两个段间裂和一个背裂。
(1)正中裂起自胆囊窝的中部,向后上方斜行抵于下腔静脉的左缘。此平面内有肝中静脉经过。
(2)左叶间裂从肝前缘的脐切迹向后上方抵于肝左静脉注入下腔静脉处,在膈面约在镰状韧带之左侧。左叶间裂将左半肝分为左外叶和左内叶。此平面上有肝左静脉的叶间支经过。
(3)右叶间裂在正中裂的右侧约距肝右缘l/3处,斜向右前方再弯向肝的右下缘。它将右半肝分为右前叶与右后叶,有肝右静脉从其平面上经过,故在肝右前、后叶切除时,沿肝右静脉分离就是右叶间裂的部位。
(4)左外叶段间裂起于肝左静脉回流入下腔静脉处,然后以斜行方向越过左外叶止于肝左缘的后中1/3处,将左外叶分成外上段和外下段,在此裂平面中有肝左静脉的段间支经过。
(5)右外叶段间裂在肝的脏面起于肝门的右切迹,横过右后叶止于右外侧缘之中点附近,将右后叶分成上段与下段,因此右切迹(即横沟)可作为右后叶段间裂在肝表面之标志。
(6)背裂位于肝脏后上缘中部,尾状叶前方,是第二肝门所在。在肝脏上极形成一弧线,将尾状叶隔开。
肝脏按上所述肝裂分成五叶四段,即左外叶、左内叶、右前叶、右后叶和尾状叶,左外叶和右后叶又各分为上下两段。这对于肝脏疾病的定位诊断和开展肝叶切除术有重要意义。
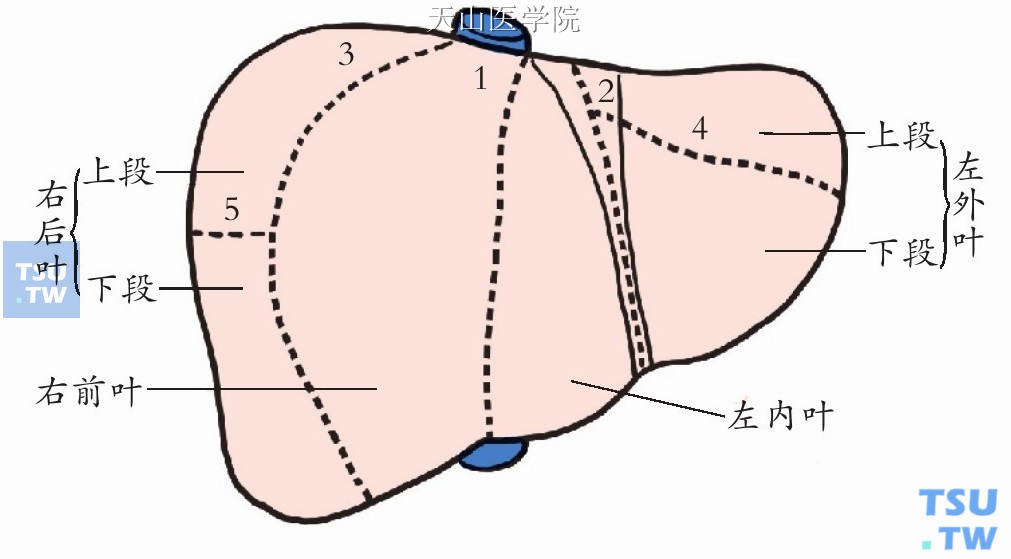
图9-1-2(1) 肝脏分叶分段(膈面)
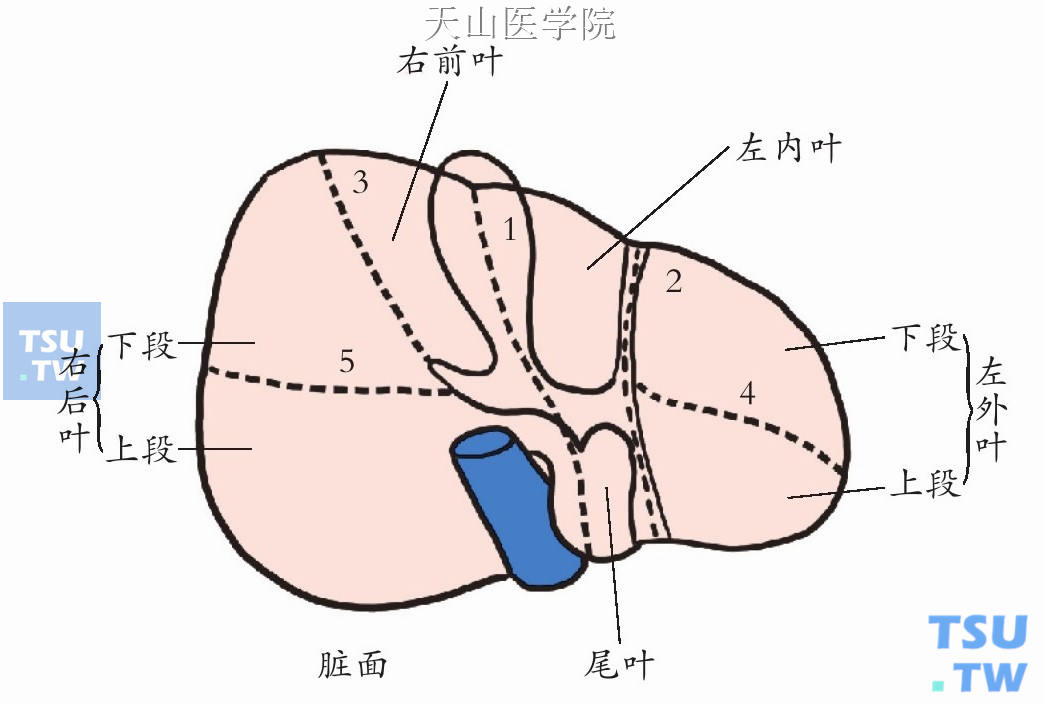
图9-1-2(2) 肝脏分叶分段(脏面)
Couinaud以肝裂、门静脉和肝静脉为基础,提出肝脏的功能性分段,将肝脏分为8段(图9-1-3)。尾状叶为Ⅰ段,左外叶为Ⅱ段和Ⅲ段,左内叶为Ⅳ段,右前叶为Ⅴ、Ⅷ段,右后叶为Ⅵ、Ⅶ段。1989年Couinaud将尾状叶分左、右两段,左侧为Ⅰ段,右侧为Ⅸ段。第一级划分称肝中界面,将肝分为左、右半肝,肝中界面以胆囊窝和下腔静脉窝为界,肝中静脉位于其中。第二级划分称区界面,右区界面以肝右静脉为界而将右半肝分为右前区和右后区,左区界面以镰状韧带为界将左半肝分为左内区和左外区。第三级划分称段界面,即各段之间的界面。
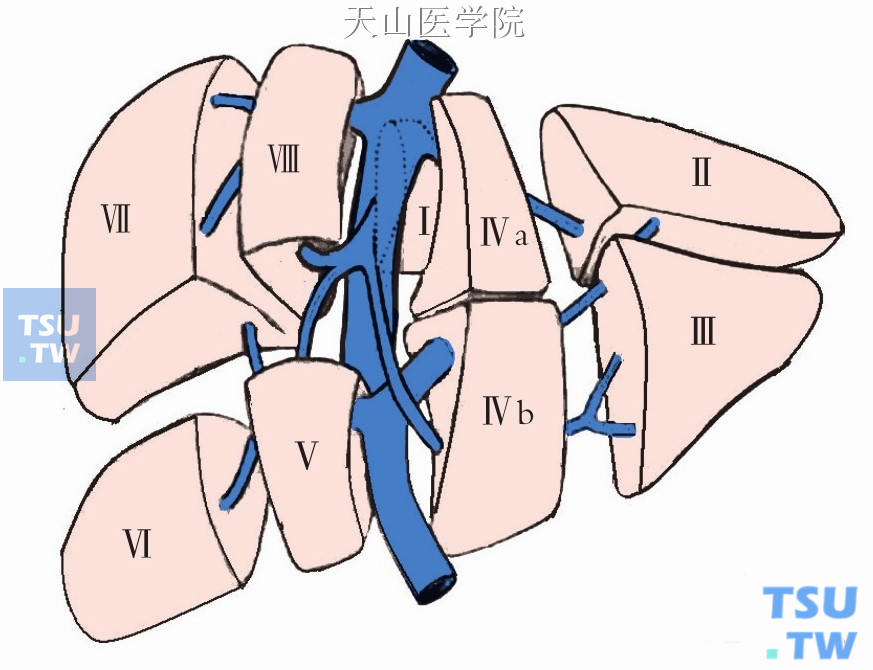
图9-1-3 肝脏Couinaud分段
肝门解剖
(1)第一肝门在肝的脏面,有H形的沟,其中部呈横行的沟,称为肝门(porta hepatis)。其内有肝管、门静脉、肝固有动脉左右支、淋巴管及神经出入。肝管位于右前方,左前方为肝动脉,门静脉位于两者后方(图9-1-4)。
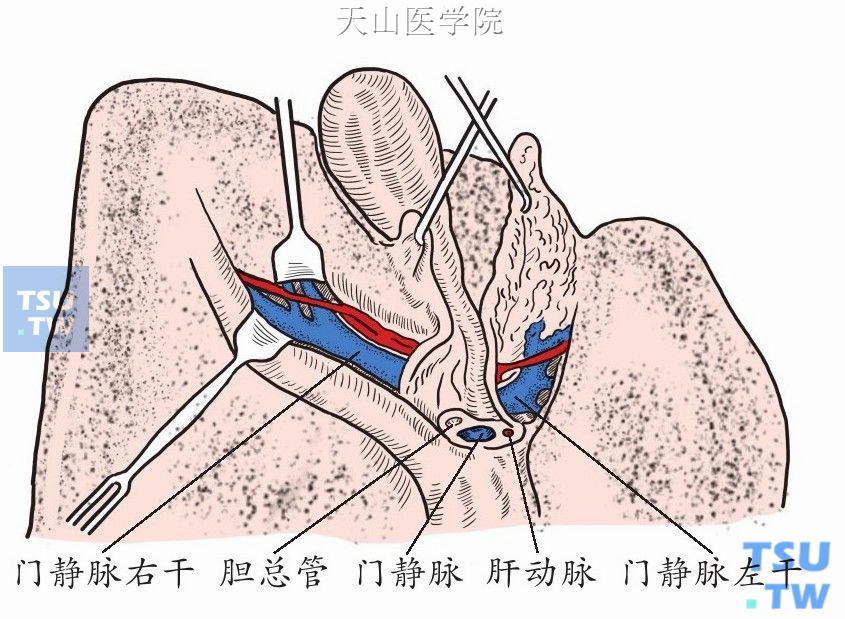
图9-1-4 第一肝门解剖
(2)肝静脉离肝汇入下腔静脉区域为第二肝门。其肝外标记是沿镰状韧带向下后方的延长线,此线正对肝左、中静脉共干后入下腔静脉处。三支主要的肝静脉均在下腔静脉窝汇入下腔静脉(图9-1-5)。
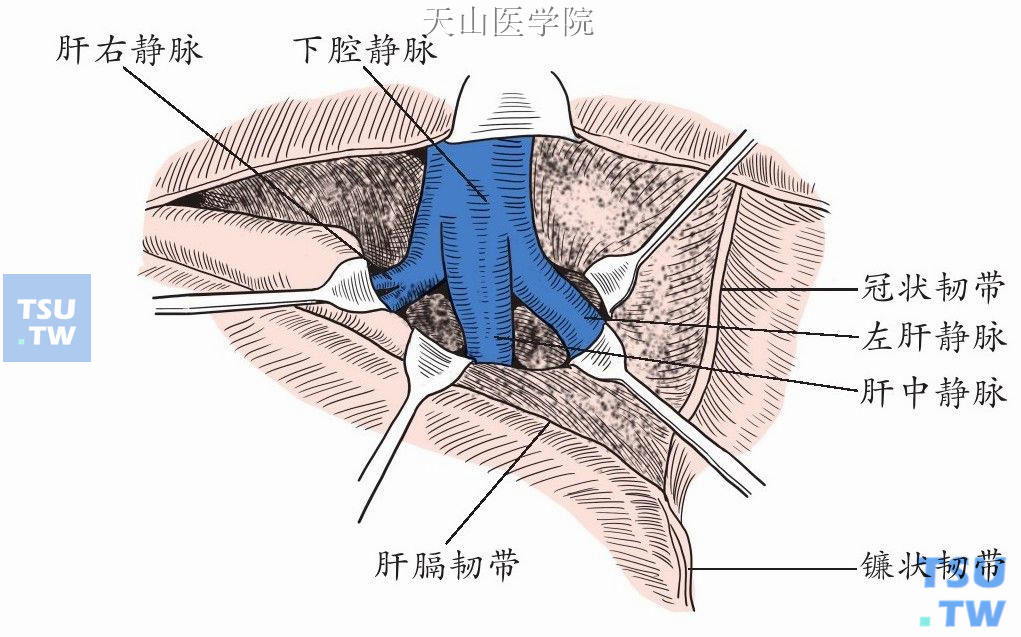
图9-1-5 第二肝门解剖
(3)直接汇入下腔静脉的小肝静脉,称为肝短静脉,在肝切除时如处理不当可引起大出血,故称为第三肝门。
术前
手术指征
1.病人一般情况良好,ECOG评分0~2分,无明显心、肺、肾等重要脏器功能障碍。
2.肝功能正常或仅有轻度损害,肝功能Child-Pugh分级属A级;或肝功能分级属B级,经短期护肝治疗后有明显改善,肝功能恢复到A级。
3.肝储备功能属正常范围。
4.肿瘤位于肝脏边缘;或肿瘤较小,位于距肝脏边缘较远的肝实质内。
禁忌证
1.恶性肿瘤已有肝外远处转移。
2.癌瘤多发,数目多于3个或肝内播散,或病变已超过半肝范围累及肝门。
3.肝癌并有严重肝硬化,术前肝功能不佳。
4.患者一般情况不佳,或心、肺、肝、肾有明显功能障碍。
术前准备
1.患者肝功能及肝储备功能的评估。
2.全身状况(包括心、肺、肾)的评估和慢性疾病的纠正及治疗。
3.影像学资料肿瘤的可切除性评估。
4.术前晚进流质,口服泻药肠道准备,术日晨禁食;术前置胃管、导尿管,目前提倡麻醉后施行;切皮前半小时预防性使用抗生素。
5.术前肝功能欠佳者,予以保肝支持治疗(白蛋白、支链氨基酸、维生素C和维生素K1等)。
麻醉
连续硬膜外麻醉及气管内插管联合麻醉。
体位
肝左叶和尾状叶肿瘤可采用平卧位,若肿瘤位于右尾状叶也可取右侧抬高60°~90°体位;右前叶肿瘤可取右侧抬高30°体位;右后叶肿瘤取右侧抬高45°~60°体位;对部分裸区或近下腔静脉的右后叶肿瘤可采用右侧抬高90°体位。
手术步骤
1.楔形切除
(1)根据肿瘤位置选择不同体位,肝右叶肿瘤一般右侧抬高30°(图9-1-6)或45°(图9-1-7),一般取右肋缘下1~2横指斜行切口,必要时可向左侧延长;左叶肿瘤也可取左肋缘下切口(图9-1-8)。
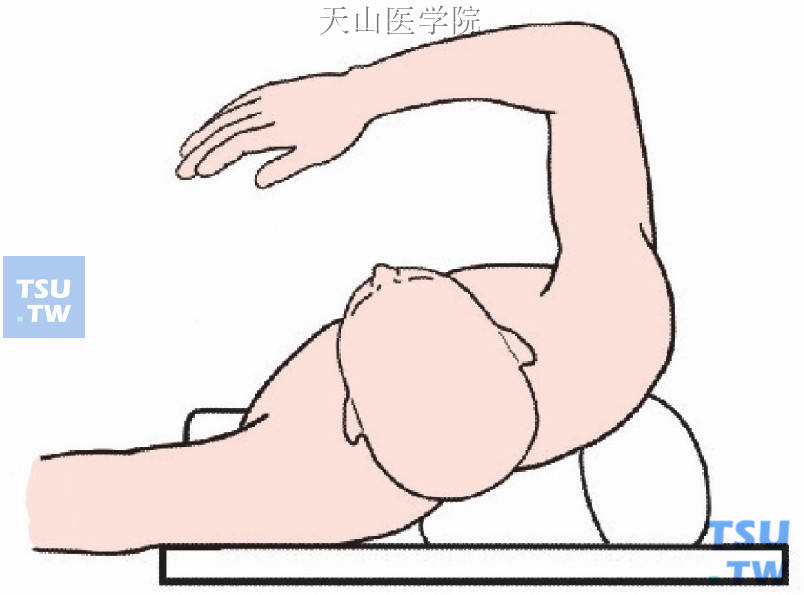
图9-1-6 右侧抬高30°
图9-1-7 右侧抬高45°
图9-1-8
(2)进腹后探查腹腔内脏器及肿瘤情况,根据肿瘤位置不同,选择性游离肝脏韧带,以充分显露肿瘤为原则。以肝右叶肿瘤为例,肿瘤位于肝右叶边缘,距肿瘤边缘2~3cm处大针粗线交锁缝扎止血[图9-1-9(1)、(2)]。
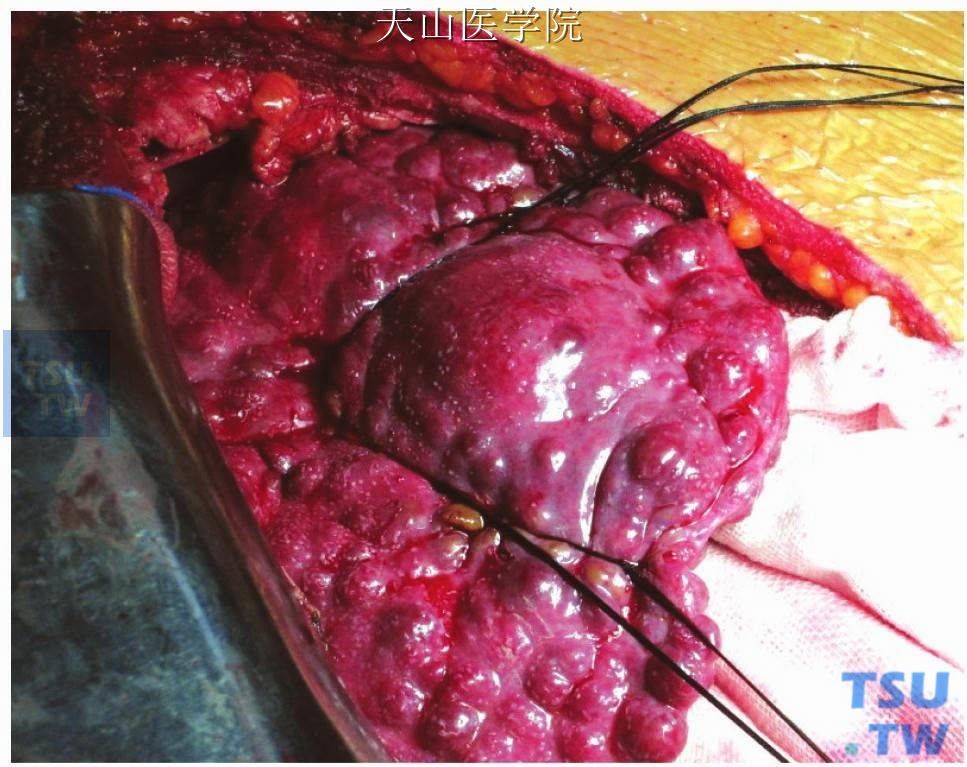
图9-1-9 (1)肿瘤边缘交锁缝扎
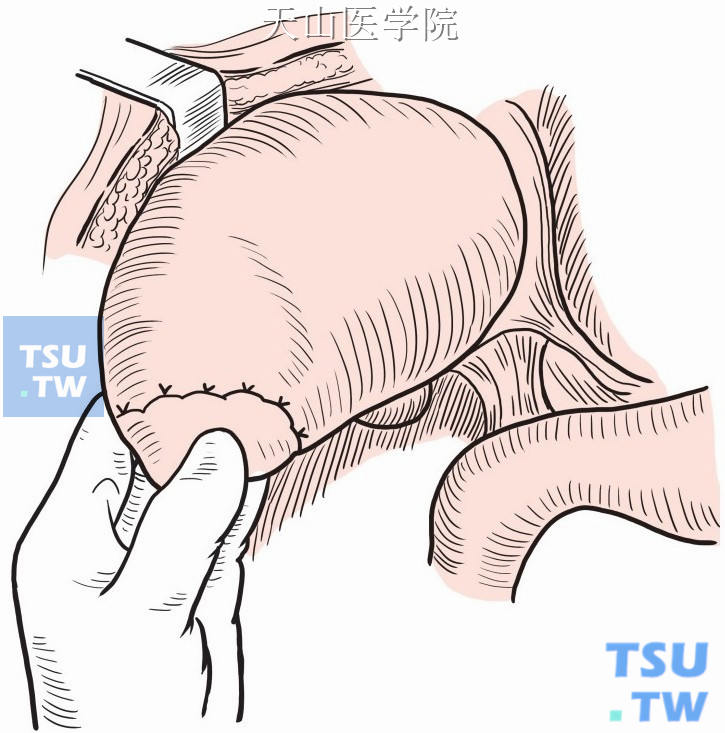
图9-1-9 (2)示意图
根据术中情况,可以阻断[图9-1-10(1)、(2)]或不阻断第一肝门。
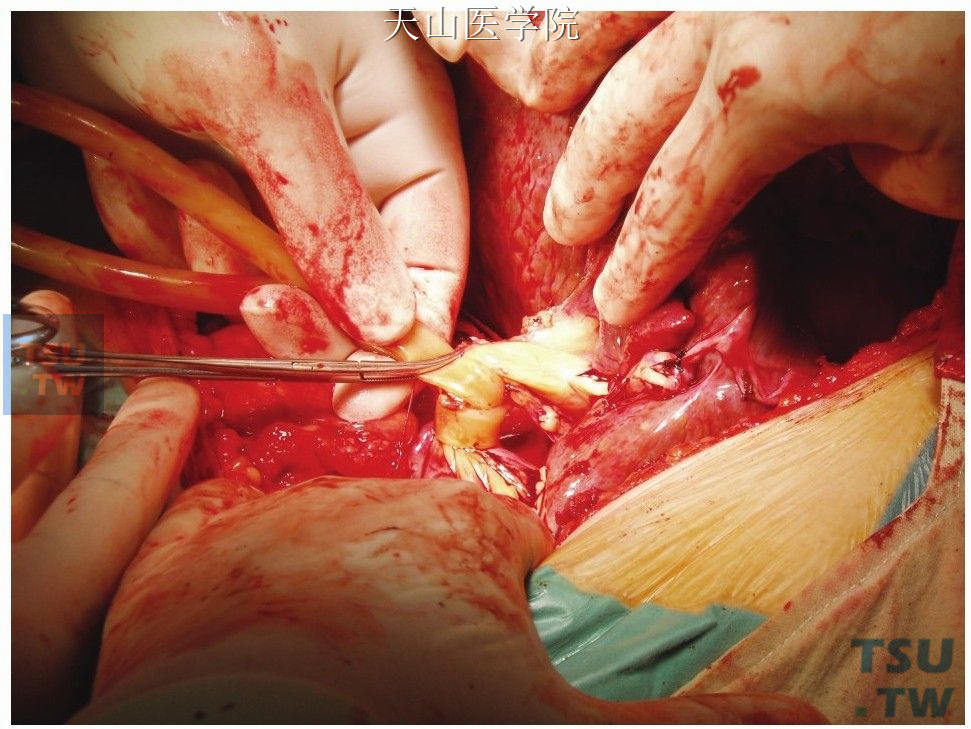
图9-1-10 (1)阻断第一肝门
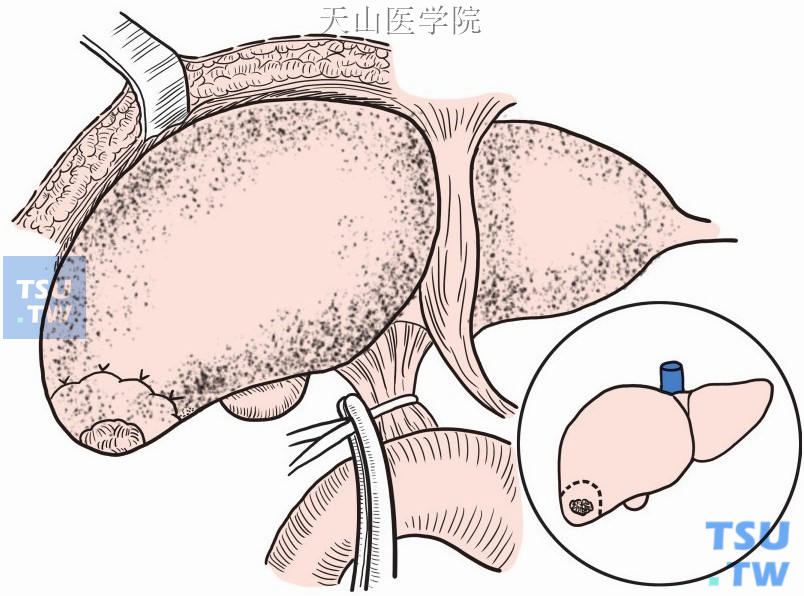
图9-1-10 (2)示意图
(3)距肿瘤边缘2cm以上电刀切开肝包膜和浅表肝组织(图9-1-11)。
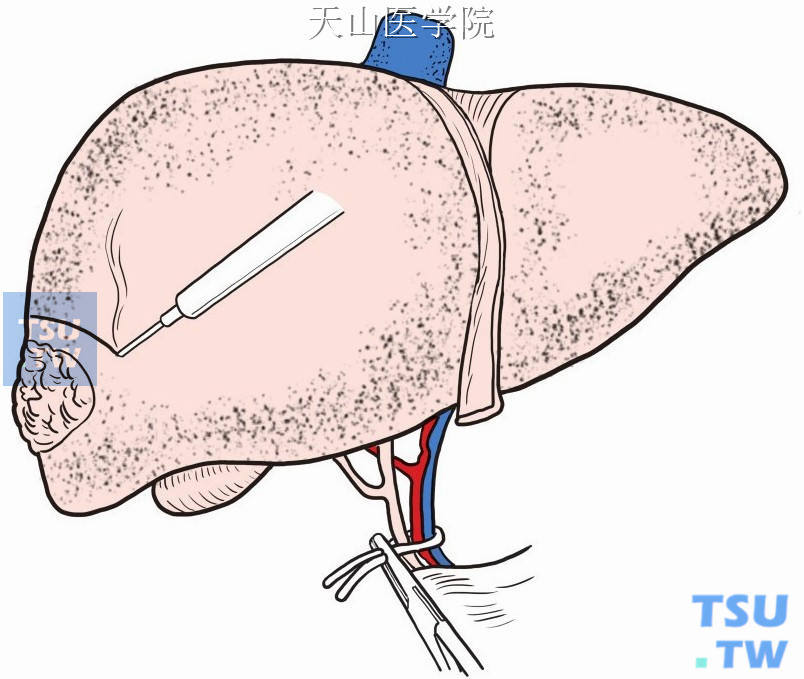
图9-1-11 电刀切开肝包膜和浅表肝组织
(4)血管钳钳夹分离肝组织,切断各管道后完整切除肿瘤,仔细结扎管道残端,大的管道缝扎(图9-1-12)。
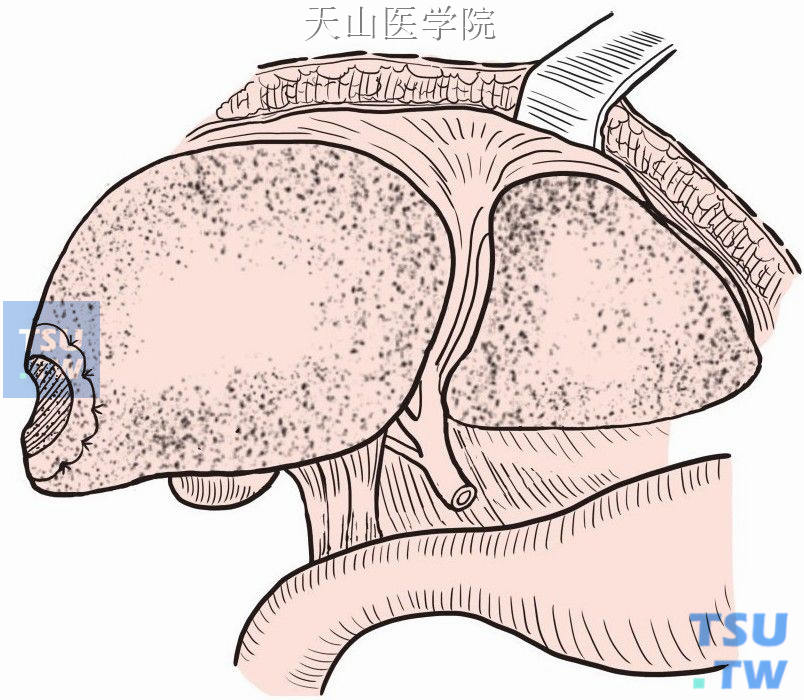
图9-1-12 切除肿瘤,结扎缝扎管道残端
(5)松开肝门阻断带,缝扎肝断面的出血点和胆漏管道,一般多行“8”字缝扎(图9-1-13)。
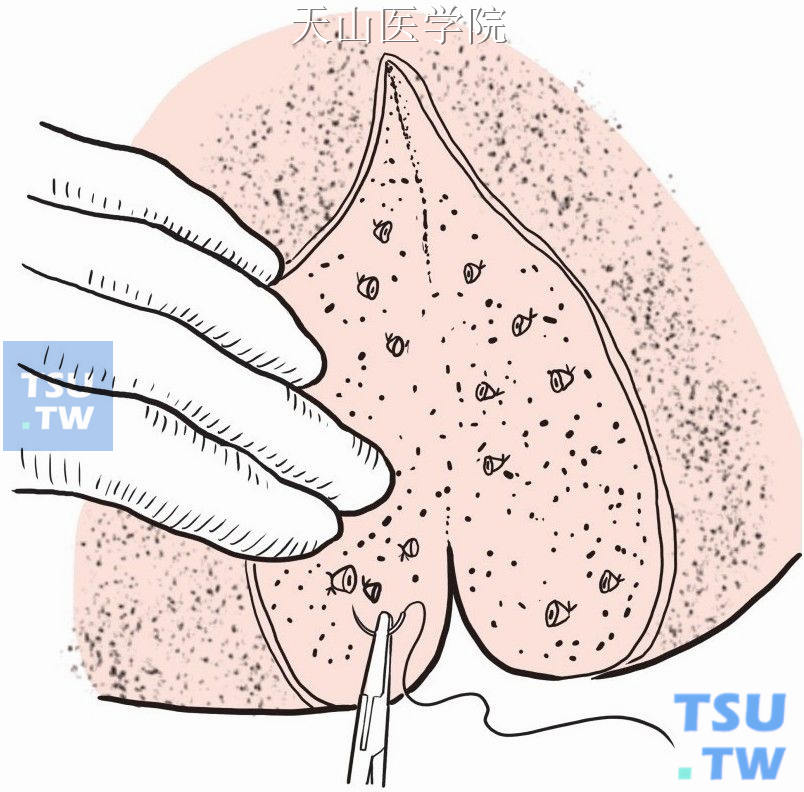
图9-1-13 缝扎肝断面出血点和胆管
(6)根据精准肝切除术的原则,目前大多数的肝切除,肝断面经仔细处理后,无明显出血和胆漏,可不予对拢缝合,创面喷涂生物蛋白胶和(或)覆盖止血海绵等材料。对于部分肝脏边缘的局部切除,根据术者的习惯,创面仍可用肝缝线和粗丝线对拢缝合(图9-1-14)。
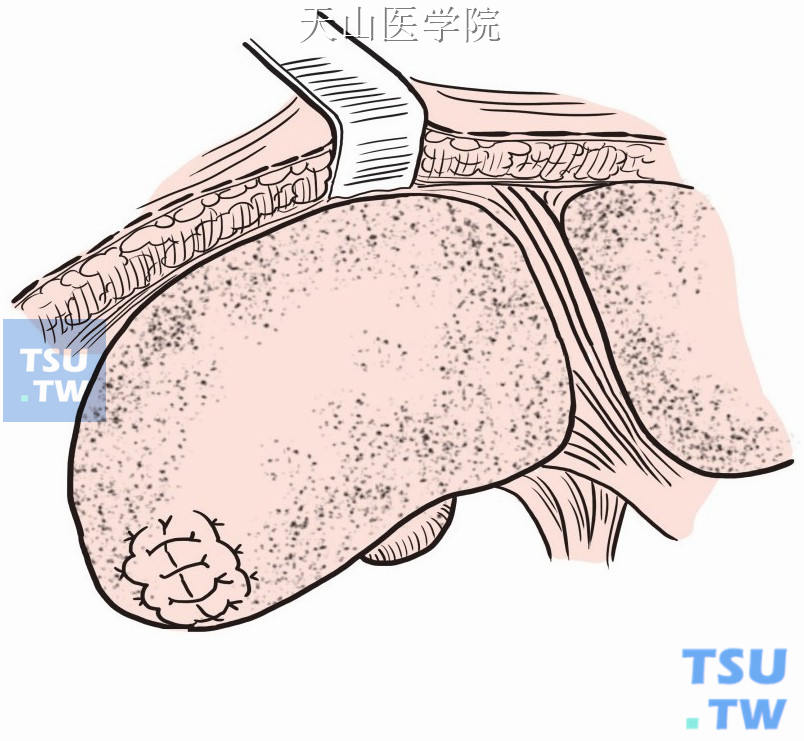
图9-1-14 创面对拢缝合
(7)生理盐水冲洗手术野,右膈下或手术区置乳胶管引流(图9-1-15)。
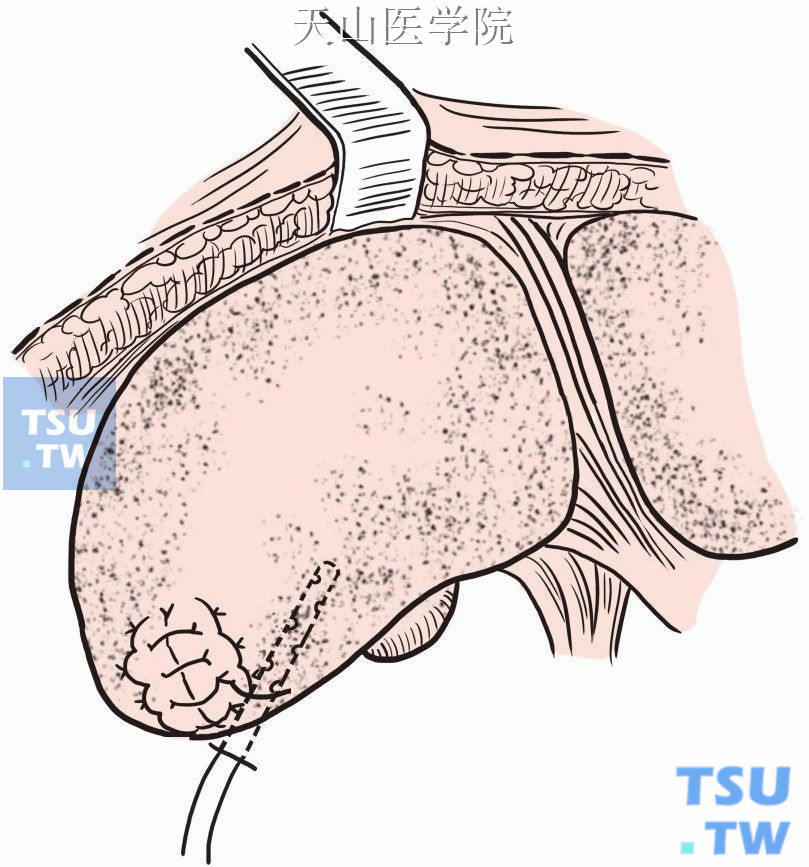
图9-1-15 乳胶管引流
2.梭形切除
(1)进腹后探查腹腔内脏器及肿瘤情况,肿瘤位于远离肝边缘的实质内,根据肿瘤位置不同,选择性游离肝脏韧带,以充分显露肿瘤为原则。以肝右叶肿瘤为例,韧带游离完后,设计唇形切口(图9-1-16)。
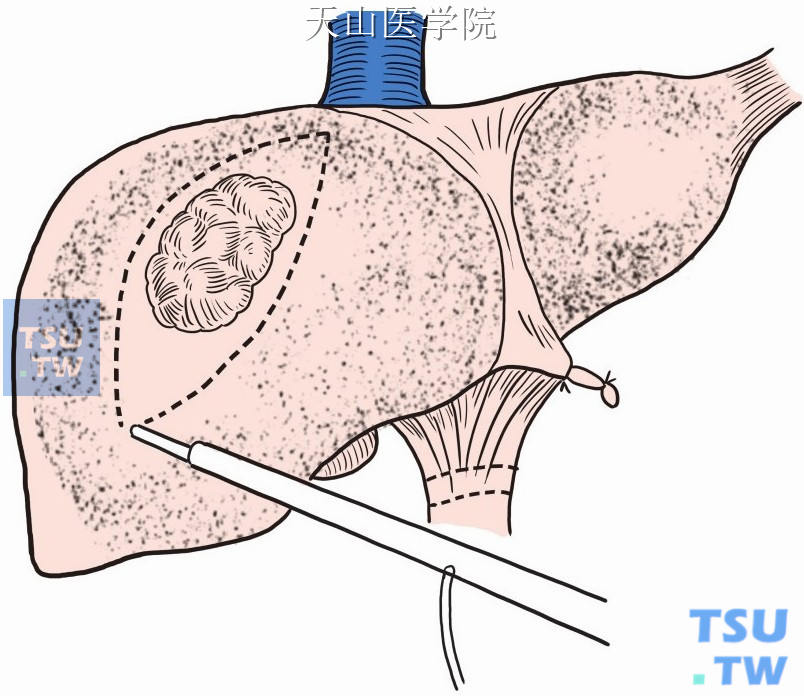
图9-1-16 标记预定切口
(2)距肿瘤旁2~3cm处大针粗线交锁缝扎止血(图9-1-17)。
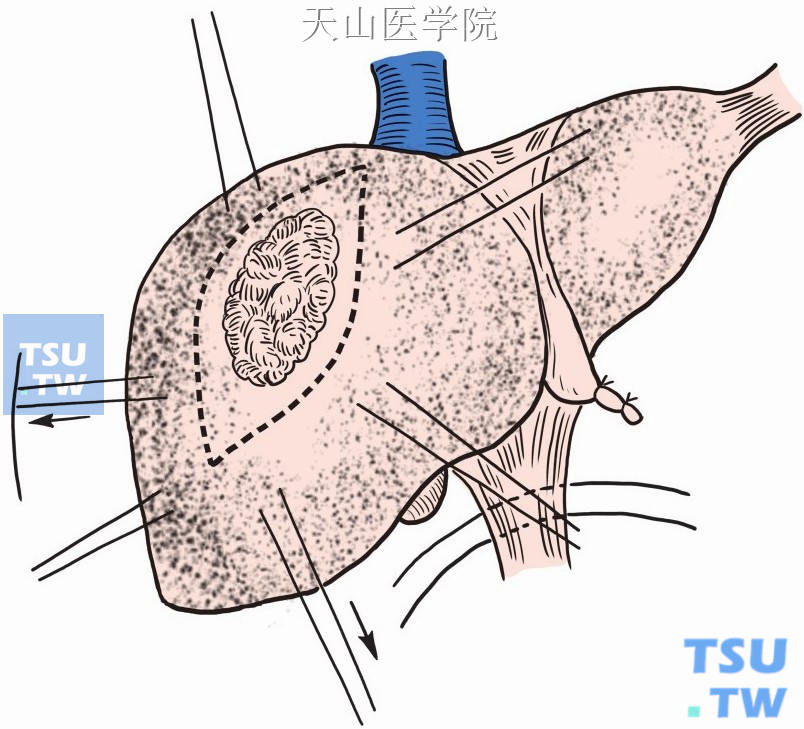
图9-1-17 肿瘤边缘缝扎止血
根据术中情况,阻断或不阻断第一肝门(图9-1-18)。
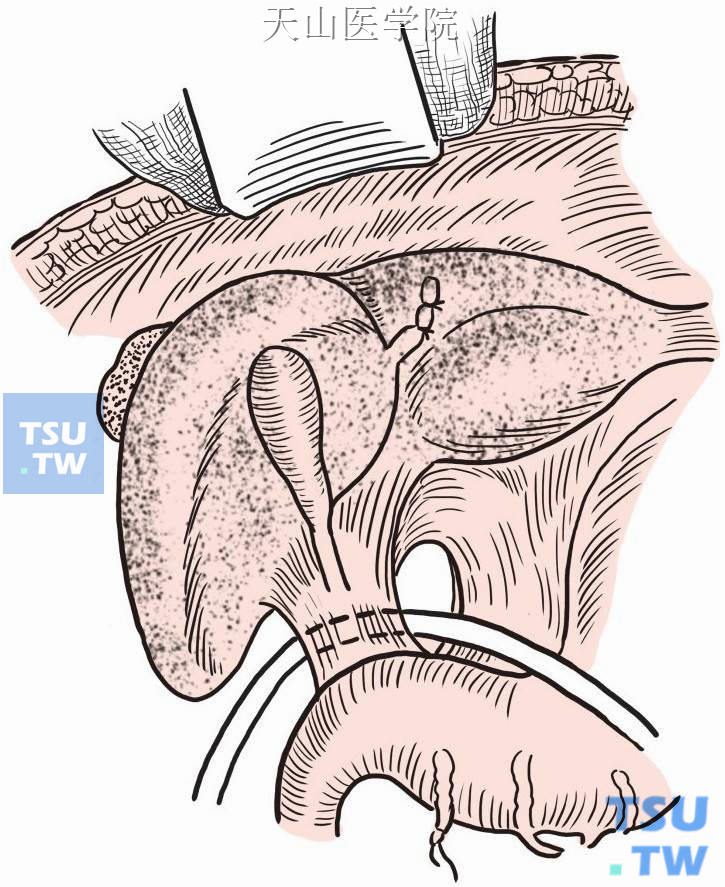
图9-1-18 第一肝门置阻断带
(3)距肿瘤旁2cm电刀棱形切开肝包膜和浅表肝组织(图9-1-19)。
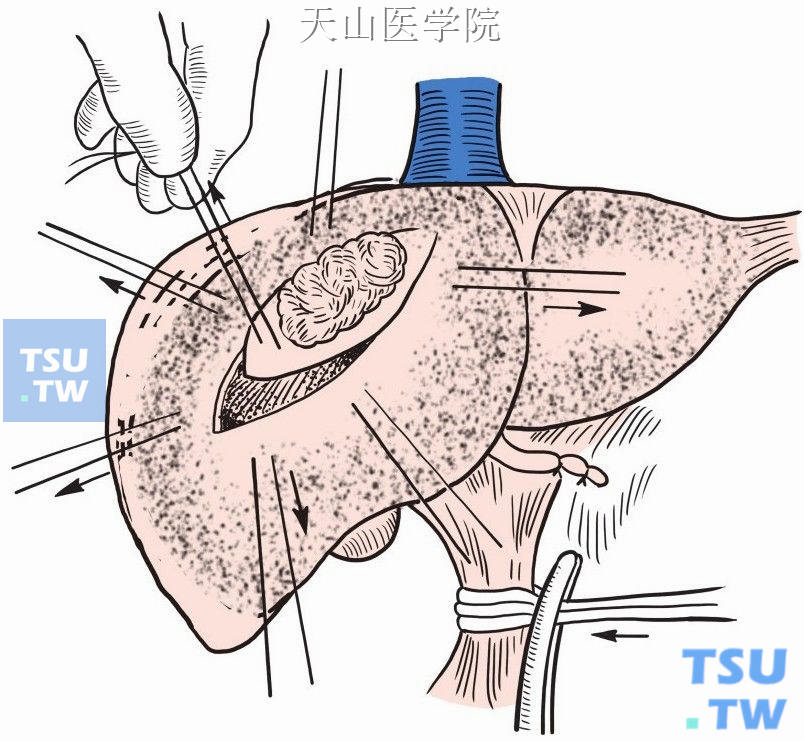
图9-1-19 切开肝包膜和浅表肝组织
(4)血管钳钳夹分离肝组织,切断各管道后完整切除肿瘤,结扎管道残端,大的管道缝扎(图9-1-20)。
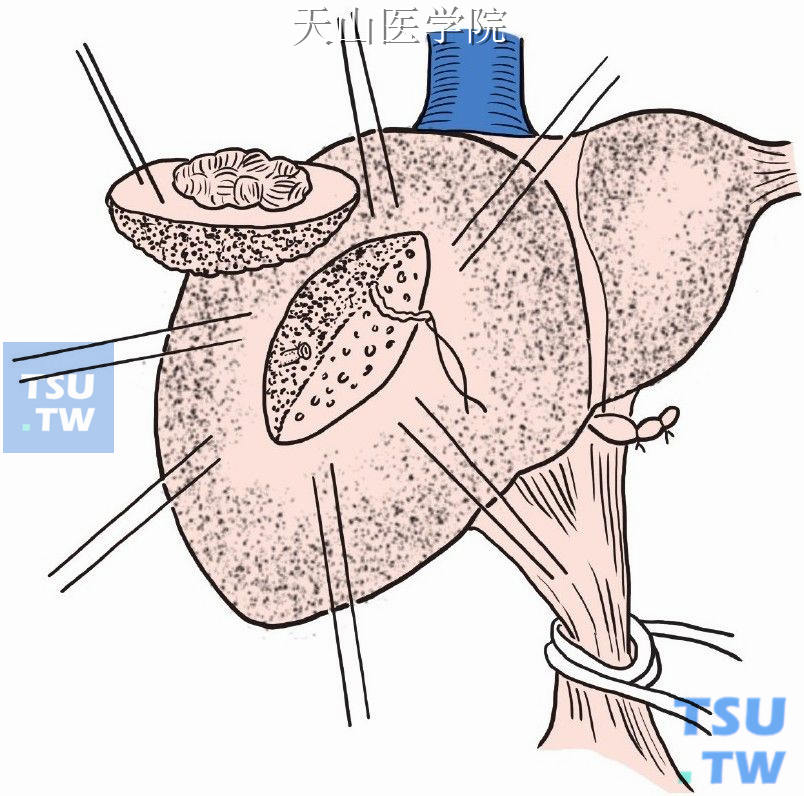
图9-1-20 切除肿瘤,管道结扎缝扎
(5)松开肝门阻断带,仔细缝扎肝断面出血点和胆漏管道(图9-1-21)。
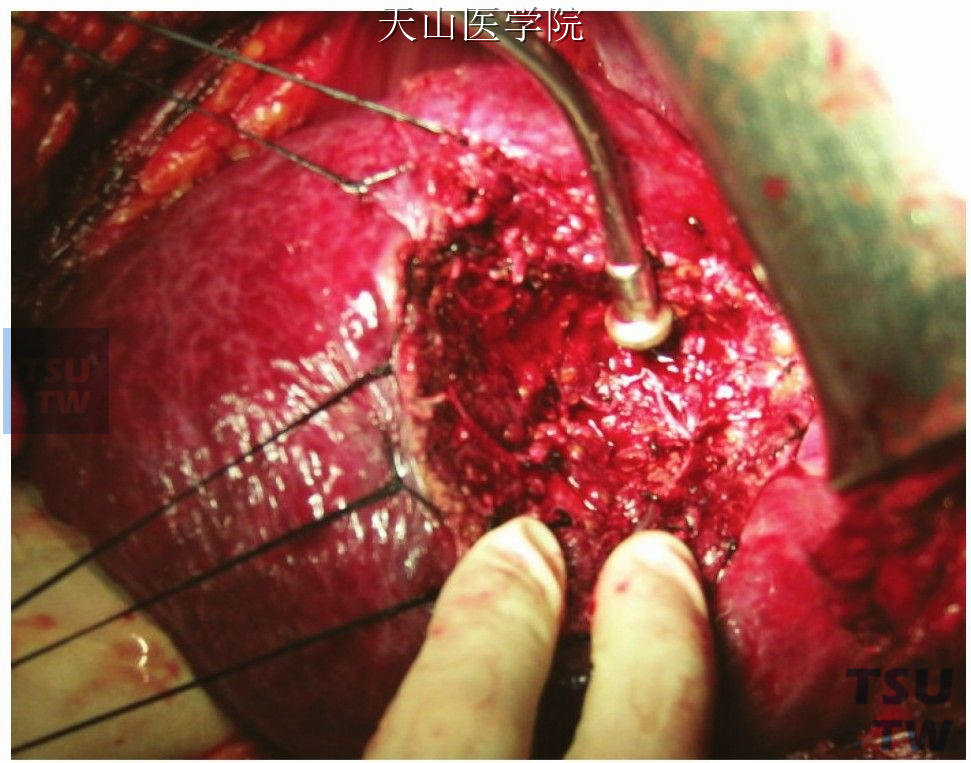
图9-1-21 缝扎肝断面出血点和胆漏管道
(6)肝断面目前一般不对拢缝合,经彻底止血和检查无胆漏后,用生物蛋白胶喷涂,止血海绵或其他止血材料覆盖创面。若不影响重要出入肝血流,根据术者习惯,有些肝断面可对拢缝合(图9-1-22)。
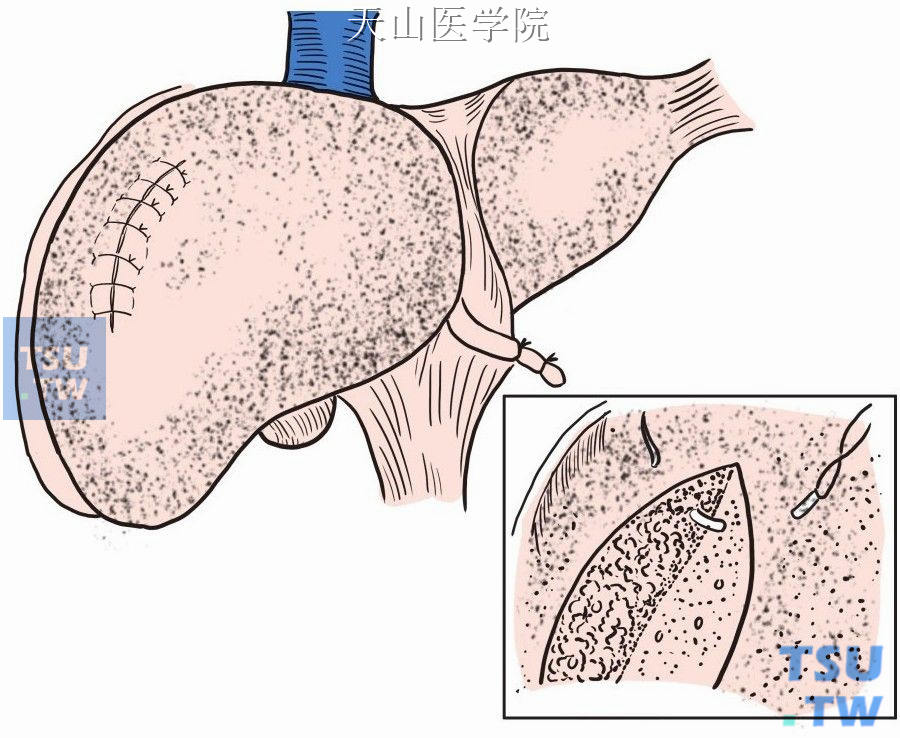
图9-1-22 创面对拢缝合
(7)生理盐水冲洗手术野,右膈下或手术区置乳胶管引流(图9-1-23)。
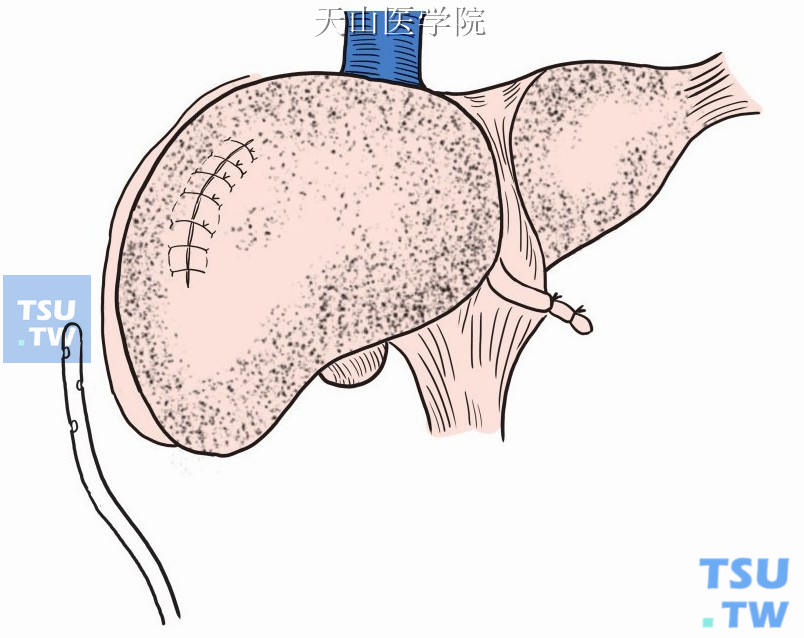
图9-1-23 手术区置乳胶管引流
手术意外的处理
1.肿瘤位于肝脏深部肝实质深部的小肝癌,单手扪摸有时不易发现,可取用双手合诊法,扪摸时应将肝脏各个部分都检查到,特别注意扪摸靠膈顶处的边缘部位、右肝裸区、肝后侧和尾状叶等较隐蔽部位。无法通过触诊扪及的肿块,术中可使用B超进行定位,术者如仍不能确认时,术中请超声科经验丰富医生协同进行检查和确认。
2.肝断面大出血为避免手术过程中可能出现较大的出血,可选用肝门阻断技术。第一肝门阻断一般用乳胶管环绕肝十二指肠韧带扎紧两圈,对无肝硬化患者单次阻断时间可达20分钟或更长,对有肝硬化的患者,一般单次阻断时间不超过10~15分钟。间歇性阻断可减少肝脏持续缺血时间,使本应较长的阻断时间分次进行,减轻肝脏损伤,但是在间歇开放期间肝脏断面失血较多,手术野不清晰,并且使手术时间延长,一般两次阻断间隔时间为5分钟。肝脏的局部切除一般很少用选择性肝血流阻断和全肝血流阻断。对于肝脏血流阻断方法的选择,应根据术前影像学检查结果和患者肝功能Child分级,术中探查肝硬化程度和肿瘤的大小、位置、边界、与周围血管的关系、肝脏切除的范围,甚至还要根据术者的经验和习惯等情况综合考虑。
肝断面的处理大致有血管钳钳夹压榨法、超声切割止血刀、CUSA、水刀、微波等。近年来出现的新型止血材料包括各种生物蛋白胶和止血海绵等,这些新器械和新材料的应用,大大减少了肝脏外科手术中的出血,提高了手术的安全性,降低了术后并发症。
3.邻近脏器侵犯肝癌侵犯膈肌或邻近其他脏器比较常见,特别是侵犯膈肌,有些并不一定侵犯,只是紧密粘连,术中的分离可致膈肌破裂,发现膈肌破裂后应及时修补,一般不需安置胸管引流。肿瘤侵犯膈肌时须直接切除部分膈肌,但范围不能过大,要保证膈肌能够缝合完整,膈肌修补后,术后应密切观察患者的呼吸,有些患者术后可出现较多的胸水。肝癌侵犯后腹膜的肾上腺和肾包膜时,可以一并切除,但是要注意妥善处理肾上腺血管,切不可损伤肾静脉。当肿瘤侵犯结肠和十二指肠时,可局部切除,然后再行结肠或十二指肠修补,必须按胃肠外科的原则进行处理,严密观察腹腔引流和腹部体征,胃管放置时间适当延长,进食时间推迟,术后应多补充白蛋白,防止肠漏。
术后处理
1.术毕平卧6小时,禁食、吸氧,必要时心电监护,胃管可视胃肠引流量适当提前去除,但须待术后3~4天肛门排气后才可进流质。
2.记出入量,包括膈下引流量、补液量、尿量等。特别注意观察引流的颜色和量。
3.定期监测肝功能、肾功能、血糖、血常规,对利尿治疗者须密切随访血电解质。
4.常规保肝治疗、小剂量制酸药物预防应激性溃疡,对肝硬化严重、凝血功能较差者宜早期输血浆和补充凝血因子。
5.适当补充白蛋白;手术当日常规予2500~3000ml静脉补液,术后第一天起予3000ml左右静脉补液,视出入量予以调整,进食后酌减,合并肝硬化严重者应适当控制补液量,以免产生大量腹水。
6.明显腹水者予利尿治疗。
7.一般不予预防性抗感染,除非出现明显感染才采用抗生素,但对于年龄较大,有糖尿病、呼吸道疾病患者应使用抗生素。
8.其余视临床情况对症处理。
临床经验
1.关于手术适应证肝癌能否切除,除了根据肿瘤病变本身的情况外,还需根据肝硬化程度及病人对手术的耐受程度进行判断。因此术者一定要严格把握手术指征,对每一个病例,做到心中有数。对肝功能欠佳的病人,予以支持保肝,切不可勉强手术,否则将导致术后肝功能衰竭的严重后果。
2.关于肝实质深部的小肝癌和术中出血的控制处理原则见“手术意外的处理”。
3.关于手术切缘问题有人认为,切缘距离肿瘤越远则手术越彻底,但实际操作时,还需要视肿瘤部位、大小及肝硬化程度而定。肿瘤切除范围增加了,手术彻底性一定程度上可以得到提高,但安全性则相对下降,有时甚至由于盲目扩大手术范围而损伤一些不应伤及的血管和胆管,这是不足取的。目前国际上尚无切缘距肝肿瘤多少厘米为根治性切除界限的标准,我们一般认为切缘距肿瘤大于1~2cm即可。对于肝门部的中央型肝癌,应紧贴肿瘤切除,以免引起大的管道损伤而致严重后果。
4.关于肝断面的处理问题良好的肝断面处理不但可有效控制术中出血量,还能显著降低术后渗血、胆漏及感染等并发症的发生率。肝断面的处理首先要妥善结扎或缝扎细小的血管,反复检查和消灭断面的出血和胆漏。按照精准肝切除的原则,应尽可能地保留残留肝脏的功能和活性,因此,目前多不主张应用“U”形交锁缝合和对拢缝合法处理肝断面,以免出现断端缺血、坏死、继发感染及流出流入道梗阻的情况。彻底止血、消灭胆漏和敞开肝断面是肝切除术的趋势,但是,对于一些肝脏周边的肿瘤,肝断面的对拢可以节省手术时间,减少出血和胆漏,仍不失是一种可选择的方法。
5.关于术后处理肝脏手术是腹部外科的大手术,而患者大多合并乙肝肝硬化,手术对患者的内环境和肝肾功能都是大的打击,因此,术后要密切观察生命体征,特别是观察引流、尿量和肝功能情况,做到早发现问题早处理,防患于未然。
