1860年von Hebre首先报道本病,称渗出性多形红斑(erythema multiforme exudativum),即现在的多形红斑轻症型(erythema multiforme minor),或称合并单纯疱疹多形红斑(herpes simplex-associated erythema multiforme,HAEM)。1922年Stevens-Johnson报道了重症型病例,称Stevens-Johnson综合征(Stevens-Johnson syndrome,SJS)。1965年Lyell描述了另一型重症型多形红斑,称中毒性表皮坏死松解症(toxic epidermal necrolysis,TEN),又称莱尔综合征(Lyell syndrome)。以上3型在临床和组织学上反映了疾病不同的严重程度,可以看作一个疾病从轻到重的病谱分布。但近年来认为3者不仅临床表现有区别,而且病因上亦存在差异,Hebre型病因与单纯疱疹病毒感染有关,SJS病因主要为药物过敏,其次为感染,TEN绝大多数为药物过敏。目前多数主张应分别作为单独疾病。本章将SJS与TEN从多形红斑中分出。
多形红斑为急性炎症性皮肤病,有自限性,皮疹多形,有红斑、丘疹、风团、水疱等,特征性皮疹为靶形损害即虹膜状皮疹,有不同程度黏膜损害,少数有内脏损害。本病春秋季节好发,男性略多于女性,以10~30岁发病率最高,20%为青少年,发病率尚无精确统计,据美国皮肤科门诊调查年发病率为1%。
预后:轻症型病程2~3周自愈,无后遗症,重症型者病程3~6周,可发生眼部后遗症,死亡率<5%。
病因及发病机制
病因不明。可能对多种抗原物质发生的免疫反应,轻症型病例与单纯疱疹病毒(HSV)感染有关,即合并单纯疱疹多形红斑,推测其发病机制为细胞介导的免疫反应。单纯疱疹患者周围血中的巨噬细胞或组织内朗格汉斯(Langerhans)细胞摄取HSV后进行处理,形成HSVDNA片段,输送至远隔部位,沉积于皮肤组织内,引起HSV特异性CD4+细胞增殖,并聚集于该处,产生干扰素γ,并引起炎症级联反应,释放多种细胞因子,产生皮肤炎症反应,其表皮内CD4+细胞可引起角质形成细胞凋亡。在多形红斑发病机制中,还存在着多种免疫现象,包括由免疫复合物介导的免疫反应等。
多形红斑发病的病因和有关因素报道很多,现将主要因素分列如下:
感染
- 细菌:溶血性链球菌、葡萄球菌、沙门菌、白喉杆菌、变形杆菌、麻风杆菌、结核杆菌、铜绿假单胞菌、军团菌、土拉菌(tularemia)、耶尔森菌(Yersinia species)、脑膜炎球菌、肺炎球菌。
- 立克次体感染:丛林斑疹伤寒(scrub typhus)。
- 支原体:支原体肺炎。
- 螺旋体:包柔疏螺旋体病(borreliosis)、梅毒。
- 衣原体:沙眼衣原体、鹦鹉热衣原体。
- 病毒:腺病毒、科萨奇病毒B5、巨细胞病毒、埃可病毒(echovirus)、肠道病毒、Epstein-Barr病毒,肝炎病毒(甲型、乙型、丙型)、单纯疱疹、流行性感冒、麻疹、流行性腮腺炎、副牛痘、脊髓灰质炎、牛痘、水痘-带状疱疹、天花病毒。
- 真菌:球孢子菌、皮肤癣菌、组织胞质菌。
- 寄生虫:毛滴虫、弓形虫。
药物
- 抗生素:青霉素、氨苄西林、四环素、阿莫西林、头孢噻污、头孢克洛、头孢氨苄、环丙沙星、红霉素、米诺环素、磺胺类药、甲氧苄啶-磺胺甲
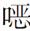 唑、万古霉素。
唑、万古霉素。 - 抗惊厥药:巴比妥、卡马西平、乙内酰脲(hydantoin)、苯妥英、巴戊酸(valproic acid)。
- 退热镇痛药:阿司匹林。
- 抗结核药:利福平、异烟肼、氨硫脲、吡嗪酰胺。
- 抗真菌药:灰黄霉素、制霉菌素、特比萘芬、氟康唑。
- 其他:喹碘仿、西咪替丁、氯贝特(clofibrate)、糖皮质激素、砷、双氯芬酸钠(diclofenac)、二磷酸盐或酯、雌激素、阿维A酯、粒细胞-巨噬细胞集落刺激因子、肼屈嗪(hydralazine)、吲哒帕胺(indapamide)、别嘌醇、甲醋唑胺(methazolamide)、甲氟喹(meflo-quine)、甲氨蝶呤、甲丙氨酯、汞、米诺地尔、硝苯地平、氮芥、非激素类抗炎药(NSAIDs)、酚酞、吡罗昔康(piroxicam)、黄体酮、典化钾、舒林酸(sulindac)、舒拉明(suramin)、噻苯达唑(thiabendazole )、硫脲嘧啶、茶碱、维拉帕米(verapamil)。
接触物
报春花、长青藤、氯化氨基汞、辣椒素、二硝基氯苯、羟苯甲酮、保泰松、普鲁士黄、松香、醋酸曲安西龙、新霉素、东莨菪碱、核黄素、维生素E、荧光素、硝酸甘油贴、茶碱油、橡胶手套、镍、甲醛、副甲醛、三氯醋酸、砜类衍化物、磺胺、棉籽油、三氯乙酰、秘鲁香脂、细海绵。
内脏疾病
胶原性疾病、血管炎、非霍奇金淋巴瘤、白血病、多发性骨髓瘤、髓样化生、红细胞增多症、新生儿暂时性选择性C4缺之症(transient selective C4 deficiency of infancy)。在相关疾病中,1963年Rowell首先报道红斑性狼疮合并多形红斑样皮疹,后称Rowell综合征(Rowell syndrome),有自身抗体ANA阳性(斑点型)、抗SS-A(Ro)抗体、抗SS-B(La)抗体阳性和类风湿因子阳性。2004年Pandhi报道1例Rowell综合征伴有磷脂综合征,有血小板减少和血凝时间延长等改变。
其他
文身、食物(橙色浆果)、物理因素(放射线、寒冷、日晒)。
以上病因和有关因素中,感染因素最为重要,尤其是单纯疱疹感染最受关注。有50%以上患者在发病前有单纯疱疹病毒感染史。巫毅等对50例多形红斑患者用ELISA法检测血清HSV特异性抗体阳性率为48%。用PCR法测定皮损中HSVDNA阳性率为56%,5例水疱液的HSV分离培养有2例培养出典型HSV。其次为药物因素,尤其重症型病例,应首先考虑药物因素。常见致敏药物为磺胺类药、青霉素类药、非激素抗炎药、抗癫痫药等。陈黎等分析了18例药源性重症多形红斑,指出引起药物以别嘌醇和卡马西平最多见,其次为解热镇痛药和青霉素。
临床症状
前驱症状有头痛、发热、四肢倦怠、食欲不振、关节和肌肉酸痛、扁桃体炎及呼吸道感染等症状。
皮疹多形,有红斑、丘疹、风团、水疱、大疱和紫癜等。根据病变的范围和症状轻重程度,临床上分3型:红斑丘疹型、局限性水疱型和重症型。
红斑丘疹型
为多形红斑轻症型,此型最常见,约占病例的80%,发病与单纯疱疹病毒感染有关,皮疹以红斑、丘疹为主,亦见风团,初起为水肿性红斑或淡红色扁平丘疹,呈圆形,略隆起,境界清楚,数目不定,分布于四肢末端伸侧面,如手、足、前臂伸侧、肘、膝、踝部等,亦见于手掌、足跖部,约有10%的病例皮疹泛发,累及躯干部位,偶见皮疹呈偏侧或沿Blaschko线分布。单个皮疹呈离心性向外扩大,1~2日内红斑直径可达1~3cm。充分发展的红斑可形成靶形损害(下图)。典型的形损害由3带组成,内带为中央部位,略凹陷,颜色深,呈暗红色或紫红色,有时为紫癜或水疱;中带为水肿性隆起,色淡;外带为淡红色斑,境界清楚。缺少任何一带均称不典型靶形损害。多形红斑除有典型皮疹外,有时还出现环状、多环状、弓形红斑。皮疹经光照后可加重。本病可出现Koebner现象(同形反应),有轻度瘙痒,黏膜损害轻,常局限于口腔黏膜,表现红斑、水疱和糜烂,本型无显著全身症状。
手背、前臂、水肿性红斑,边缘部呈暗红色,中央有水疱或紫癜,即所谓靶样损害
局限性水疱型
介于轻症和重症型之间。皮疹以水疱为主,红斑中央有水疱或红斑为水疱围绕,皮疹数目不多,局限于四肢末端部位,有黏膜损害。
重症型
多形红斑重症型(erythema multiforme major),发病前有前驱症状,经1~13天后,突然发病,红斑数目多,主要分布于四肢,常扩散至躯干,有多数典型的靶形损害,有发热等全身症状,黏膜损害严重,可累及2个部位的黏膜,常见口腔黏膜充血、水疱、糜烂、溃疡,严重时影响饮食和张口活动。眼部黏膜充血、水肿,有畏光、流泪。肛门、外生殖器部位黏膜可出现水疱、糜烂、结痂。全身浅表淋巴结肿大。
多形红斑除以上临床型外,尚有以下特殊类型:
- 持久性多形红斑(persistent erythema multiforme):指红斑一直保持初发状态,发展缓慢,可长久不变,病程可达数月,对常规治疗有抵抗;
- 复发性多形红斑(recurrent erythema multiforme):皮损反复发作,病程可持续多年,多数与单纯疱疹病毒感染相关;
- 慢性口腔多形红斑:多形红斑局限于口腔,或以口腔黏膜损害为主,兼有皮损,常反复发作,口腔所有部位均可累及,常见于舌、齿龈、颊黏膜,表现不同程度红斑、糜烂和深在性出血性大疱,尚可伴有其他部位黏膜损害。
实验室检查:重症病例白细胞计数增高,血沉增快,氨基移换酶轻度升高,电解质紊乱,肝、肾功能异常。感染时糜烂面分泌物培养及血培养可阳性。
组织病理
分真皮型、表皮型和混合型。
- 真皮型:真皮乳头显著水肿,可形成表皮下水疱,真皮上部血管扩张,内皮细胞肿胀,血管周围有淋巴细胞、组织细胞浸润,可见少量嗜酸性粒细胞和嗜中性粒细胞。
- 表皮型:表皮内个别角质形成细胞坏死,呈深红色,核固缩或消失,基底层液化变性,真表皮分离,可形成表皮下水疱。
- 混合型:多数病例为真表皮型混合存在,真表皮连接处有淋巴细胞浸润和基底细胞液化变性,形成界面皮炎,严重时形成表皮下水疱,表皮水肿,有海绵形成,有时见表皮内小水疱和细胞外移,有少数角质形成细胞坏死。
真皮上部水肿,有红细胞外溢,但无嗜中性粒细胞、核尘等血管炎改变。以上改变与取材皮损部位有关,形损害中心区表现为表皮型变化,边缘区表现为真皮型变化。
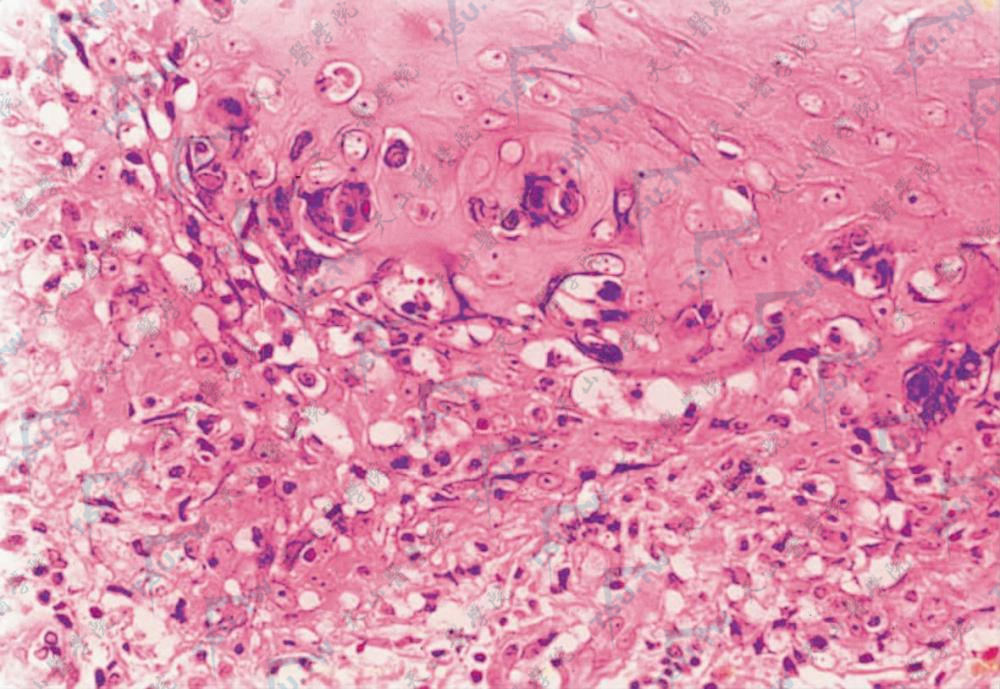
表皮下部多个角质形成细胞坏死,伊红色深染。界面空泡变性,有炎细胞浸润(HE染色×400)
诊断及鉴别
本病皮疹多形,有典型的靶形损害,好发于四肢末端,对称分布,有黏膜损害,重症者有发热等全身症状,组织病理上有个别角质形成细胞坏死,合并HSV感染时皮损部位HSV抗原检测阳性,需与以下疾病鉴别:
- 离心性环状红斑:红斑环状、多环状,缺乏典型的靶形皮损,常无黏膜损害,组织病理上表皮无角质形成细胞坏死。
- 寻常性天疱疮:皮疹以大疱为主,尼氏征阳性,无靶形皮损,组织病理上表皮有棘刺松解现象,疱腔内有棘刺松解细胞,直接免疫荧光检查显示表皮内有IgG细胞间抗体。
- 固定性药疹:红斑孤立存在,好发于皮肤黏膜交界处和体孔周围,消退后留色素沉着,有服药史。
- 移植物抗宿主反应:急性期皮肤出现红斑、丘疹,红斑融合成片,有水疱,无典型的靶形损害,黏膜损害不明显。慢性期出现苔藓样反应和硬皮病样皮肤改变。
- 急性全身性发疹性脓疱病:为药物引起的过敏反应,初期出现猩红热样皮疹,迅速出现多数小脓疱,可出现水疱、紫癜和不典型靶形皮损,水疱尼氏征阳性,亦有黏膜损害,与重症型多形红斑相似,但前者有广泛性小脓疱,组织病理上表皮内有海绵状脓疱,真皮乳头内有嗜中性粒细胞聚集,无单个角质形成细胞坏死。
- Stevens-Johnson综合征(SJS):与多形红斑的区别在于皮损范围和严重程度不同,SJS更为严重,皮损不仅在四肢,而且可广泛地累及躯干部、面部,出现紫癜性斑片和不典型的靶形损害。黏膜损害更广泛,至少累及2个部位以上的黏膜。眼部黏膜病变严重可致失明。
治疗
病因治疗:病因明确者,针对病因治疗。
局部治疗:对皮损应用清洁、保护、止痒、温和消炎剂,如植物油、炉甘石洗剂、氧化锌油剂、硅油霜、糖皮质激素软膏等。口腔病变应用含漱剂,保持口腔清洁。眼部病变及早请眼科会诊,协同处理,防止产生后遗症。肛门、尿道口及外生殖器部位可用0.05%氯己定液清洁,有感染时及时应用抗生素。
全身治疗:
- 口服抗组胺类药、多种维生素,重症者补充水分和营养,保持水、电解质的平衡。
- 对重症型病例系统应用糖皮质激素治疗意见不一,有认为应用激素可增加并发症,使单纯疱疹病毒等感染扩散,不宜应用。但有的认为对重症型病例早期、短程、系统应用糖皮质激素可及时控制病情发展,减轻症状和缩短病程,应用时要注意其副作用。陈黎等报道18例药源性重症型多形红斑,强调早期应用中等至大剂量糖皮质激素(甲泼尼龙40~80mg/d,静脉滴注)。
- 重症型病例可静脉注射免疫球蛋白治疗,尤其适用于糖皮质激素疗效不佳或有糖皮质激素禁忌证者。陈黎等应用静脉注射免疫球蛋白剂量为0.4g/(kg·d),连用4~5日。
- 其他疗法:包括应用左旋咪唑、环磷酰胺、环孢素、氨苯砜、沙利度胺等。
预防:对合并疱疹病毒感染的多形红斑,可应用阿昔洛韦治疗单纯疱疹,或预防其复发。Tatnall等对20例复发性多形红斑(每年复发4次以上)病例,进行双盲对照试验,治疗组服用阿昔洛韦400mg,每日2次,连续6个月,治疗期间未见复发,对比安慰剂组有显著性差异,其研究提示连续性应用阿昔洛韦治疗可以完全抑制发作,有些病例可以达到疾病缓解。
