亚急性甲状腺炎(subacute thyroiditis)主要分为亚急性肉芽肿性和亚急性淋巴细胞性甲状腺炎两型,两型均为亚急性临床过程,均与免疫因素有关,但亚急性淋巴细胞性甲状腺炎的本质为一种自身免疫性甲状腺炎,本篇先说说亚急性肉芽肿性甲状腺炎。
亚急性肉芽肿性甲状腺炎最早于1904年由de Quervain描述。此后,涉及的名称有肉芽肿性巨细胞性甲状腺炎(granulomatous giant cell thyroiditis)、巨细胞性甲状腺炎(giant cell thyroiditis)、亚急性疼痛性甲状腺炎(subacute painful thyroiditis)和de Quervain甲状腺炎等。本病多见于中年及年轻女性,女性多于男性。女性与男性之比3∶1。Iitaka等报道,3344例本病患者的年龄为14~75岁,发病高峰在44~49岁,男女之比为1∶9.7。
发病与病毒感染相关
本病的病因未明。一般认为与病毒感染有关,多数患者于上呼吸道感染后发病。发病时,患者血清某些病毒抗体滴度升高,并有柯萨奇病毒、EB病毒、腺病毒、流感病毒和腮腺炎病毒等感染的依据。当腮腺炎流行时造成流行性甲状腺炎,患者血清中有高滴度的抗腮腺炎病毒抗体,但在受累的甲状腺组织内,仅2例甲状腺组织培养出腮腺炎病毒。患者对病毒存在遗传易感性与HLA-B35相关。近年发现,本病患者循环中存在直接针对TSHR的抗体,并证实存在针对甲状腺抗原的致敏T淋巴细胞,所以本病病因不能完全以病毒感染来解释,是否有自身免疫异常,尚无定论。
亚急性甲状腺炎和自身免疫性甲状腺炎的主要环境因素是病毒感染。亚急性甲状腺炎主要可能与反转录病毒和腮腺炎病毒感染有关,Graves病可能与反转录病毒(HTLV-1、HFV和SV40)有关,慢性淋巴细胞性甲状腺炎可能主要与反转录病毒HTLV-1、肠病毒、风疹病毒、腮腺炎病毒、EB病毒和细小病毒(parvovirus)有关。
滤泡破坏和炎症细胞浸润伴肉芽肿形成是本病的病理特征
甲状腺滤泡上皮细胞的破坏及滤泡完整性的丧失是本病病理生理的主要结局。已经生成的TH与异常的碘化物一起从滤泡释放入血中,使血清T4及T3升高,TSH下降,临床上出现甲亢表现。由于滤泡上皮细胞的破坏,TSH不能增加对放射性碘的摄取,致使放射性碘摄取率减低。在疾病的后期,滤泡内贮存的激素已排尽,血T4及T3下降,有时可降至甲减水平,而TSH常高于正常。如病情不再活动,甲状腺摄碘率可高于正常一段时间,最终随着激素分泌的恢复,血T3、T4和TSH正常。
甲状腺通常中度结节状肿大,常不对称,病变可局限于甲状腺的一部分,累及一侧或双侧甲状腺。包膜纤维组织增生,并和周围组织粘连,但很少侵及甲状腺附近器官。甲状腺质地较硬,有弹性,切面灰白色或浅黄色。病变与周围甲状腺分界清楚。镜下病变呈灶性分布,范围大小不一,各处病变处于不同的病变阶段。早期可见滤泡破坏,上皮细胞崩解、基底膜碎裂,类胶质减少或消失。中性粒细胞浸润,形成微小脓肿。病变进一步发展,可见组织细胞和多核巨细胞位于滤泡内,围绕胶质形成肉芽肿。上皮样细胞与多核巨细胞构成结核样肉芽组织,但无干酪样坏死。
在肉芽肿形成期,单核/巨噬细胞进入滤泡腔,产生血管内皮细胞生长因子(VEGF)、碱性成纤维细胞生长因子(bFGF)、血小板衍生生长因子(PDGF)、转化生长因子-β (TGF-β)和上皮细胞生长因子(EGF),激发肉芽肿形成;而在恢复期,EGF增加而TGF-β减少有助于滤泡形成,而VEGF 和bFGF升高有助于血管形成。细胞凋亡亦参与本病的发生,Bax表达促进甲状腺滤泡细胞增殖。
本病经数月后,炎症逐渐消退,最后纤维化而痊愈。病灶之间可见新生的小滤泡,腔内无胶质。上皮细胞呈立方或低柱状,有的含有胶质和吸收空泡,也可见中等或较大的甲状腺滤泡,胞内有胶质。上皮细胞呈立方或扁平状。
上呼吸道感染后甲状腺疼痛及TH与摄131I率分离支持诊断
本病多见于中年女性,发病有季节性(如夏季是其发病的高峰季节)。患者起病时常有上呼吸道感染的表现。典型病例可分为早期(伴甲亢)、中期(伴甲减,分过渡期和甲减期两期)以及恢复期(甲状腺功能正常)3期。
早期
起病多急骤,常伴有上呼吸道感染症状和体征,如发热、畏寒、疲乏无力和食欲不振,淋巴结肿大。最为特征性的表现是甲状腺部位的疼痛和压痛,常向颌下、耳后或颈部等处放射,咀嚼和吞咽时疼痛加重。甲状腺病变范围不一,可先从一叶开始,以后扩大或转移到另一叶,或始终限于一叶。病变腺体肿大,坚硬,压痛显著。少数患者首先表现为无痛性硬结节。病变广泛时,滤泡内的TH和碘化蛋白大量释放入血,因而可伴有甲亢的表现,如一过性心悸和神经过敏等,但通常不超过2个月。
在临床上,发热伴颈前疼痛与压痛强烈提示亚急性甲状腺炎可能;但是患者就诊时,往往已经度过急性期或因为发热与疼痛轻微而被忽视,因而病史询问是诊断本病的最重要依据。依据甲状腺肿大、疼痛、压痛伴全身症状,发病前上呼吸道感染史,血沉增快,血清T3、T4升高而甲状腺摄131I率降低(分离现象),诊断不难确定。Ito医院提出本病的诊断标准为:①甲状腺肿大、疼痛、质硬、触痛,常伴上呼吸道感染症状和体征(发热、乏力、食欲不振、颈部淋巴结肿大等);②血沉加快;③甲状腺摄131I率受抑制;④一过性甲亢;⑤血TgAb或TPOAb阴性或滴度较低;⑥甲状腺细针穿刺或活检有多核巨细胞或肉芽肿改变。
甲亢期血沉增快和T3/T4升高与摄131I率降低是本病的突出特征,其具体表现是:①一般检查:血白细胞计数轻至中度增高,中性粒细胞正常或稍高,偶见淋巴细胞增多,血沉明显增快(≥40mm/h,可达100mm/h);呼吸道病毒抗体滴度增高,一般6个月后逐渐消失。②甲状腺功能:甲亢期血清TT3、TT4、FT3和FT4升高,TSH分泌受抑制,甲状腺摄131I率降低,呈“分离现象”。这是由于甲状腺滤泡细胞破坏,贮存的T3、T4漏入血液循环,使血T3、T4升高,反馈抑制垂体分泌TSH,甲状腺摄碘功能减退;其次,炎症损害滤泡细胞摄碘功能。因此在甲亢期,甲状腺摄131I率可低至测不出;甲减期血清TT3、TT4、FT3和FT4减低,TSH升高,甲状腺摄131I率呈反跳性升高。③彩色多普勒超声:在急性阶段,增大的甲状腺组织血流不增加伴有低回声区;恢复阶段显示轻微血流增加的等回声区;一般1年以后血流恢复正常。④甲状腺扫描:可见图像残缺或显影不均匀,一叶肿大者常见无功能结节或一叶残缺。⑤甲状腺活检:可见特征性多核巨细胞或肉芽肿样改变。
中期
中期亦称过渡期。本病多为自限性,大多持续数周至数月可完全缓解,少数患者可迁延1~2年,个别留有永久性甲减。当甲状腺滤泡内TH由于感染破坏而发生耗竭,甲状腺实质细胞尚未修复前,血清TH可降至甲减水平。99mTc扫描可见甲状腺呈普遍放射性稀疏,边缘不规整,颌下腺显浓影(下图)。但大部分患者不出现临床型甲减表现,经历甲亢期后,可由过渡期直接进入恢复期。少数患者出现甲减表现(2~4个月),其后甲状腺功能逐渐恢复正常。个别患者由于甲状腺损坏严重,遗留有永久甲减。约1/3的患者留有结节性甲状腺肿。

亚急性甲状腺炎(99mTc);注:甲状腺呈普遍放射性稀疏,边缘不规整,颌下腺显浓影
恢复期
症状渐好转,甲状腺肿或及甲状腺结节逐渐消失;有些病例遗留小结节,以后缓慢吸收。如果治疗及时,患者多可完全恢复。极少数演变成永久性甲减。本病各期的甲状腺功能改变见下表。
亚急性肉芽肿性甲状腺炎不同病期的表现
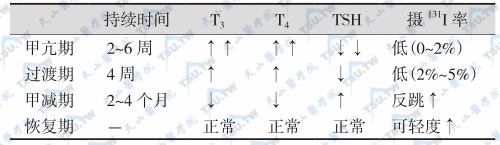
注:↑:升高;↑↑:明显升高;↓:下降;↓↓:明显下降
反复发作后遗留炎性结节或永久性甲减
轻症或不典型病例的甲状腺仅略增大,疼痛和压痛轻微,不发热,全身症状轻,临床上无甲亢或甲减表现。自数周至半年(一般2~3个月)后痊愈。反复发作病例在病情缓解后,又反复发作。留有结节性甲状腺肿或炎性甲状腺结节的患者可表现为持续性TPOAb/TgAb阳性或反复发作性甲亢。Iitaka对3344例亚急性甲状腺炎患者进行24年随访,发现在第1次发病完全康复后(14.5±4.5)年内有48例第2次复发;第2次发病后(7.6±2.4)年内有5例第3次发病。但复发病例的临床表现及实验室检查结果较初发病例轻,病程持续时间也较短。反复发作病例多遗留有甲状腺结节或永久性甲减。
个别病例可形成所谓的慢性隐匿型甲状腺炎(silent thyroiditis),发作期的症状很轻,发作的持续时间一般为4~6个月,发作时的主要表现为血T3、T4升高,TSH降低和TgAb 和TPOAb阳性,TH治疗多无效,必要时应采用131I治疗。
排除甲状腺囊肿/结节出血/亚急性淋巴细胞性甲状腺炎/其他甲状腺疾病
颈前包块伴有疼痛者除本病外,还可见于甲状腺囊肿或腺瘤样结节急性出血、甲状腺癌急性出血、急性化脓性甲状腺炎、迅速长大的甲状腺癌、疼痛性桥本甲状腺炎、甲状舌骨导管囊肿感染、支气管腮裂囊肿感染和颈前蜂窝组织炎等,需注意鉴别。但亚急性甲状腺炎、甲状腺囊肿或腺瘤样结节急性出血占全部病例的90%以上。
如果鉴别特别困难,可试用糖皮质激素治疗数日,协助诊断;亚急性甲状腺炎所致的甲状腺疼痛对糖皮质激素的反应相当敏感,一般用药的当日或次日即可收到明显止痛效果。反之,如果糖皮质激素治疗无效或效果很差时,基本可以排除亚急性甲状腺炎可能。
甲状腺囊肿或腺瘤样结节急性出血:用力活动后常骤然出现甲状腺疼痛,甲状腺局部有波动感,血沉和甲状腺功能正常,超声包块内有液性暗区。
亚急性淋巴细胞性甲状腺炎:见后述。不伴甲状腺的疼痛或压痛,但可反复发作(10%~15%);无病毒感染前驱症状,很少有病毒抗体滴度改变,血沉大多正常;甲状腺活检示淋巴细胞性甲状腺炎改变。
甲状腺肿瘤:甲状腺肿瘤很少出现局部疼痛,但当肿瘤发生出血坏死或压迫神经时,疼痛可能成为患者的就诊原因。当与亚急性甲状腺炎鉴别困难时,应行B超或MRI检查。如果诊断仍有困难,亦可用糖皮质激素治疗试验进行鉴别。
甲状腺的其他疾病:急性发作型桥本甲状腺炎也可伴轻微甲状腺疼痛和触痛,但较少见,一般不伴明显的碘代谢紊乱和血沉加速,血TgAb或TPOAb显著升高。细针穿刺细胞学示自身免疫性甲状腺炎改变,但无巨细胞。急性化脓性甲状腺炎多见于上呼吸道感染后,起病急,可有畏寒、寒战、发热、心动过速;甲状腺有肿胀和触痛,颈前区可出现炎症浸润性硬结。末梢血白细胞计数升高,以多形核白细胞为主,血培养可为阳性,血沉加快。甲状腺扫描显像可见局部有放射性减低区。细针穿刺细胞学检查可抽吸出脓汁,镜检见大量的脓细胞、坏死细胞及组织碎屑。抗生素治疗有效,不引起甲减。如未经治疗,脓肿可向周围组织穿破而出现纵隔脓肿或气管/食管瘘。甲状腺癌患者的甲状腺呈局限性肿大,且无明显症状,扫描可为冷结节,需与甲状腺癌鉴别。但本病的疼痛可自行缓解或迅速波及对侧,血沉快,摄131I率低,应用泼尼松治疗疗效显著,可资鉴别。必要时,甲状腺穿刺活检有助于鉴别。
Riedel甲状腺炎(Riedel thyroiditis)为一种罕见的慢性甲状腺炎,其病变以纤维炎症过程(fibroinflammatory process)、甲状腺实质和周围组织被破坏与侵袭为特征,发病可能主要与IgG4的免疫损害有关,因而认为Riedel甲状腺炎属于IgG4相关性硬化性疾病(IgG4-related sclerosing diseases,IgG4-RSD)的一种表现。但是有些患者在病情进程中有反复发作表现,可酷似亚急性甲状腺炎或与亚急性甲状腺炎合并存在,或以前有过亚急性甲状腺炎病史。故应注意鉴别。
对症处理和特殊治疗
一般治疗和对症治疗
症状较轻者不需特殊处理,可适当休息,并给以非甾体类消炎镇痛剂。阿司匹林0.5~1.0g或吲哚美辛(消炎痛)25mg,每日3~4次,疗程约2周。对于疼痛剧烈或顽固性疼痛患者,新一代的环氧化酶-2抑制剂(cyclooxygenase 2 inhibitor)依托考昔(etoricoxib,120mg/d,每日1次)的止痛和抗炎效果较佳。
糖皮质激素治疗
糖皮质激素具有抗炎和缩短甲亢期的病程等作用。全身症状较重、持续高热,甲状腺肿大伴压痛明显者,可采用糖皮质激素治疗。首选泼尼松20~40mg/ d,在治疗后数小时即可缓解疼痛,甲状腺肿大开始缩小,用药1~2周后逐渐减量,疗程1~2个月,但停药后部分患者可能反复,再次用药仍然有效。亦可合用非甾体类消炎镇痛剂,消除疼痛,减少反复。伴甲亢时,不需服用抗甲状腺药物治疗,有些患者可给予小剂量普萘洛尔。如病程较长,有可能发生甲减,对这些患者应考虑加服甲状腺粉40~60mg/d,或L-T4 100~150μg/d,直到甲状腺功能恢复正常为止(一般为3~6个月)。加服甲状腺粉可以加强垂体的反馈调节,减少TSH分泌,有利于甲状腺肿及结节的缩小及症状消除。
部分患者对糖皮质激素治疗的反应不敏感,疗效差,其原因不明,此时要考虑做如下处理:①加用TH制剂或非甾体类抗炎药。②反复发作者可继续使用糖皮质激素,但宜增加原有剂量。③B超检查,了解是否存在甲状腺结节或脓肿。④排除α-干扰素所致的甲状腺炎可能。⑤除甲状腺结节外,其他临床症状和体征均消失者不能认为治疗失败;甲状腺结节可按一般性结节处理,并追踪观察。⑥仅有局部疼痛者,要注意甲状腺结节压迫神经或合并咽喉炎可能,这种情况亦不能认为治疗无效。
甲减的治疗
如有甲减表现,可给予L-T4,但一般应在使用6个月后停用,因为绝大多数甲减可逐渐恢复。如停用L-T4后,再发生甲减,提示为永久性(5%~10%),需终生给予TH替代治疗。
手术治疗
本病一般不需手术治疗,但难治性病例和长期反复发作病例可采用手术切除病灶。
